
Wetenschap
Welke andere stoffen kunnen we in plaats van koperoxide gebruiken bij de bereiding van sulfaat?
1. IJzer(II)sulfide (FeS) :Bij verhitting in aanwezigheid van zuurstof ondergaat ijzer(II)sulfide oxidatie om ijzer(III)oxide en zwaveldioxide te vormen. Het zwaveldioxide kan vervolgens worden omgezet in zwavelzuur, waarmee sulfaten kunnen worden bereid.
2. Zinksulfide (ZnS) :Net als ijzer(II)sulfide kan zinksulfide worden geoxideerd tot zinkoxide en zwaveldioxide. Het zwaveldioxide kan vervolgens worden omgezet in zwavelzuur voor de sulfaatbereiding.
3. Loodsulfide (PbS) :Loodsulfide kan ook worden geoxideerd tot loodoxide en zwaveldioxide. Vanwege de giftige aard van loodverbindingen wordt deze methode echter niet vaak gebruikt.
4. Natriumbisulfiet (NaHSO3) :Natriumbisulfiet is een reductiemiddel dat kan worden gebruikt om zwaveldioxide om te zetten in zwavelzuur. Deze methode wordt vaak gebruikt in industriële processen voor de productie van sulfaat.
5. Calciumsulfaat (CaSO4) :Calciumsulfaat, ook wel gips genoemd, kan gebruikt worden als uitgangsmateriaal voor de bereiding van andere sulfaten. Door calciumsulfaat te laten reageren met natriumcarbonaat (Na2CO3) kan natriumsulfaat (Na2SO4) worden verkregen.
6. Bariumsulfaat (BaSO4) :Bariumsulfaat is een in water onoplosbare verbinding die kan worden gebruikt als uitgangsmateriaal voor de bereiding van andere sulfaten. Door bariumsulfaat te laten reageren met natriumcarbonaat kan natriumsulfaat worden verkregen.
Dit zijn slechts enkele voorbeelden van stoffen die in plaats van koperoxide kunnen worden gebruikt bij de bereiding van sulfaat. De keuze van de stof hangt af van verschillende factoren zoals beschikbaarheid, kosten, reactiviteit en de specifieke vereisten van het gewenste sulfaat.
 Hoe rangschikte Mendelejev de chemische elementen in het periodiek systeem?
Hoe rangschikte Mendelejev de chemische elementen in het periodiek systeem?  Welke massa zuurstof bevat hetzelfde aantal moleculen als 42 g stikstof?
Welke massa zuurstof bevat hetzelfde aantal moleculen als 42 g stikstof?  Coin Corrosion Science Experiments voor kinderen
Coin Corrosion Science Experiments voor kinderen  Nieuwe digitale filterbenadering heeft tot doel chemische metingen te verbeteren
Nieuwe digitale filterbenadering heeft tot doel chemische metingen te verbeteren Collageen in kraakbeenweefsel gedraagt zich als vloeibare kristallen op een smartphonescherm
Collageen in kraakbeenweefsel gedraagt zich als vloeibare kristallen op een smartphonescherm
 Frequent Flyer Levy zou degenen belasten die het luchtverkeer domineren
Frequent Flyer Levy zou degenen belasten die het luchtverkeer domineren  Olympische skiërs en snowboarders strijden op 100% nepsneeuw:heeft dit invloed op de prestaties?
Olympische skiërs en snowboarders strijden op 100% nepsneeuw:heeft dit invloed op de prestaties? Trumps voorgestelde EPA-verlagingen zouden een onvoorstelbare impact hebben, volksgezondheidsdeskundige zegt:
Trumps voorgestelde EPA-verlagingen zouden een onvoorstelbare impact hebben, volksgezondheidsdeskundige zegt: Hoe evolueerden planten voor het eerst in allerlei verschillende vormen en maten? Om daarachter te komen, hebben we een miljard jaar plantengeschiedenis in kaart gebracht
Hoe evolueerden planten voor het eerst in allerlei verschillende vormen en maten? Om daarachter te komen, hebben we een miljard jaar plantengeschiedenis in kaart gebracht  Hoe een klein stadje in Japan zijn donkere lucht fel verdedigt
Hoe een klein stadje in Japan zijn donkere lucht fel verdedigt
Hoofdlijnen
- Maak een lijst van de 3 stappen die optreden tijdens de interfase
- Menselijke resten gevonden in grote Australische krokodil
- Geheime taal van cellen? Nieuwe celberekeningen ontdekt
- Eten en drinken, wat het over ons zegt
- Spin eet spin:wetenschappers ontdekken 18 nieuwe op spinnen jagende pelikaanspinnen in Madagaskar
- Verschillende diëten van bonobogroepen kunnen inzicht bieden in de manier waarop cultuur tot stand komt
- Antibioticaresistentie:onderzoekers slagen erin resistentiegenen te blokkeren
- Ondergrondse schimmelinteracties met bomen helpen bij het verklaren van invasies van niet-inheemse planten
- Hoe regelt het lichaam de hartslag?
- Beschermend membraan voor pacemakers voorkomt ophoping van fibrotisch weefsel

- Neutronenstudie van glaucoommedicijnen biedt aanwijzingen over enzymdoelen voor agressieve kankers

- Video:Hoe chemie de warme chocolademelk kan verbeteren

- Nieuwe mechanismen ontdekt om luchtmoleculen te scheiden
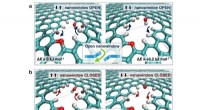
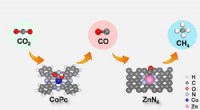
- Tandemkatalysator om de elektroreductie van kooldioxide tot methaan te verbeteren
 Hoe high-tech stoffen je lichaam zullen transformeren
Hoe high-tech stoffen je lichaam zullen transformeren  Gericht op verborgen zak voor behandeling van beroerte en epileptische aanvallen
Gericht op verborgen zak voor behandeling van beroerte en epileptische aanvallen De Gough Map:de vroegste wegenkaart van Groot-Brittannië?
De Gough Map:de vroegste wegenkaart van Groot-Brittannië?  Wetenschappers werken aan een periodiek systeem voor ecologie
Wetenschappers werken aan een periodiek systeem voor ecologie  Wat Cassini's 'grote finale' ons leerde over het binnenste van Saturnus
Wat Cassini's 'grote finale' ons leerde over het binnenste van Saturnus  NIST actualiseert en breidt zijn vlaggenschipcatalogus van informatiesysteembeveiligingen bij
NIST actualiseert en breidt zijn vlaggenschipcatalogus van informatiesysteembeveiligingen bij Antimoon werkt niet in een magnesiumbatterij, maar het is precies wat tin nodig heeft om energie op te slaan
Antimoon werkt niet in een magnesiumbatterij, maar het is precies wat tin nodig heeft om energie op te slaan  Confrontatie kan blanke vooroordelen verminderen, studie vondsten
Confrontatie kan blanke vooroordelen verminderen, studie vondsten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

