
Wetenschap
Hoeveel natriumnitraat wordt geproduceerd als 1,7 g zilver en 1,5 g jodide reageren?
AgNO3 + NaI → AgI + NaNO3
Uit de vergelijking kunnen we zien dat 1 mol zilvernitraat reageert met 1 mol natriumjodide om 1 mol zilverjodide en 1 mol natriumnitraat te produceren.
De molaire massa van zilvernitraat is 169,87 g/mol en de molaire massa van natriumjodide is 149,89 g/mol.
Daarom is 1,7 g zilver gelijk aan 1,7 g / 169,87 g/mol =0,01 mol zilvernitraat.
En 1,5 g natriumjodide is gelijk aan 1,5 g / 149,89 g/mol =0,01 mol natriumjodide.
Omdat de molverhouding tussen zilvernitraat en natriumjodide 1:1 bedraagt, is zilvernitraat de beperkende reactant in dit geval.
Daarom is de maximale hoeveelheid natriumnitraat die kan worden geproduceerd 0,01 mol natriumnitraat.
De molmassa van natriumnitraat is 84,99 g/mol, dus 0,01 mol natriumnitraat is gelijk aan 0,01 mol * 84,99 g/mol =0,85 g natriumnitraat.
Daarom is de hoeveelheid natriumnitraat die wordt geproduceerd wanneer 1,7 g zilver en 1,5 g jodide reageren 0,85 g.
Hoofdlijnen
- Onderzoekers laten zien hoe probiotica de immuniteit van planten versterken
- Wat betekent microscoopveld in de wetenschap?
- Orgelsystemen die betrokken zijn bij homeostase
- Onderzoekers tonen een nieuwe holistische benadering van genetica en plantenveredeling
- Welke cellen zou je gebruiken om DNA van een levende persoon te extraheren?
- Hoe een cellenvorm zijn functie beïnvloedt
- Welk type organisch macromolecuul is glucose?
- Eerder onbekend slaapmuizenhabitat geïdentificeerd
- De taal van cellulaire communicatie begrijpen
- Een Trojaanse paardenbenadering kan leiden tot behandelingen voor sommige antibioticaresistente bacteriën
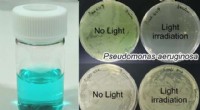
- Wetenschappers ontwerpen nieuw responsief poreus materiaal geïnspireerd op eiwitten

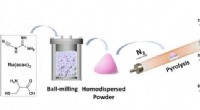
- Nieuwe katalyse met één atoom zorgt voor reductieve amineringsreactie
- Nieuwe geleidende coating kan de biometrische en draagbare technologie van de toekomst ontsluiten

- Onderzoekers creëren een nieuw akoestisch slim materiaal geïnspireerd op haaienhuid

 Bill wil miljarden uitgeven om verouderde dammen in landen te repareren
Bill wil miljarden uitgeven om verouderde dammen in landen te repareren Hoe zwarte dozen werken
Hoe zwarte dozen werken  Micron brengt microchipfabriek naar de staat New York
Micron brengt microchipfabriek naar de staat New York Meelkracht om voedselzekerheid te vergroten
Meelkracht om voedselzekerheid te vergroten Griekenland opnieuw getroffen door hoge temperaturen, Saharastof
Griekenland opnieuw getroffen door hoge temperaturen, Saharastof  Einde van het e-mailtijdperk? Ik koop het niet
Einde van het e-mailtijdperk? Ik koop het niet  430 miljoen jaar oude uitgestorven stekelhuidigen gevonden in Engeland
430 miljoen jaar oude uitgestorven stekelhuidigen gevonden in Engeland Duinen gevangen in een krater op Mars vormen dit interessante patroon
Duinen gevangen in een krater op Mars vormen dit interessante patroon
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


