
Wetenschap
Kan een neutraal ongebonden atoom het valentie-octet voltooien?
Een neutraal, niet-gebonden atoom kan een volledig valentieoctet bereiken als het een stabiele elektronenconfiguratie bereikt. Dit kan worden bereikt door elektronen te winnen of te verliezen totdat de buitenste elektronenschil van het atoom volledig gevuld is, wat meestal uit acht elektronen bestaat. Atomen met een compleet valentieoctet hebben edelgassenconfiguraties en zijn over het algemeen stabiel en niet-reactief.
Neem bijvoorbeeld het natriumatoom (Na), dat een neutrale toestand heeft. Natrium heeft één valentie-elektron in zijn buitenste 2s-orbitaal met de elektronische configuratie 2s^1. Om een compleet valentieoctet te verkrijgen, kan het natriumatoom zijn 2s-elektron verliezen, wat resulteert in de vorming van +1 kation met een stabiele elektronenconfiguratie van Ne, 1s^22s^22p^6.
 Deeltjes die kleiner zijn dan een atoom
Deeltjes die kleiner zijn dan een atoom  Afstemmingsstrategieën en structuureffecten van elektrokatalysatoren voor de koolstofdioxidereductiereactie
Afstemmingsstrategieën en structuureffecten van elektrokatalysatoren voor de koolstofdioxidereductiereactie Wat is de uitgebalanceerde vergelijking voor de verbranding van heptaan in reactie met zuurstof?
Wat is de uitgebalanceerde vergelijking voor de verbranding van heptaan in reactie met zuurstof?  Wetenschappers suggereren een nieuwe methode voor het synthetiseren van een veelbelovend magnetisch materiaal
Wetenschappers suggereren een nieuwe methode voor het synthetiseren van een veelbelovend magnetisch materiaal Hoe dichtheidsmetingen te beschrijven?
Hoe dichtheidsmetingen te beschrijven?
 Onderzoek vindt ruimte voor verbetering in het vervuilde stroomgebied van Zuid-Korea
Onderzoek vindt ruimte voor verbetering in het vervuilde stroomgebied van Zuid-Korea Waarom de VS 17 jaar terugkijkt om hun klimaatdoelen vast te stellen
Waarom de VS 17 jaar terugkijkt om hun klimaatdoelen vast te stellen Waarom hout drijft in water?
Waarom hout drijft in water?  AP Was There:Het tijdperk van klimaatverandering begint
AP Was There:Het tijdperk van klimaatverandering begint Hoe Duitsland uiteindelijk de lichten uitdoet in de zwarte kolenmijn
Hoe Duitsland uiteindelijk de lichten uitdoet in de zwarte kolenmijn
Hoofdlijnen
- Hoe nitraat de genexpressie in peulvruchten reguleert
- Luie valsspeler leeft onder de grond,
- Uitbreiding tonijnquota stap achteruit voor instandhouding
- Internationaal onderzoek geeft inzicht in hoe fibrose kan beginnen en verwoestend kan worden in verschillende lichaamsweefsels
- Stop en ga in het kaliumkanaal
- Onderzoek naar koeiengenen laat zien waarom de meeste klonen falen
- Van goot naar darm:hoe antimicrobieel resistente microben van de omgeving naar de mens reizen
- Waarom zou een verandering in de DNA-sequentie dat organisme veroorzaken?
- Het schapengenoom:onderzoek laat zien hoe schapen zich voor het eerst van geiten scheidden
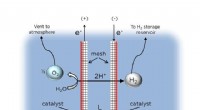
- Ingenieurs ontwikkelen drijvende boorinstallatie voor zonne-energie voor elektrolyse van zeewater
- Lasertechnieken en fotochemie vinden ongrijpbare moleculaire bouwsteen
- Nanocontainers voor gerichte medicijnafgifte

- NRL pigmentpakket voor schepen vertraagt verkleuring, verlaagt de belasting van de zonnetemperatuur

- Voorspelling van de vervorming en prestaties van onderdelen gemaakt door additieve fabricage

 Zaterdagcitaten:Honden prijzen; de evolutie van bruin vet; hoe SSRI's depressie verlichten. Plus:Boeings Starliner
Zaterdagcitaten:Honden prijzen; de evolutie van bruin vet; hoe SSRI's depressie verlichten. Plus:Boeings Starliner  Biologisch afbreekbare bruggen:levende structuren die reageren op de omgeving
Biologisch afbreekbare bruggen:levende structuren die reageren op de omgeving Kan de kleur van licht de kristalgroei beïnvloeden?
Kan de kleur van licht de kristalgroei beïnvloeden?  Het verzorgen van Bobwhite kwartelkuikens
Het verzorgen van Bobwhite kwartelkuikens  Werkzoekenden in de chemie hebben moeilijke vooruitzichten tijdens pandemie
Werkzoekenden in de chemie hebben moeilijke vooruitzichten tijdens pandemie Tijdens de meiose resulteert het proces van oversteken in nieuwe combinaties van allelen omdat?
Tijdens de meiose resulteert het proces van oversteken in nieuwe combinaties van allelen omdat?  Studie geeft nieuw inzicht in hoe klimaatverandering de barrière-eilanden van Virginia transformeert
Studie geeft nieuw inzicht in hoe klimaatverandering de barrière-eilanden van Virginia transformeert  Metaal vereenvoudigt de synthese van antilichaamgeneesmiddelen
Metaal vereenvoudigt de synthese van antilichaamgeneesmiddelen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

