
Wetenschap
Wat is de Lewis-structuur van CH3COH?
Om de Lewis-structuur van CH3COH te tekenen, moeten we eerst het totale aantal valentie-elektronen in het molecuul bepalen. Koolstof heeft vier valentie-elektronen, waterstof heeft één valentie-elektron en zuurstof heeft zes valentie-elektronen. Het totale aantal valentie-elektronen in CH3COH is daarom:
$$\text{Totale valentie-elektronen} =(4 \maal 1) + (3 \maal 1) + (1 \maal 6) =14$$
Vervolgens moeten we de atomen met elkaar verbinden met enkele bindingen. We beginnen met het verbinden van het koolstofatoom met de drie waterstofatomen en het zuurstofatoom. Dit geeft ons de volgende structuur:
```
H H H
| | |
C - O - H
|
H
```
Vervolgens voegen we aan elk atoom losse elektronenparen toe, zodat elk atoom een compleet octet aan elektronen heeft. Dit geeft ons de volgende Lewis-structuur:
```
H H H
| | |
C - O - H
| |
H :
```
In deze Lewis-structuur heeft het koolstofatoom vier bindingen (drie enkele bindingen en één dubbele binding) en heeft het een compleet octet aan elektronen. Het zuurstofatoom heeft twee bindingen (een enkele binding en een dubbele binding) en heeft een compleet octet aan elektronen. De waterstofatomen hebben elk één binding en een compleet duet van elektronen.
 Waarom exploderen azijn en zuiveringszout als ze met elkaar gemengd worden?
Waarom exploderen azijn en zuiveringszout als ze met elkaar gemengd worden?  Wat maakt wijn droog? Het is gemakkelijk te proeven, maar veel moeilijker te meten
Wat maakt wijn droog? Het is gemakkelijk te proeven, maar veel moeilijker te meten Doorbraak in de niet-oxidatieve koppeling van methaan:directe omzetting in propyleen bij lage temperatuur
Doorbraak in de niet-oxidatieve koppeling van methaan:directe omzetting in propyleen bij lage temperatuur  Wat gebeurt er als kopersulfaat oplost in water?
Wat gebeurt er als kopersulfaat oplost in water?  Ingenieurs produceren op additieve wijze elektriciteitspalen van biologisch afgeleide en gerecyclede materialen
Ingenieurs produceren op additieve wijze elektriciteitspalen van biologisch afgeleide en gerecyclede materialen
 Niet op één lijn:hoe botsend beleid verschrikkelijke gevolgen voor het milieu heeft
Niet op één lijn:hoe botsend beleid verschrikkelijke gevolgen voor het milieu heeft  Wie is groener? Mijngevecht zet elektrische auto's tegenover bloem
Wie is groener? Mijngevecht zet elektrische auto's tegenover bloem  Nieuwe analyse doet twijfel rijzen over de voorspelde afname van aardbevingen in Oklahoma
Nieuwe analyse doet twijfel rijzen over de voorspelde afname van aardbevingen in Oklahoma Rapport roept op tot verbeterde methoden om door aardbevingen veroorzaakte bodemvervloeiing te beoordelen
Rapport roept op tot verbeterde methoden om door aardbevingen veroorzaakte bodemvervloeiing te beoordelen NASA onderzocht regenval in orkaan Michael terwijl deze zich ontwikkelde
NASA onderzocht regenval in orkaan Michael terwijl deze zich ontwikkelde
Hoofdlijnen
- Onderzoek modelleert hoe dodelijk virus zich verplaatst onder Pacifische zalm en forel
- In meercellige organismen zijn er verschillende soorten cellen die zich in weefsels en organen hebben georganiseerd om speciale functies uit te voeren. Wat is de functie van een huidcel?
- Gedragstherapie tegen veroudering:Onderzoekers bestuderen het effect van therapieën op oudere honden
- Hoe de mondialisering menselijke parasieten virulenter zou kunnen maken
- Engels domineert wetenschappelijk onderzoek. Hier leest u hoe we dit kunnen oplossen en waarom het ertoe doet
- Nieuw onderzoek lost een van de meest verhitte geschillen over evolutionaire biologie op robuuste wijze op
- Verschillen mannelijke en vrouwelijke dinosaurussen? Een nieuwe statistische techniek helpt bij het beantwoorden van de vraag
- Baby-orang-oetan geboren in Tampas Busch Gardens via keizersnede is een zeldzame prestatie
- Ben jij een zoetekauw? Honingbijen klauwen
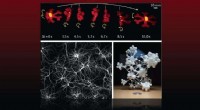
- Onderzoekers brengen de voortgang in kaart van ontworpen materialen die reageren op externe prikkels
- Metaal-organische raamwerken kunnen ondanks de aanwezigheid van water gassen scheiden

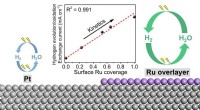
- Nieuwe mechanismen voor verbetering van de activiteit van bimetaalkatalysatoren voor waterstofopwekking en brandstofcellen
- Warmtegeleidend plastic kan leiden tot lichtere elektronica, auto's

- Upcycling van plastic zakken tot batterijonderdelen

 Rood licht voor stress:een van kleur veranderend organisch kristal
Rood licht voor stress:een van kleur veranderend organisch kristal Vereiste chemische reacties om homeostase te handhaven
Vereiste chemische reacties om homeostase te handhaven Techniek combineert op licht gebaseerde analytische methoden met microfluïdische monsterverwerking voor de diagnose van pathogenen
Techniek combineert op licht gebaseerde analytische methoden met microfluïdische monsterverwerking voor de diagnose van pathogenen Een nieuwe interpretatie van petrogenese van de vroege continentale korst van de aarde
Een nieuwe interpretatie van petrogenese van de vroege continentale korst van de aarde Europese technologieleiders waarschuwen voor EU-belasting op digitale diensten
Europese technologieleiders waarschuwen voor EU-belasting op digitale diensten Verbeterde voorspelling van residuen van bestrijdingsmiddelen
Verbeterde voorspelling van residuen van bestrijdingsmiddelen Verbetering van de prestaties van een thermo-elektrisch materiaal door selectieve atomen gedeeltelijk te vervangen door kationen
Verbetering van de prestaties van een thermo-elektrisch materiaal door selectieve atomen gedeeltelijk te vervangen door kationen Het dragen van tasers verhoogt het gebruik van geweld door de politie, studie vondsten
Het dragen van tasers verhoogt het gebruik van geweld door de politie, studie vondsten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

