
Wetenschap
Hoe water de assemblage van collageen, de bouwsteen van alle mensen, begeleidt
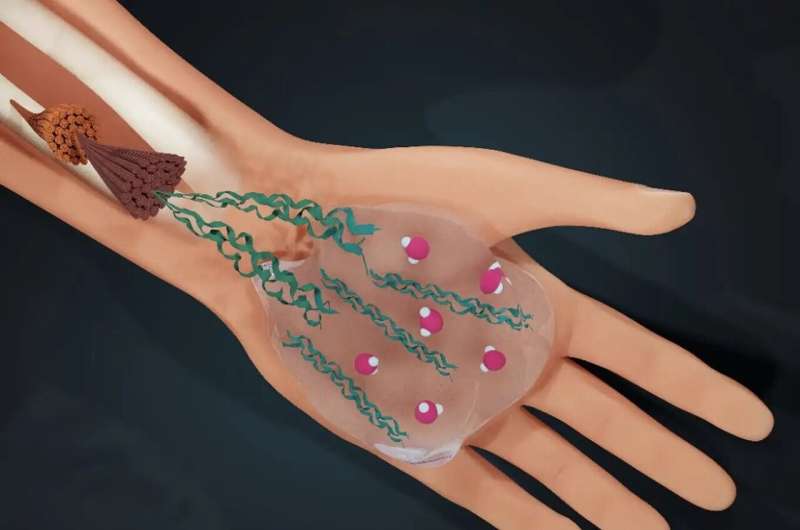
Water bepaalt het leven:de mens bestaat voor driekwart uit water. Een internationaal onderzoeksteam onder leiding van de Universiteit van Amsterdam (UvA) heeft nu ontdekt hoe water ook de structuur bepaalt van het materiaal dat ons bij elkaar houdt:collageen.
In een artikel gepubliceerd in PNAS , verduidelijken de onderzoekers de rol van water in de moleculaire zelfassemblage van collageen. Ze laten zien dat door water te vervangen door zijn 'tweelingmolecuul' zwaar water (D2 O), kan men de interactie tussen collageenmoleculen 'afstemmen' en zo het proces van zelfassemblage van collageen beïnvloeden. De bevindingen zullen helpen om het weefselfalen als gevolg van erfelijke collageengerelateerde ziekten, zoals de ziekte van broze botten (osteogenesis imperfecta), beter te begrijpen.
Zoals hoofdauteur dr. Giulia Giubertoni van het Van 't Hoff Institute for Molecular Sciences (HIMS) van de UvA het stelt:"Bij het bestuderen van deze en andere collageenziekten hebben veel onderzoekers, waaronder ikzelf, ... altijd een belangrijk deel van de kennis gemist. puzzel, en de mogelijkheid dat weefselfalen gedeeltelijk te wijten zou kunnen zijn aan de interactie tussen water en collageen, werd niet erg serieus genomen. We laten nu zien dat het verstoren van de waterlaag rond het eiwit, zelfs maar een heel klein beetje, dramatische gevolgen heeft voor de collageenassemblage."
Giubertoni wil onderzoekers in de collageenziektegemeenschap ervan bewust maken dat zeer subtiele veranderingen in de water-collageeninteractie kunnen bijdragen aan collageenziekten. Deze veranderingen kunnen mogelijk bijvoorbeeld voortkomen uit mutaties in het collageeneiwit die optreden bij genetische ziekten. De onderzoekers suggereren ook dat veranderde interacties tussen water en collageen een bijdragende factor zijn bij verschillende leeftijdsgebonden ziekten waarbij weefseldisfunctie betrokken is.
Het spul waar we van gemaakt zijn
Collageen is voor een groot deel 'het materiaal waar we van gemaakt zijn':ongeveer een derde van alle eiwitten in ons lichaam is collageen, dat de mechanische integriteit van al het menselijke bindweefsel waarborgt.
Onze huid en bloedvaten strekken zich bijvoorbeeld uit zonder te scheuren en onze botten kunnen hoge belastingen weerstaan zonder te breken. Collageen wordt door onze cellen geproduceerd als afzonderlijke eiwitten die samenkomen in grotere structuren die fibrillen worden genoemd. Deze fibrillen worden verder samengevoegd tot netwerken die de basis vormen voor onze weefsels.
Omdat collageen wordt gevormd in de waterige omgeving van menselijke cellen, speelt water een cruciale rol bij de assemblage ervan. De interactie van watermoleculen met eiwitten resulteert in collageen dat het meest geschikt is voor zijn functie. Maar wat zit er precies achter deze collageen-optimaliserende rol van water? Hoe doet water dat? En zal het begrijpen van dit mechanisme inzicht bieden in aandoeningen waarbij er iets mis is met collageen, zoals osteogenesis imperfecta? Dit waren de centrale vragen van het onderzoek gepubliceerd in PNAS .
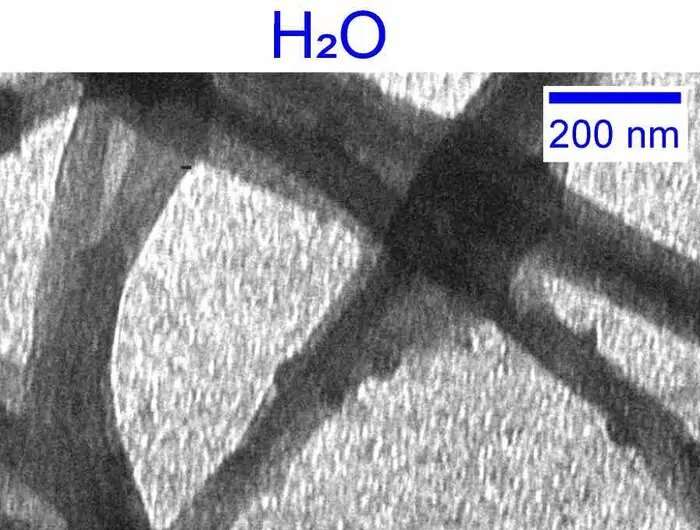
Introductie van zwaar water
Om de rol van water bij de vorming van collageen te onderzoeken, besloot Giubertoni – samen met haar UvA-collega prof. Sander Woutersen en hun medewerker prof. Gijsje Koenderink (Technische Universiteit Delft) – water te vervangen door het zwaardere 'tweelingmolecuul' D 2 O. Aanvankelijk ontdekt door Nobelprijswinnaar Harold Urey in 1931, in D2 O de waterstofatomen (H) van water worden vervangen door de isotoop deuterium (D) waaraan een toegevoegd neutron in de kern zit. D2 O of 'zwaar water' is dus de 'dichtstbijzijnde vervanging' van gewoon water in de natuur.
In interactie met eiwitten kan D2 O is minder krachtig dan H2 O. Dit komt door bindingen tussen D2 O-moleculen (zogenaamde waterstofbruggen) zijn sterker dan die tussen H2 O-moleculen. Dit beïnvloedt de interactie met eiwitten zoals collageen.
Giubertoni, Woutersen en Koenderink wilden graag onderzoeken welk effect dit zou hebben op de collageenaanmaak. Samen met een multidisciplinair onderzoeksnetwerk konden ze vaststellen dat het gebruik van zwaar water resulteert in een tien keer snellere collageenvorming en uiteindelijk in een minder homogeen, zachter en minder stabiel collageenvezelnetwerk.
Een zeer effectieve moderator
De verklaring is dat de verminderde interactie van het zware water met het collageeneiwit het voor het eiwit gemakkelijker maakt om de D2 af te schudden. O moleculen en reorganiseren zichzelf.
Dit bevordert de vorming van het collageennetwerk, maar resulteert ook in een slordiger, minder optimaal collageennetwerk. Water fungeert dus als bemiddelaar tussen collageenmoleculen en vertraagt de assemblage om de functionele eigenschappen van levende weefsels te garanderen.
Deze ontdekking biedt nieuwe perspectieven op de manier waarop water de eigenschappen van collageen beïnvloedt, waardoor nauwkeurige aanpassingen in de mechanische eigenschappen van levende weefsels mogelijk zijn. Het creëert ook nieuwe mogelijkheden voor het creëren van op collageen gebaseerde materialen waarbij macroscopische eigenschappen kunnen worden gecontroleerd en verfijnd door subtiele variaties in de samenstelling van het oplosmiddel, in plaats van significante veranderingen aan te brengen in de chemische structuur van de moleculaire bouwstenen.
Een soortgelijke "onderzoeks"-benadering zou in de toekomst ook kunnen worden gebruikt om de rol van water op te helderen bij het aansturen en begeleiden van de assemblage van andere eiwitten die in staat zijn om in grotere structuren te assembleren. Giubertoni gaat verder onderzoeken hoe defecten in collageen de interactie met water beïnvloeden, en welke rol dit speelt bij het falen van weefsel bij collageenziekten.
Meer informatie: Giulia Giubertoni et al, Opheldering van de rol van water bij de zelfassemblage van collageen door de isotopische hydratatie van collageen te moduleren, Proceedings of the National Academy of Sciences (2024). DOI:10.1073/pnas.2313162121
Journaalinformatie: Proceedings van de Nationale Academie van Wetenschappen
Aangeboden door Universiteit van Amsterdam
 Hoe mensen het klimaat op aarde in slechts 160 jaar hebben laten ontsporen
Hoe mensen het klimaat op aarde in slechts 160 jaar hebben laten ontsporen Schatting van de slijtage van ijs op fysieke structuren in de komende decennia of zelfs eeuwen
Schatting van de slijtage van ijs op fysieke structuren in de komende decennia of zelfs eeuwen Uit onderzoek blijkt dat de droogte in de Braziliaanse Cerrado de ergste is sinds zeven eeuwen
Uit onderzoek blijkt dat de droogte in de Braziliaanse Cerrado de ergste is sinds zeven eeuwen  Vulkaan Alaska barst opnieuw uit nog een aswolk opsturen (update)
Vulkaan Alaska barst opnieuw uit nog een aswolk opsturen (update) Overstromingen veroorzaakt door oude gegevens
Overstromingen veroorzaakt door oude gegevens
Hoofdlijnen
- Studie kan bijdragen aan toolbox voor resourcemanagers
- Vrouwelijke vissen houden van zingende mannetjes
- Hoe een mRNA-sequentie
- Antiverouderingsbehandelingen - The Science of Living Longer
- Zeldzame diepzee-inktvis gefilmd op diepte
- Structuur van het cardiovasculaire systeem
- Spin eet spin:wetenschappers ontdekken 18 nieuwe op spinnen jagende pelikaanspinnen in Madagaskar
- Fossiele apentanden openen een nieuw venster in oude seizoensklimaten
- Hoge prijzen van dierlijke producten onderdeel van een vicieuze cirkel naar uitsterven
- filmpje:natto, de stinkende, slijmerige sojabonensnack

- Computerprogramma kan een 2D-tekening in vrije vorm vertalen naar een DNA-structuur
- Waarom zijn planten groen? Model van onderzoeksteams reproduceert fotosynthese

- Zink reguleert de opslag en afgifte van neurotransmitters

- Waarom worden sommige legeringen sterker bij kamertemperatuur?

 findNano-app zet nanotech in je zak
findNano-app zet nanotech in je zak Gecombineerde voedingsstoffen en opwarming verhogen de methaanemissies van meren enorm
Gecombineerde voedingsstoffen en opwarming verhogen de methaanemissies van meren enorm Wat doet acetonalcohol met een gramkleuring?
Wat doet acetonalcohol met een gramkleuring?  Facebook onthult nieuwe cryptocurrency
Facebook onthult nieuwe cryptocurrency Twijfel je over het klimaat? Misschien ervaar je eco-angst
Twijfel je over het klimaat? Misschien ervaar je eco-angst  7,5 miljard en nog meer:hoeveel mensen kan de aarde ondersteunen?
7,5 miljard en nog meer:hoeveel mensen kan de aarde ondersteunen? Justitie niet blind voor gendervooroordelen
Justitie niet blind voor gendervooroordelen Vervagende lichten:uitgebreid onderzoek onthult meerdere bedreigingen voor de vuurvliegpopulaties in Noord-Amerika
Vervagende lichten:uitgebreid onderzoek onthult meerdere bedreigingen voor de vuurvliegpopulaties in Noord-Amerika
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

