
Wetenschap
Sterker dan de natuur:geoptimaliseerde radicalen als potentiële nieuwe katalysatoren
De natuur gebruikt enzymen voor verschillende stofwisselingsprocessen. Deze biologische katalysatoren zijn uiterst efficiënt. Biomimetische katalysatoren op basis van goedkope uitgangsmaterialen uit het laboratorium die de efficiëntie van de natuurlijke enzymen kunnen reproduceren en kunnen functioneren onder omgevingsomstandigheden zijn daarom van groot belang voor onderzoek en industrie.
In een project onder leiding van het Instituut voor Chemie van de Humboldt-Universität zu Berlin (HU) hebben onderzoekers een speciale groep biologische katalysatoren onderzocht die bekend staan als oxidasen. Deze enzymen katalyseren verschillende oxidatiereacties, waarbij elektronen vrijkomen uit de ene stof en worden geabsorbeerd door een andere. Kleine, zeer reactieve deeltjes, zogenaamde radicalen, spelen vaak een belangrijke rol in deze processen.
Oxiderende capaciteit verbeterd door binding aan ijzer
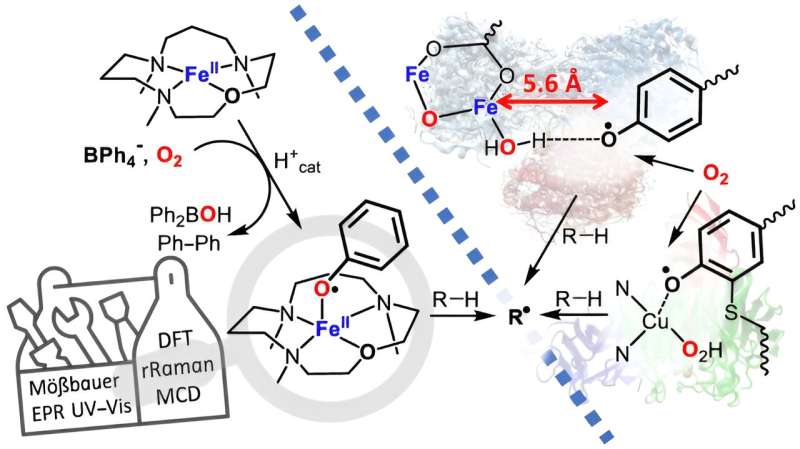
Het enzym dat momenteel van belang is, is galactose-oxidase dat in veel soorten schimmels wordt aangetroffen, waarbij een fenoxylradicaal als oxidatiemiddel wordt gebruikt. Het team onder leiding van HU-onderzoeker Kallol Ray heeft nu een manier gevonden om de fenoxylradicaal in het laboratorium zo te benutten dat de oxidatiecapaciteit aanzienlijk vergroot kan worden.
In het natuurlijk voorkomende enzym wordt het fenoxylradicaal gestabiliseerd door een zwavelatoom, wat de oxidatiecapaciteit ervan beperkt. De onderzoekers hebben nu het oxidatievermogen verbeterd door een ongemodificeerde fenoxylradicaal aan ijzer te hechten en hebben dit ijzer-fenoxylradicaal voor het eerst chemisch gekarakteriseerd. Ray's team werkte aan dit project samen met collega's van de Technische Universiteit van Berlijn en de Universiteit van Michigan, VS.
Het werk is gepubliceerd in het tijdschrift Nature Chemistry .
Eerste beschrijving van het ijzerfenoxylradicaal – belangrijk voor onderzoek en industrie
"We verwachten dat ons werk het startpunt zal zijn voor meer gerichte inspanningen om de ijzer-fenoxylradicaalinteractie te gebruiken voor verschillende biochemische reacties", zegt Ray. "Dit kan de ontwikkeling ondersteunen van nieuwe katalysatoren die nodig zijn voor alternatieve energietechnologieën en andere biotechnologische toepassingen."
De onderzoeksresultaten van Ray en zijn team zijn van groot belang voor zowel onderzoek als toepassing, aangezien de reactie gekatalyseerd door galactose-oxidase (oxidatie van een primaire alcohol tot het overeenkomstige aldehyde) een van de belangrijkste en meest gebruikte chemische reacties is in organische processen. synthese.
De bevindingen zouden ook in de industrie kunnen worden gebruikt om het klimaatschadelijke gas methaan om te zetten in vloeibare methanol. In tegenstelling tot methaan, een vluchtig gas en daardoor moeilijk te hanteren, is methanol gemakkelijk te transporteren en als synthetische brandstof te gebruiken. Momenteel is er veel energie nodig om methaan om te zetten in methanol. De chemische reactie vindt alleen plaats bij hoge temperaturen (> 500 graden Celsius) en onder hoge druk. Biomimetische katalysatoren zouden deze energie-input aanzienlijk kunnen verminderen.
"In dit project was het spannend om de onverwachte structurele en functionele gelijkenis van ons synthetische systeem met natuurlijke enzymen te zien", zegt Dustin Kass, een Ph.D. student in de onderzoeksgroep van Kallol Ray en de hoofdauteur van deze studie.