
Wetenschap
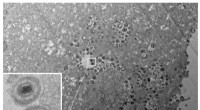
Deling en groei van synthetische blaasjes
Krediet:Wiley
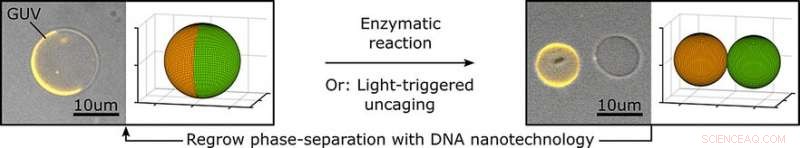
Een grote uitdaging voor de productie van synthetische cellen is dat ze zich moeten kunnen delen om nakomelingen te krijgen. In het journaal Angewandte Chemie , een team uit Heidelberg heeft nu een reproduceerbaar delingsmechanisme voor synthetische blaasjes geïntroduceerd. Het is gebaseerd op osmose en kan worden gecontroleerd door een enzymatische reactie of licht.
Organismen kunnen niet eenvoudigweg voortkomen uit levenloos materiaal ("abiogenese"), cellen komen altijd uit reeds bestaande cellen. Het vooruitzicht van synthetische cellen die van de grond af worden gebouwd, verschuift dit paradigma. Echter, een obstakel op dit pad is de kwestie van gecontroleerde verdeling - een vereiste om 'nakomelingen' te hebben.
Een team van het Max Planck Instituut voor Medisch Onderzoek in Heidelberg, Universiteit van Heidelberg, de Max Planck-school is belangrijk voor het leven, en Exzellenzcluster 3D-materie op bestelling gemaakt, onder leiding van Kerstin Göpfrich, heeft nu een mijlpaal bereikt door volledige controle te krijgen over de verdeling van blaasjes. Om dit te behalen, ze produceerden "gigantische unilamellaire blaasjes, " Dit zijn bellen van micrometerformaat met een omhulsel gemaakt van een lipidedubbellaag die lijkt op een natuurlijk membraan. Een verscheidenheid aan lipiden werd gecombineerd om fasegescheiden blaasjes te produceren - blaasjes met membraanhelften die verschillende samenstellingen hebben. Wanneer de concentratie van opgeloste stoffen in de omringende oplossing wordt vergroot, osmose zorgt ervoor dat water het blaasje door het membraan verlaat. Dit krimpt het volume van het blaasje terwijl het membraanoppervlak gelijk blijft. De resulterende spanning op het fase-interface vervormt de blaasjes. Ze vernauwen zichzelf langs hun "evenaar" - toenemend met toenemende osmotische druk - totdat de twee helften volledig scheiden om twee (nu eenfasige) "dochtercellen" met verschillende membraansamenstellingen te vormen. Wanneer de scheiding die optreedt alleen afhangt van de concentratieverhouding van osmotisch actieve deeltjes (osmolariteit) en onafhankelijk is van de grootte van het blaasje.
De methode waarmee de osmolariteit wordt verhoogd, speelt ook geen rol. De methoden die door het team werden gebruikt, omvatten het gebruik van een sucrose-oplossing en het toevoegen van een enzym dat glucose en fructose splitst om de concentratie langzaam te verhogen. Door licht te gebruiken om de splitsing van moleculen in de oplossing te starten, kregen de onderzoekers volledige ruimtelijke en temporele controle over de scheiding. Met behulp van strak gecontroleerde, door lokale bestraling kon de concentratie selectief worden verhoogd rond een enkel blaasje, het triggeren om selectief te delen.
Het team is ook in staat om de enkelfasige cellen terug te laten groeien tot in fase gescheiden blaasjes door ze te fuseren met kleine blaasjes die het andere type membraan hebben. Dit werd mogelijk gemaakt door enkele strengen DNA aan beide verschillende soorten membraan te bevestigen. Deze binden aan elkaar en brengen de membranen van de dochtercel en het miniblaasje in zeer nauw contact zodat ze kunnen samensmelten. De resulterende gigantische blaasjes kunnen vervolgens verdere delingscycli ondergaan.
"Hoewel deze synthetische delingsmechanismen aanzienlijk verschillen van die van levende cellen, " zegt Göpfrich, "de vraag rijst of soortgelijke mechanismen een rol hebben gespeeld bij het begin van het leven op aarde of betrokken zijn bij de vorming van intracellulaire blaasjes."
 Het sonderen van wateren huid
Het sonderen van wateren huid Een keramische resurfacing prothese voor heupgewrichten
Een keramische resurfacing prothese voor heupgewrichten Biobased chemicaliën staan centraal
Biobased chemicaliën staan centraal Wetenschappers identificeren bioactieve stoffen in cacaobonen om medicijnen te ontwikkelen om skeletaandoeningen te bestrijden
Wetenschappers identificeren bioactieve stoffen in cacaobonen om medicijnen te ontwikkelen om skeletaandoeningen te bestrijden Hoe Net Ionic vergelijkingen in de chemie te doen
Hoe Net Ionic vergelijkingen in de chemie te doen
 Een stemmingslift nodig? We hebben 4 manieren gevolgd waarop de Australische omgeving zichzelf heeft hersteld in 2020
Een stemmingslift nodig? We hebben 4 manieren gevolgd waarop de Australische omgeving zichzelf heeft hersteld in 2020 Wat zijn de oorzaken van overmatig vissen?
Wat zijn de oorzaken van overmatig vissen?  Hoe werkt wind?
Hoe werkt wind?  Scheidingstechnieken om waterzuiveringsinstallaties te behandelen
Scheidingstechnieken om waterzuiveringsinstallaties te behandelen Er vindt een regimewisseling plaats in de Noordelijke IJszee, wetenschappers zeggen:
Er vindt een regimewisseling plaats in de Noordelijke IJszee, wetenschappers zeggen:
Hoofdlijnen
- Is hangry een echte emotie?
- Het belang van het bestuderen van de DNA-genetica van het menselijk geslacht
- Designer-molecuul wijst op behandeling voor ziekten veroorzaakt door DNA-herhalingen
- Technologie verhoogt melkgift met 9 procent
- Mannelijke dolfijnen bieden geschenken aan om vrouwtjes aan te trekken
- Gemuteerd kikkergen stoot roofdieren af
- Wat is de structuur van stamcellen?
- Met extra suiker, bladeren worden ook dik
- Wat is de functie van de pellet?
- Screening op macrocyclische peptiden
- Machine learning biedt een nieuwe manier om chirale kristallen te ontwerpen

- Sulphur biedt veelbelovend batterij-alternatief van de volgende generatie
- Kleurveranderende coatings geactiveerd door temperatuurveranderingen
- Extreme kou kan de dynamiek van herpesvirusinfecties onthullen
 Gamers kennen de kracht van flow:wat als leerlingen het ook zouden kunnen benutten?
Gamers kennen de kracht van flow:wat als leerlingen het ook zouden kunnen benutten? Hoeveel uren van het daglicht in de zomer?
Hoeveel uren van het daglicht in de zomer?  Native Plants of the Texas Coastal Plains
Native Plants of the Texas Coastal Plains  Hoe het volume van een container te berekenen
Hoe het volume van een container te berekenen Onderzoekers creëren een prachtig huwelijk van kwantumvijanden
Onderzoekers creëren een prachtig huwelijk van kwantumvijanden Een van de redenen waarom COVID-19 erger is voor zwarte gemeenschappen:politiegeweld
Een van de redenen waarom COVID-19 erger is voor zwarte gemeenschappen:politiegeweld Een model maken van een maansverduistering en een zonsverduistering
Een model maken van een maansverduistering en een zonsverduistering Afbeelding:Frosty krater op Mars
Afbeelding:Frosty krater op Mars
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Portuguese | German | Dutch | Danish | Norway | Spanish | Swedish |

-
Wetenschap © https://nl.scienceaq.com

