
Wetenschap
De opwarming van de aarde aanpakken met nieuwe nanodeeltjes en zonneschijn
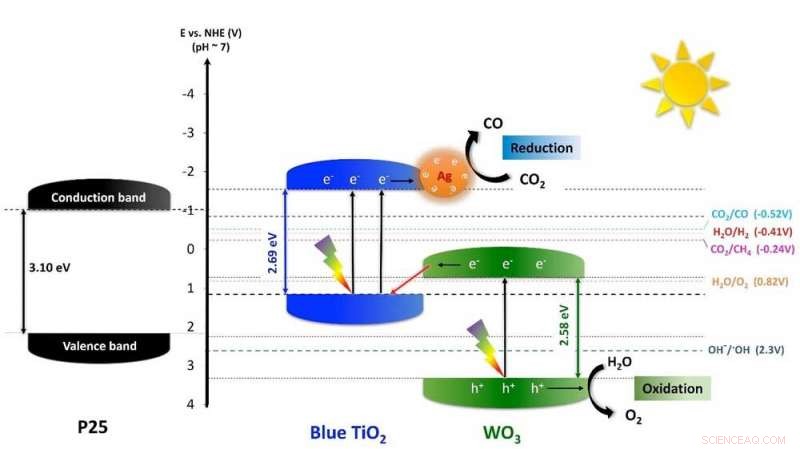
Figuur 1. Voorgesteld energiediagram dat het elektronenoverdrachtmechanisme in TiO . weergeeft 2 /WO 3 -Ag hybride nanodeeltjes. Dit zogenaamde Z-schema toont de stroom van geladen deeltjes (elektronen, e- en gaten, , h+) door de verschillende componenten van de nanodeeltjes. Blauwe TiO 2 en WO 3 's e- kan lager innemen (valentieband, VB) en hoger (geleidende band, CB) energieniveaus. Fotonen uit zonlicht (donder) leveren de energie voor de e- om omhoog te springen van de VB naar de CB (zwarte pijlen wijzen naar boven), h+ achterlatend. TiO 2 's onderste band is dichtbij, net iets lager dan het hogere bandniveau van WO3, dus e- van de hoge band van WO3 kan migreren naar de VB van blauwe TiO 2 zijn gaten te vangen. Na scheiding, de opgewonden e-sprong van de CB van TiO 2 op zilveren nanodeeltjes waardoor de omzetting van CO 2 in CO, terwijl de fotogegenereerde h+ in de WO 3 plaats oxideren water (H 2 O) om zuurstof te vormen (O 2 ). Krediet:Instituut voor Basiswetenschappen
zonlicht oogsten, onderzoekers van het Centre for Integrated Nanostructure Physics, binnen het Instituut voor Basiswetenschappen (IBS, Zuid-Korea) gepubliceerd in Materialen vandaag ("Fase-selectieve zeer efficiënte nanogestructureerde, met metaal versierde hybride halfgeleiders voor zonneconversie van CO 2 to Absolute CO Selectivity") een nieuwe strategie om koolstofdioxide (CO 2 ) in zuurstof (O 2 ) en zuiver koolmonoxide (CO) zonder bijproducten in water. Deze kunstmatige fotosynthesemethode zou nieuwe oplossingen kunnen bieden voor milieuvervuiling en het broeikaseffect.
Terwijl, bij groene planten, fotosynthese lost CO . op 2 in suikers, de kunstmatige fotosynthese die in dit onderzoek wordt gerapporteerd, kan CO . omzetten 2 in zuurstof en zuivere CO als output. Dit laatste kan vervolgens worden ingezet voor een breed scala aan toepassingen in de elektronica, halfgeleider, farmaceutisch, en chemische industrieën.
De sleutel is om de juiste krachtige fotokatalysator te vinden om de fotosynthese te laten plaatsvinden door licht te absorberen, converteren CO 2 , en zorgen voor een efficiënte stroom van elektronen, wat essentieel is voor het hele systeem.
Titaanoxide (TiO 2 ) is een bekende fotokatalysator. Het heeft al veel aandacht getrokken op het gebied van zonne-energieconversie en milieubescherming vanwege zijn hoge reactiviteit, lage toxiciteit, chemische stabiliteit, en lage kosten.
Terwijl conventionele TiO 2 kan alleen UV-licht absorberen, het IBS-onderzoeksteam rapporteerde eerder twee verschillende soorten blauwgekleurde TiO 2 (of "blauwe titania") nanodeeltjes die zichtbaar licht kunnen absorberen dankzij een verminderde bandgap van ongeveer 2,7 eV.
Ze waren gemaakt van geordende anatase/wanorde rutiel (Ao/Rd) TiO 2 (genaamd, HYL's blauwe TiO 2 -I) ("Een orde/stoornis/waterverbindingssysteem voor zeer efficiënte co-katalysatorvrije fotokatalytische waterstofgeneratie"), en ongeordende anatase/geordende rutiel (Ao/Rd) TiO 2 (genaamd, HYL's blauwe TiO 2 -II) ("Zichtbaar-licht-gedreven, Metaalvrije CO 2 Vermindering"), waarbij anatase en rutiel verwijzen naar twee kristallijne vormen van TiO 2 en de introductie van onregelmatigheden (wanorde) in het kristal verbetert de absorptie van zichtbaar en infrarood licht.
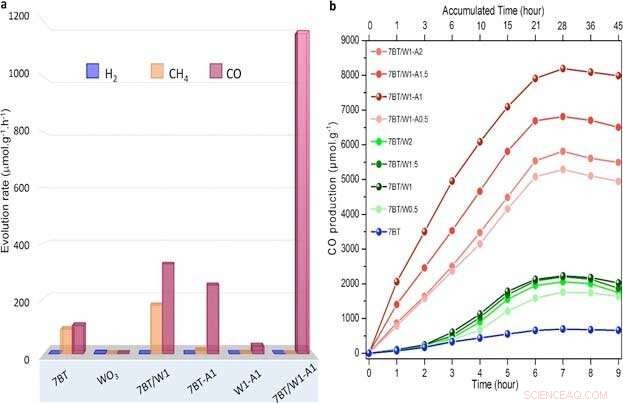
Figuur 2. Efficiënte en selectieve productie van CO met verschillende nanodeeltjes. (a) De grafiek laat zien dat hybride TiO 2 /WO 3 -Ag (7BT/W1-A1) nanodeeltjes zijn het beste in het selectief produceren van pure CO, zonder H 2 en CH 4 bijproducten binnen een tijdsbestek van zeven uur. Deze zijn te vergelijken met nanodeeltjes van blauw TiO 2 , WO 3 , hybride TiO 2 /WO 3 (7BT/W1) en hybride TiO 2 /Ag (W1-A1). (b) CO-productie met behulp van verschillende hybride nanodeeltjes gemaakt van TiO2 / WO3-Ag (rode lijnen), TiO 2 /WO 3 (groene lijnen) en TiO 2 -alleen nanodeeltjes (blauwe lijnen) binnen negen uur. 7BT/W1-A1 met een concentratie van 1 procent zilver heeft de beste prestaties. Krediet:Instituut voor Basiswetenschappen
Voor de efficiënte kunstmatige fotosynthese voor de omzetting van CO 2 in zuurstof en zuivere CO, IBS-onderzoekers wilden de prestaties van deze nanodeeltjes verbeteren door blauwe (Ao/Rd) TiO . te combineren 2 met andere halfgeleiders en metalen die de oxidatie van water tot zuurstof kunnen verbeteren, parallel aan CO 2 reductie tot alleen CO.
Het onderzoeksteam behaalde de beste resultaten met hybride nanodeeltjes gemaakt van blauw titania, wolfraamtrioxide (WO 3 ), en 1 procent zilver (TiO 2 /WO 3 –Ag).
WO 3 werd gekozen vanwege de lage valentiebandpositie met zijn smalle bandgap van 2,6 eV, hoge stabiliteit, en lage kosten. Zilver werd toegevoegd omdat het de absorptie van zichtbaar licht verbetert, door een collectieve oscillatie te creëren van vrije elektronen die worden opgewekt door licht, en geeft ook een hoge CO-selectiviteit.
De hybride nanodeeltjes vertoonden ongeveer 200 keer betere prestaties dan nanodeeltjes gemaakt van TiO 2 alleen en TiO 2 /WO 3 zonder zilver.
Uitgaande van water en CO 2 , deze nieuwe hybride katalysator produceerde O2 en zuivere CO, zonder enige bijproducten, zoals waterstofgas (H2) en methaan (CH4). De schijnbare kwantumopbrengst dat de verhouding is van verschillende gereageerde elektronen tot het aantal invallende fotonen was 34,8 procent, en de snelheid van gereageerde elektronen 2333,44 µmol g-1h-1. Dezelfde meting was lager voor nanodeeltjes zonder zilver (2053,2 µmol g-1h-1), en voor nanodeeltjes met alleen blauwe TiO 2 (912,4 µmol g-lh-1).
 Kooldioxide transformeren - onderzoekers ontwikkelen nieuwe tweestaps CO2-conversietechnologie
Kooldioxide transformeren - onderzoekers ontwikkelen nieuwe tweestaps CO2-conversietechnologie Veiliger maandverband gemaakt van palmzetmeel
Veiliger maandverband gemaakt van palmzetmeel Zullen de futures-superbatterijen van zeewater worden gemaakt?
Zullen de futures-superbatterijen van zeewater worden gemaakt? Wetenschappers hebben een manier voorgesteld om in water oplosbare fullereenverbindingen voor medicijnen te produceren
Wetenschappers hebben een manier voorgesteld om in water oplosbare fullereenverbindingen voor medicijnen te produceren Vers houden:nieuwe op AI gebaseerde strategie kan de versheid van rundvleesmonsters beoordelen
Vers houden:nieuwe op AI gebaseerde strategie kan de versheid van rundvleesmonsters beoordelen
Hoofdlijnen
- Vroege mensen gepaard met ingeteelde neanderthalers - tegen een prijs
- Schapen kunnen menselijke gezichten van foto's herkennen
- Studie:Grote witte haaien zwemmen steeds dieper
- 5 manieren om optimistisch te blijven in een neergaande economie
- Genotype & Phenotype Definitie
- Kunnen darmbacteriën de volgende sportdrank worden?
- Hoe kan een puntmutatie de eiwitsynthese doen stoppen?
- 6 veelvoorkomende hallucinaties en wat ze ons vertellen
- Biomedical Engineering Project Onderwerpen voor High School
- Het spliceosoom - nu beschikbaar in hoge definitie
- Nieuwe tool analyseert ziekte- en medicijneffecten met ongekende nauwkeurigheid en consistentie

- Zoals de hond van Pavlov, deze thermoplast leert een nieuwe truc:lopen

- Hoe plankton en bacteriën oceaanspray vormen

- Uit een spaghetti-achtige wirwar van microvezels en water komt een veelbelovend nieuw materiaal

 Boren stopt op controversiële oliebron 240 mijl van Zuid-Florida nadat bedrijf de put te droog vindt
Boren stopt op controversiële oliebron 240 mijl van Zuid-Florida nadat bedrijf de put te droog vindt Quantum computing met enkele fotonen komt dichter bij de realiteit
Quantum computing met enkele fotonen komt dichter bij de realiteit Chemische ingenieurs publiceren paper waarin theorieën over glasovergang worden uitgedaagd
Chemische ingenieurs publiceren paper waarin theorieën over glasovergang worden uitgedaagd Afzonderlijke moleculen wegen met licht
Afzonderlijke moleculen wegen met licht Wat zijn de vijf hoofdlijnen van breedte?
Wat zijn de vijf hoofdlijnen van breedte?  De laatste bevindingen over de MOSAiC ijsschots
De laatste bevindingen over de MOSAiC ijsschots Nieuwe superzware elementen synthetiseren om de achtste periode van het periodiek systeem te openen
Nieuwe superzware elementen synthetiseren om de achtste periode van het periodiek systeem te openen Prototype vliegende auto Boeing voltooit eerste testvlucht
Prototype vliegende auto Boeing voltooit eerste testvlucht
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

