
Wetenschap
De oorzaak van capaciteitsverlies vinden in een metaaloxide batterijmateriaal

Sooyeon Hwang (zittend), Dong Su (links, staan, en Shuang Li in het Brookhaven Lab's Centre for Functional Nanomaterials, waar ze elektronenmicroscopen gebruikten om te zien hoe de kristalstructuur en chemische aard van een batterij-elektrode gemaakt van een ijzeroxide materiaal genaamd magnetiet evolueerde toen lithium werd ingebracht en geëxtraheerd gedurende 100 laad- en ontlaadcycli. Krediet:Brookhaven National Laboratory
Vanwege hun hoge energieopslagdichtheid, materialen zoals metaaloxiden, sulfiden, en fluoriden zijn veelbelovende elektrodematerialen voor lithium-ionbatterijen in elektrische voertuigen en andere technologieën. Echter, hun capaciteit vervaagt zeer snel. Nutsvoorzieningen, wetenschappers die een elektrode bestuderen die is gemaakt van een goedkoop en niet-toxisch ijzeroxidemateriaal, magnetiet genaamd, hebben een scenario voorgesteld - beschreven in het online nummer van 20 mei van Natuurcommunicatie - dat verklaart waarom.
"Magnetiet, onder andere elektrodematerialen van het conversietype (d.w.z. materialen die worden omgezet in geheel nieuwe producten wanneer ze reageren met lithium), kunnen meer energie opslaan dan de huidige elektrodematerialen omdat ze meer lithiumionen kunnen bevatten, " zei studieleider Dong Su, leider van de Electron Microscopy Group bij het Center for Functional Nanomaterials (CFN) - een Office of Science User Facility van het Amerikaanse Department of Energy (DOE) in het Brookhaven National Laboratory. "Echter, de capaciteit van deze materialen neemt zeer snel af en is afhankelijk van de stroomdichtheid. Bijvoorbeeld, onze elektrochemische testen van magnetiet hebben aangetoond dat de capaciteit ervan zeer snel daalt binnen de eerste 10 oplaad- en ontlaadcycli met hoge snelheid."
Om erachter te komen wat er achter deze slechte fietsstabiliteit zit, de wetenschappers karakteriseerden hoe de kristalstructuur en de chemische aard van magnetiet evolueerden toen de batterij 100 cycli voltooide. Voor deze karakteriseringsstudies ze combineerden transmissie-elektronenmicroscopie (TEM) bij de CFN en synchrotron-röntgenabsorptiespectroscopie (XAS) bij de Advanced Photon Source (APS) - een DOE Office of Science User Facility in het Argonne National Lab. in TEM, een elektronenstraal wordt door een monster doorgelaten om een beeld of een diffractiepatroon te produceren dat karakteristiek is voor de structuur van het materiaal; XAS gebruikt in plaats daarvan een röntgenstraal om de chemie van het materiaal te onderzoeken.
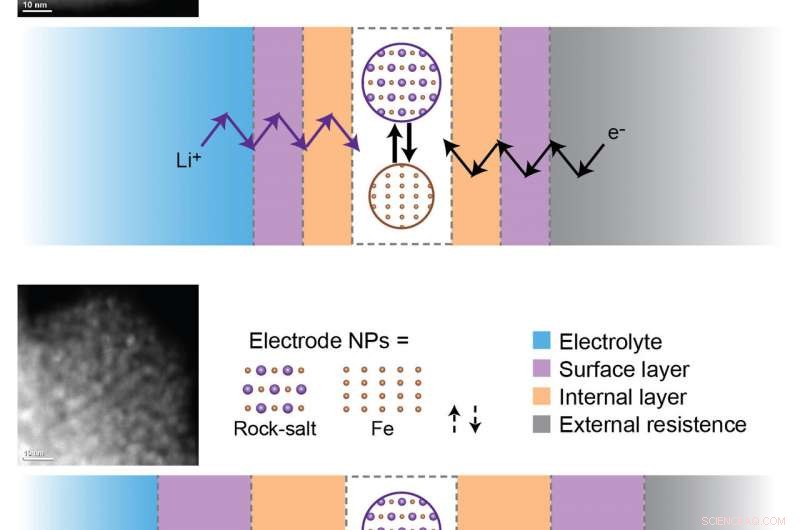
De afname van de batterijcapaciteit is te wijten aan de vorming en verdikking van interne en oppervlaktepassiveringslagen tijdens laad- en ontlaadcycli. Om de elektrochemische reacties te laten plaatsvinden, lithiumionen (Li+) en elektronen (e-) moeten door al deze lagen reizen om actieve nanodeeltjes (NP's) bij de elektrode te bereiken. Boven:Fe3O4 (ijzeroxide) monster na drie cycli. Bodem:Fe3O4-monster na 100 cycli. De ontwikkeling van kinetische barrières tijdens langdurige cycli beperkt elektrochemische reacties in die mate dat er na 100 cycli geen reductie-oxidatiereacties optreden bij de elektrodematerialen. Krediet:Brookhaven National Laboratory
Met behulp van deze technieken, de wetenschappers ontdekten dat magnetiet tijdens de eerste ontlading volledig uiteenvalt in metallische ijzernanodeeltjes en lithiumoxide. In de volgende aanklacht, deze omzettingsreactie is niet volledig omkeerbaar - resten van metallisch ijzer en lithiumoxide blijven. Bovendien, de oorspronkelijke "spinel" -structuur van magnetiet evolueert in een "steenzout" -structuur (de locatie van ijzeratomen is niet geheel identiek in de twee structuren) in de geladen toestand. Met daaropvolgende laad- en ontlaadcycli, steenzoutijzeroxide interageert met lithium om een composiet te vormen van lithiumoxide en metallische ijzernanodeeltjes. Omdat de omzettingsreactie niet volledig omkeerbaar is, deze restproducten stapelen zich op. De wetenschappers ontdekten ook dat de elektrolyt (het chemische medium dat ervoor zorgt dat lithiumionen tussen de twee elektroden kunnen stromen) in latere cycli uiteenvalt.
"Onze realtime TEM-onderzoeken in ultrahoog vacuüm hebben ons in staat gesteld te zien hoe de structuur van steenzoutijzeroxide verandert wanneer lithium wordt geïntroduceerd na de eerste cycli, " zei Su. "Deze studie vertegenwoordigt op unieke wijze de in situ lithiëring van een precycled monster. Bij eerdere in-situ-onderzoeken werd alleen gekeken naar de initiële laad- en ontlaadcycli. Echter, we moeten weten wat er gedurende vele cycli gebeurt om batterijen met een langere levensduur te ontwerpen, omdat de structuur bij de geladen elektrode anders is dan die van de oorspronkelijke staat."
Op basis van hun resultaten, de wetenschappers stelden een verklaring voor de capaciteitsvervaging voor.
"Omdat lithiumoxide een lage elektronische geleidbaarheid heeft, de accumulatie creëert een barrière voor de elektronen die heen en weer pendelen tussen de positieve en negatieve elektrode van de batterij, " verklaarde mede-hoofdauteur Sooyeon Hwang, een stafwetenschapper in de CFN Electron Microscopy Group. "We noemen deze barrière een interne passiveringslaag. Op dezelfde manier elektrolytische ontleding belemmert de ionengeleiding door een oppervlaktepassiveringslaag te vormen. Deze opeenhoping van obstakels blokkeert elektronen en lithiumionen om actieve elektrodematerialen te bereiken, waar de elektrochemische reacties plaatsvinden."
De wetenschappers merkten op dat het gebruik van de batterij bij een lage stroomsterkte een deel van deze capaciteit kan herstellen door de laadsnelheid te vertragen om voldoende tijd te geven voor elektronentransport; echter, er zijn andere oplossingen nodig om het probleem uiteindelijk op te lossen. Ze zijn van mening dat het toevoegen van andere elementen aan het elektrodemateriaal en het veranderen van de elektrolyt de capaciteitsvervaging zou kunnen verbeteren.
"De kennis die we hebben opgedaan, kan over het algemeen worden toegepast op andere conversieverbindingen, die ook met hetzelfde probleem worden geconfronteerd met interne en externe passiveringslagen, " zei co-corresponderende auteur Zhongwei Chen, een professor aan de Universiteit van Waterloo, Canada. "We hopen dat deze studie kan helpen bij toekomstig fundamenteel onderzoek naar deze veelbelovende elektrodematerialen van het conversietype."
 Zeer selectief adsorberend materiaal trekt ongewenste stoffen aan om bioproductie ten goede te komen
Zeer selectief adsorberend materiaal trekt ongewenste stoffen aan om bioproductie ten goede te komen Hoe een vaste concentratie te berekenen
Hoe een vaste concentratie te berekenen  Wetenschappers stellen voor om machine learning te gebruiken om materiaaleigenschappen te voorspellen
Wetenschappers stellen voor om machine learning te gebruiken om materiaaleigenschappen te voorspellen Het effect van oplossingsconcentratie op geleidbaarheid
Het effect van oplossingsconcentratie op geleidbaarheid  Sensoren voor de versheid van voedsel kunnen de houdbaarheidsdatum vervangen om voedselverspilling tegen te gaan
Sensoren voor de versheid van voedsel kunnen de houdbaarheidsdatum vervangen om voedselverspilling tegen te gaan
 Zeespiegel blijft stijgen nadat emissietoezeggingen van Parijs in 2030 aflopen
Zeespiegel blijft stijgen nadat emissietoezeggingen van Parijs in 2030 aflopen De sterkte van tektonische platen kan de vorm van het Tibetaanse plateau verklaren, studie vondsten
De sterkte van tektonische platen kan de vorm van het Tibetaanse plateau verklaren, studie vondsten NASA meet potentiële tropische cycloon 10s temperatuur
NASA meet potentiële tropische cycloon 10s temperatuur Welke dieren in het regenwoud zijn scavengers?
Welke dieren in het regenwoud zijn scavengers?  Diesellekkage uit getroffen olietanker bij Sri Lanka
Diesellekkage uit getroffen olietanker bij Sri Lanka
Hoofdlijnen
- Wanneer vissen:Timing is belangrijk voor vissen die migreren om zich voort te planten
- Biologen kijken naar het verleden voor vroege genetische ontwikkeling van kleine spinnen- en insectenogen
- Nieuw onderzoek lost een van de meest verhitte geschillen over evolutionaire biologie op robuuste wijze op
- Zes belangrijkste celfuncties
- Fase waarin de Nucleus & Nucleolus zijn hervormd
- Competitie (biologie): definitie, types en voorbeelden
- Een biobank van omkeerbare mutante embryonale stamcellen
- Wat zijn de vier macromoleculen van het leven?
- RIP Jeremy de lefty tuinslak
- Mariene vervuiling:hoe verdunnen plastic additieven in water en hoe riskant zijn ze?

- Potentieel alternatief voor petroleumpolycarbonaat dat bronnen van omgevingshormonen bevat

- Structuur van de belangrijkste hersenreceptor die het behandeldoel is voor epilepsie, angst opgelost
- Isotopen zoeken

- Hoe isotoniciteit te berekenen

 Hoe windsnelheid schatten met een Flag
Hoe windsnelheid schatten met een Flag Red onze oceanen om onze gezondheid te beschermen - wetenschappers vragen om een wereldwijd actieplan
Red onze oceanen om onze gezondheid te beschermen - wetenschappers vragen om een wereldwijd actieplan Donkere materie sleept de meest massieve spiraalstelsels naar halsbrekende snelheden
Donkere materie sleept de meest massieve spiraalstelsels naar halsbrekende snelheden Elektronen in kwantumvloeistof halen energie uit laserpulsen
Elektronen in kwantumvloeistof halen energie uit laserpulsen Vingertopaanraking aanwijzing voor menselijke voorouders die boomtopomgevingen exploiteren
Vingertopaanraking aanwijzing voor menselijke voorouders die boomtopomgevingen exploiteren Dwerggenoot van EPIC 206011496 gedetecteerd door astronomen
Dwerggenoot van EPIC 206011496 gedetecteerd door astronomen Zwaardere regen en mest betekenen meer algenbloei
Zwaardere regen en mest betekenen meer algenbloei De meeste EU-landen missen luchtkwaliteitsdoelen:rapport
De meeste EU-landen missen luchtkwaliteitsdoelen:rapport
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

