
Wetenschap
Betere RNA-interferentie, geïnspireerd door de natuur:nieuwe nanodeeltjes bieden de beste genuitschakeling ooit
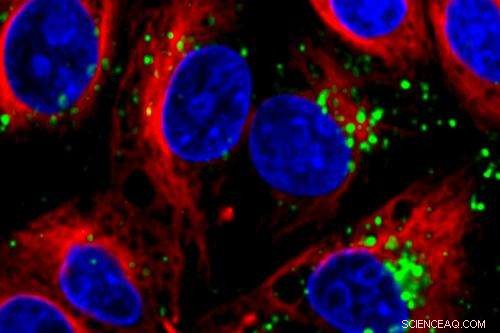
MIT-ingenieurs hebben nanodeeltjes ontworpen die korte strengen RNA (groen) in cellen kunnen afleveren (kernen zijn blauw gekleurd). Krediet:Gaurav Sahay, Yizhou Dong, Omid Veiseh
Geïnspireerd door kleine deeltjes die cholesterol door het lichaam vervoeren, Chemische ingenieurs van het MIT hebben nanodeeltjes ontworpen die fragmenten van genetisch materiaal kunnen leveren die ziekteverwekkende genen uitschakelen.
Deze aanpak, bekend als RNA-interferentie (RNAi), belooft veel voor de behandeling van kanker en andere ziekten. Echter, het leveren van voldoende RNA om het zieke weefsel te behandelen, terwijl bijwerkingen in de rest van het lichaam worden vermeden, moeilijk is gebleken.
De nieuwe MIT-deeltjes, die korte strengen RNA omsluiten in een bol van vetmoleculen en eiwitten, doelgenen in de lever efficiënter tot zwijgen brengen dan enig eerder toedieningssysteem, vonden de onderzoekers in een studie met muizen.
"Waar we enthousiast over zijn, is dat er maar een heel kleine hoeveelheid RNA nodig is om gen-knockdown in de hele lever te veroorzaken. Het effect is specifiek voor de lever - we krijgen geen effect in andere weefsels waar je het niet wilt, " zegt Daniël Anderson, de Samuel A. Goldblith Associate Professor of Chemical Engineering en een lid van MIT's Koch Institute for Integrative Cancer Research.
Anderson is senior auteur van een paper waarin de deeltjes in de Proceedings van de National Academy of Sciences de week van 10 februari. Robert Langer, de David H. Koch Institute Professor aan het MIT, is ook een auteur.
Het onderzoeksteam, waaronder wetenschappers van Alnylam Pharmaceuticals, ontdekte ook dat de nanodeeltjes genen in niet-menselijke primaten krachtig tot zwijgen kunnen brengen. De technologie is in licentie gegeven aan een bedrijf voor commerciële ontwikkeling.
Natuurlijke inspiratie
RNA-interferentie is een natuurlijk voorkomend fenomeen dat wetenschappers proberen uit te buiten sinds de ontdekking in 1998. Fragmenten van RNA, bekend als kort interfererend RNA (siRNA), schakelen specifieke genen in levende cellen uit door de boodschapper-RNA-moleculen te vernietigen die de instructies van het DNA naar de rest van de cel.
Wetenschappers hopen dat deze aanpak nieuwe behandelingen kan bieden voor ziekten veroorzaakt door enkelvoudige mutaties, zoals de ziekte van Huntington, of kanker, door gemuteerde genen te blokkeren die kankergedrag bevorderen. Echter, het ontwikkelen van RNAi-therapieën is een uitdaging gebleken omdat het moeilijk is om grote hoeveelheden siRNA op de juiste plaats af te leveren zonder bijwerkingen in andere weefsels of organen te veroorzaken.
In eerdere onderzoeken is Anderson en Langer toonden aan dat ze met kleine doses siRNA meerdere genen konden blokkeren door het RNA in vetachtige moleculen, lipidoïden genaamd, te wikkelen. In hun laatste werk, de onderzoekers wilden deze deeltjes verbeteren, ze efficiënter maken, selectiever, en veiliger, zegt Yizhou Dong, een postdoc aan het Koch Institute en hoofdauteur van het artikel.
"We wilden echt materialen ontwikkelen voor klinisch gebruik in de toekomst, "zegt hij. "Dat is ons uiteindelijke doel met het materiaal om te bereiken."
De ontwerpinspiratie voor de nieuwe deeltjes kwam uit de natuurlijke wereld, in het bijzonder kleine deeltjes bekend als lipoproteïnen, die cholesterol en andere vetmoleculen door het lichaam transporteren.
Net als lipoproteïne-nanodeeltjes, de nieuwe lipopeptidedeeltjes van het MIT-team zijn bollen waarvan de buitenmembranen zijn samengesteld uit lange ketens met een vettige lipidestaart die naar het deeltje is gericht. In de nieuwe deeltjes het hoofd van de ketting, die naar buiten gericht is, is een aminozuur (de bouwstenen van eiwitten). Strengen van siRNA worden in de bol gedragen, omgeven door meer lipopeptide-moleculen. In het membraan ingebedde cholesterolmoleculen en een buitenste laag van het polymeer PEG helpen de structuur te stabiliseren.
De onderzoekers stemden de chemische eigenschappen van de deeltjes af, die hun gedrag bepalen, door de aminozuren in de deeltjes te variëren. Er zijn 21 aminozuren gevonden in meercellige organismen; de onderzoekers creëerden ongeveer 60 lipopeptidedeeltjes, elk met een ander aminozuur gekoppeld aan een van de drie chemische groepen:een acrylaat, een aldehyde, of een epoxide. Deze groepen dragen ook bij aan het gedrag van de deeltjes.
David Putnam, een universitair hoofddocent biomedische technologie aan de Cornell University, zegt dat hij onder de indruk is van de benadering van het team om na te bootsen hoe het lichaam vetmoleculen met lipoproteïnedeeltjes transporteert.
"Ze hebben die machine gekaapt en iets gemaakt dat lijkt op de lipoproteïnestructuren en siRNA rechtstreeks naar de lever zal brengen. Ze bouwen voort op Moeder Natuur en maken het zo efficiënt mogelijk, " zegt Putnam, die geen deel uitmaakte van het onderzoeksteam.
Gerichte aanval
De onderzoekers testten vervolgens het vermogen van de deeltjes om het gen voor een bloedstollingseiwit genaamd Factor VII uit te schakelen. die in de lever wordt geproduceerd door cellen die hepatocyten worden genoemd. Het meten van Factor VII-niveaus in de bloedbaan laat zien hoe effectief de siRNA-silencing is.
In dat beginscherm, het meest efficiënte deeltje bevatte het aminozuur lysine gekoppeld aan een epoxide, dus de onderzoekers creëerden nog eens 43 nanodeeltjes vergelijkbaar met die, voor verder testen. De beste van deze verbindingen, bekend als cKK-E12, bereikte gen-uitschakeling vijf keer efficiënter dan die bereikt met een eerder siRNA-bezorgingsvehikel.
In een apart experiment de onderzoekers leverden siRNA om een tumorsuppressorgen te blokkeren dat in alle lichaamsweefsels tot expressie wordt gebracht. Ze ontdekten dat de afgifte van siRNA heel specifiek was voor de lever, die het risico van off-target bijwerkingen zou moeten minimaliseren.
"Dat is belangrijk omdat we niet willen dat het materiaal alle doelen in het menselijk lichaam tot zwijgen brengt, ", zegt Dong. "Als we patiënten met een leverziekte willen behandelen, we willen alleen doelen in de lever het zwijgen opleggen, geen andere celtypen."
In tests bij niet-menselijke primaten, de onderzoekers ontdekten dat de deeltjes een gen genaamd TTR (transthyretine) effectief konden dempen, die is betrokken bij ziekten, waaronder seniele systemische amyloïdose, familiale amyloïde polyneuropathie, en familiale amyloïde cardiomyopathie.
Het MIT-team probeert nu meer te weten te komen over hoe de deeltjes zich gedragen en wat er met ze gebeurt als ze eenmaal zijn geïnjecteerd. in de hoop de prestaties van de deeltjes verder te verbeteren. Ze werken ook aan nanodeeltjes die zich richten op andere organen dan de lever, wat een grotere uitdaging is omdat de lever een natuurlijke bestemming is voor vreemd materiaal dat uit het bloed wordt gefilterd.
Dit verhaal is opnieuw gepubliceerd met dank aan MIT News (web.mit.edu/newsoffice/), een populaire site met nieuws over MIT-onderzoek, innovatie en onderwijs.
 Nieuw chemisch proces een eerste stap naar het maken van nucleaire brandstof met vuur
Nieuw chemisch proces een eerste stap naar het maken van nucleaire brandstof met vuur Banden die binden, en kan worden losgemaakt
Banden die binden, en kan worden losgemaakt Wetenschappers ontwikkelen een nieuwe methode om de efficiëntie van luchtreinigers te verbeteren
Wetenschappers ontwikkelen een nieuwe methode om de efficiëntie van luchtreinigers te verbeteren De mechanische eigenschappen van JIS SCM 420H staal
De mechanische eigenschappen van JIS SCM 420H staal  Peel-off coating houdt ontzilting schoner en groener
Peel-off coating houdt ontzilting schoner en groener
 De kust doseren:de lekkende leidingen van Baltimore County genezen de Chesapeake Bay
De kust doseren:de lekkende leidingen van Baltimore County genezen de Chesapeake Bay Nieuwe studie kan een revolutie teweegbrengen in de manier waarop we recyclen
Nieuwe studie kan een revolutie teweegbrengen in de manier waarop we recyclen Herstel na groot sterven werd vertraagd door meer uitstervingen
Herstel na groot sterven werd vertraagd door meer uitstervingen De moleculaire kenmerken van opgeloste organische stof in een eutrofe kustbaai
De moleculaire kenmerken van opgeloste organische stof in een eutrofe kustbaai Egypte wil katoenrenaissance weven
Egypte wil katoenrenaissance weven
Hoofdlijnen
- Opwarming van de oceaan signaleert verandering van dieet voor Europese aalscholvers
- Wetenschappers zouden supermodelbouwers moeten zijn
- Hoe evolueert het leven?
- De Stoned Ape-hypothese:hebben paddo's de menselijke evolutie beïnvloed?
- De oorsprong van genen voor het maken van bloemen
- Hoe natuurlijke selectie werkt
- Het verschil tussen een sporofyt en gametofyt
- Plant: definitie, evolutie, taxonomie
- Koeltechnologie om de levensvatbaarheid van het gekoelde muizensperma gedurende 10 dagen te behouden
- Grootte bepaalt hoe nanodeeltjes biologische membranen beïnvloeden
- Diffusie en detectie op afstand van hete dragers in grafeen

- Kleine lezer maakt snel, goedkope DNA-sequencing mogelijk
- Team gebruikt gouden lolly om ongrijpbaar interferentie-effect op nanoschaal te observeren

- De rauwe kracht van menselijke beweging
 Model voor het voorspellen van een sneeuwlaag in de bergen geeft een duidelijker beeld van de afvoer in het voorjaar, gevolgen van klimaatverandering
Model voor het voorspellen van een sneeuwlaag in de bergen geeft een duidelijker beeld van de afvoer in het voorjaar, gevolgen van klimaatverandering Team meet het verbreken van een enkele chemische binding
Team meet het verbreken van een enkele chemische binding Renault-aandelen versnellen op Nissan-fusiegesprek
Renault-aandelen versnellen op Nissan-fusiegesprek Hoe waarschijnlijkheid te berekenen
Hoe waarschijnlijkheid te berekenen Star Wars:De evolutie van de Death Star weerspiegelt de groeiende angst van Hollywood voor een klimaatapocalyps
Star Wars:De evolutie van de Death Star weerspiegelt de groeiende angst van Hollywood voor een klimaatapocalyps Graden omzetten in inches of millimeters
Graden omzetten in inches of millimeters Wetenschappers stellen 3D-grafeenachtige hyper-honingraatstructuren voor
Wetenschappers stellen 3D-grafeenachtige hyper-honingraatstructuren voor Magnetische nanokubussen assembleren zichzelf tot spiraalvormige superstructuren
Magnetische nanokubussen assembleren zichzelf tot spiraalvormige superstructuren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Portuguese | Swedish | German | Dutch | Danish | Norway | Spanish |

-
Wetenschap © https://nl.scienceaq.com

