
Wetenschap
Chemici remmen een kritische versnelling van celonsterfelijkheid
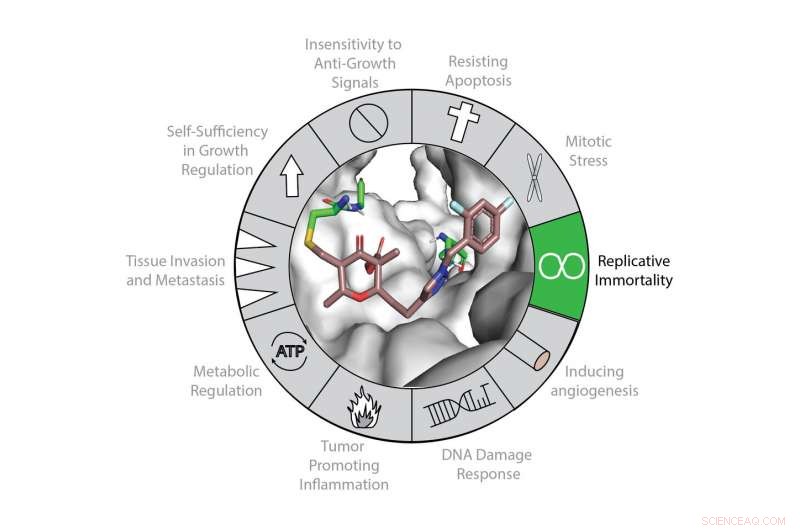
Telomerase-expressie draagt voornamelijk bij aan de "kenmerken van kanker" door zijn canonieke rol bij het onderhoud van telomeren en replicatieve sterfte. Telomerase (weergegeven in grijs) kan worden geremd met een nieuwe klasse van covalente inactivatoren (weergegeven in kleur). Krediet:Northwestern University
Een van de kenmerken van kanker is celonsterfelijkheid. Een organisch chemicus van de Northwestern University en zijn team hebben nu een veelbelovend moleculair hulpmiddel ontwikkeld dat zich richt op en remt op een van de onderliggende versnellingen van celonsterfelijkheid:het enzym telomerase.
Dit enzym wordt in ongeveer 90% van de menselijke kankercellen tot overexpressie gebracht en is een belangrijk onderwerp van studie geworden voor kankeronderzoekers. Normale cellen hebben het gen voor telomerase, maar het wordt meestal niet uitgedrukt.
"Telomerase is het primaire enzym dat ervoor zorgt dat kankercellen voor altijd kunnen leven, " zei Karl A. Scheidt, die het onderzoek leidde. "We willen deze onsterfelijkheid kortsluiten. Nu hebben we een eerste in zijn soort klein molecuul ontworpen dat onomkeerbaar bindt aan telomerase, haar activiteit stopzetten. Dit mechanisme biedt een nieuwe weg voor de behandeling van kanker en het begrijpen van cellulaire veroudering."
Scheidt is hoogleraar scheikunde aan het Weinberg College of Arts and Sciences en hoogleraar farmacologie aan de Northwestern University Feinberg School of Medicine.
Het grote idee voor het ontwerp van kleine moleculen kwam uit de natuur. Een decennium geleden, Scheidt was geïntrigeerd door de biologische activiteit van chrolactomycine, dat wordt geproduceerd door bacteriën en waarvan is aangetoond dat het telomerase remt.
Scheidt en zijn team gebruikten chrolactomycine als uitgangspunt bij het ontwerp van hun kleine moleculen. Ze produceerden in de loop der jaren meer dan 200 verbindingen, en de verbinding die ze NU-1 noemen, was de meest effectieve van de geteste. De synthese is zeer efficiënt, minder dan vijf stappen nemen.
"NU-1 remt telomerase in tegenstelling tot alles wat eraan voorafging, "Zei Scheidt. "Het doet dit door een covalente binding te vormen. Een ander voordeel van NU-1 is dat de moleculaire structuur wetenschappers in staat moet stellen lading toe te voegen, zoals een therapeut."
De studie werd vorige week gepubliceerd door het tijdschrift ACS Chemische Biologie .
Alle menselijke cellen hebben telomeren, korte DNA-sequenties die de uiteinden van elke DNA-streng afdekken. Het is hun taak om onze chromosomen en DNA te beschermen. Als een cel zich deelt, de telomeren worden korter totdat ze hun werk niet meer kunnen doen. Natuurlijke celdood volgt.
In tegenstelling tot, kankercellen, met hun verhoogde telomerase-activiteit, onsterfelijk worden door het normale proces van telomeerverkorting om te keren. Het enzym telomerase kopieert telomeren keer op keer, verlenging van de telomeren. Het resultaat is onbeperkte celdeling en onsterfelijkheid. De beroemde HeLa-cellen, geïsoleerd uit het baarmoederhalskankerweefsel van Henrietta Lacks in de jaren vijftig, zijn nog aan het verdelen.
Telomerase is al tientallen jaren een doelwit voor onderzoek naar kankertherapieën. In 2009, drie wetenschappers ontvingen de Nobelprijs voor Fysiologie of Geneeskunde voor hun eerdere onderzoek naar telomeren en telomerase.
Na het ontwikkelen van hun nieuwe verbindingen, Scheidt en zijn team zijn een samenwerking aangegaan met professor Stephen Kron van de Universiteit van Chicago en Scott Cohen van het Children's Medical Research Institute in Sydney om de extra-telomere rol van telomerase-remming te onderzoeken.
De onderzoeken waren gericht op hoe de nieuwe verbindingen op moleculair niveau interageren met telomerase en hoe telomeraseremming cellen gevoelig maakt voor chemotherapie en bestraling. Van dit werk, NU-1 steeg naar de top.
"Door deze studie te publiceren, we testen dit voortreffelijke hulpmiddel om te zien wat het kan doen en om meer te leren over telomerase, "Zei Scheidt. "We blijven het ook beter maken."
Het onderzoek is gedaan in menselijke cellen. De volgende stappen, Scheidt zei, zijn om krachtigere verbindingen te maken en deze in diermodellen te onderzoeken.
 Pinda-familiegeheim voor het maken van chemische bouwstenen onthuld
Pinda-familiegeheim voor het maken van chemische bouwstenen onthuld Oude waterzuiveringsmethoden
Oude waterzuiveringsmethoden  Zelfherstellend materiaal kan zichzelf opbouwen uit koolstof in de lucht
Zelfherstellend materiaal kan zichzelf opbouwen uit koolstof in de lucht Onderzoekers rapporteren nieuwe oxyfluorideverbinding voor fotokatalyse
Onderzoekers rapporteren nieuwe oxyfluorideverbinding voor fotokatalyse Meer zien met PET-scans:verrassend nieuw mechanisme voor bevestiging van chemische tracers ontdekt
Meer zien met PET-scans:verrassend nieuw mechanisme voor bevestiging van chemische tracers ontdekt
 Onderzoek naar ecologische en technologische effecten op cultuurevolutie op verschillende ruimtelijke schalen
Onderzoek naar ecologische en technologische effecten op cultuurevolutie op verschillende ruimtelijke schalen De effecten van menselijke activiteit op de koolstofcyclus
De effecten van menselijke activiteit op de koolstofcyclus VS zet zich schrap voor extreme hitte nu de weekendtemperaturen stijgen
VS zet zich schrap voor extreme hitte nu de weekendtemperaturen stijgen Pilootproject om te waarschuwen voor potentieel gevaarlijke meteotsunami-golven in de Grote Meren
Pilootproject om te waarschuwen voor potentieel gevaarlijke meteotsunami-golven in de Grote Meren Hittegolftemperaturen in India passeren 50 Celsius
Hittegolftemperaturen in India passeren 50 Celsius
Hoofdlijnen
- Genetische veranderingen helpen muggen om aanvallen van pesticiden te overleven
- Neushoornstroper krijgt 20 jaar cel in Zuid-Afrika
- Hoe een tRNA-sequentie uit een DNA-sequentie te krijgen
- De voordelen van het bestuderen van cellen onder een lichtmicroscoop
- Nieuwe studie benadrukt de effecten van een wereldwijde strategie om de antibioticaconsumptie in de productie van voedseldieren te verminderen
- Waarom blozen mensen?
- Fasen van de cardiale actiepotentiaal
- Hoe de lengte van DNA-fragmenten
- Hoe wordt een bij een bijenkoningin?
- Origami diagnostisch apparaat biedt betaalbare malariadiagnoses

- Loodhalogenideperovskieten zijn niet ferro-elektrisch

- Wetenschappers vinden een manier om DNA-oppervlaktehybridisatie te versnellen

- Kristallen bouwen op een zeer heet oppervlak

- Wiskundig model van thermoplastisch composiet helpt bij het ontwerpen en certificeren van zeer betrouwbare constructies
 Gemanipuleerde microben kunnen biologisch afbreekbare kunststoffen produceren tegen lagere kosten en milieu-impact dan plantaardige kunststoffen
Gemanipuleerde microben kunnen biologisch afbreekbare kunststoffen produceren tegen lagere kosten en milieu-impact dan plantaardige kunststoffen Hoe weet ik of een pauw mannelijk of vrouwelijk is
Hoe weet ik of een pauw mannelijk of vrouwelijk is De vulkaan Stromboli in Italië barst uit, vonken enorme aswolk
De vulkaan Stromboli in Italië barst uit, vonken enorme aswolk Spanningen in transistoren berekenen
Spanningen in transistoren berekenen  Herbestemming van dimethyloxalylglycine om het glutaminemetabolisme te remmen
Herbestemming van dimethyloxalylglycine om het glutaminemetabolisme te remmen Neerslag titratie technieken
Neerslag titratie technieken  Computationele tool voor materiaalfysica groeit in populariteit
Computationele tool voor materiaalfysica groeit in populariteit De taal van cellulaire communicatie begrijpen
De taal van cellulaire communicatie begrijpen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

