
Wetenschap
Nieuwe nanodeeltjes helpen sepsisbehandeling bij muizen

Tegoed:CC0 Publiek Domein
Sepsis, de overdreven reactie van het lichaam op een infectie, treft meer dan 1,5 miljoen mensen en alleen al in de VS overlijden er elk jaar minstens 270.000 mensen. De standaardbehandeling van antibiotica en vloeistoffen is voor veel patiënten niet effectief, en degenen die overleven, lopen een hoger risico op overlijden.
In nieuw onderzoek gepubliceerd in het tijdschrift Nature Nanotechnology vandaag rapporteerde het laboratorium van Shaoqin "Sarah" Gong, een professor bij het Wisconsin Institute for Discovery aan de Universiteit van Wisconsin-Madison, een nieuwe op nanodeeltjes gebaseerde behandeling die ontstekingsremmende moleculen en antibiotica levert.
Het nieuwe systeem redde het leven van muizen met een geïnduceerde versie van sepsis die bedoeld was om als model voor menselijke infecties te dienen, en is een veelbelovend proof-of-concept voor een mogelijke nieuwe therapie, in afwachting van aanvullend onderzoek.
De nieuwe nanodeeltjes leverden de chemische stof NAD + of de gereduceerde vorm NAD(H), een molecuul dat een essentiële rol speelt in de biologische processen die energie genereren, genetisch materiaal bewaren en cellen helpen zich aan te passen aan en stress te overwinnen. Hoewel NAD(H) bekend staat om zijn ontstekingsremmende functie, werd klinische toepassing belemmerd omdat NAD(H) niet rechtstreeks door cellen kan worden opgenomen.
"Om klinische vertaling mogelijk te maken, moeten we een manier vinden om NAD(H) efficiënt af te leveren aan de beoogde organen of cellen. Om dit doel te bereiken, hebben we een aantal nanodeeltjes ontworpen die NAD(H) direct in de cel kunnen transporteren en afgeven. , terwijl voortijdige afgifte en afbraak van geneesmiddelen in de bloedbaan wordt voorkomen", zegt Gong, die ook aanstellingen heeft bij de afdeling Biomedische Technologie en de afdeling Oogheelkunde en Visuele Wetenschappen van de UW School of Medicine and Public Health.
Het interdisciplinaire werk werd geleid door Gong samen met Mingzhou Ye en Yi Zhao, twee postdoctorale fellows in het Gong-lab. John-Demian Sauer, een professor in de afdeling Medische Microbiologie en Immunologie, werkte ook mee aan het project.
Sepsis kan dodelijk zijn in twee fasen. Eerst begint een infectie in het lichaam. Het immuunsysteem reageert door een drastische ontsteking te creëren die de bloedstroom belemmert en bloedstolsels vormt, die weefselsterfte kunnen veroorzaken en een kettingreactie kunnen veroorzaken die leidt tot orgaanfalen. Daarna corrigeert het lichaam zichzelf door het immuunsysteem te onderdrukken, wat op zijn beurt de vatbaarheid voor infecties verhoogt. Het beheersen van complicaties veroorzaakt door ontsteking is van vitaal belang bij sepsistherapie.
Het lipide-gecoate calciumfosfaat of metaal-organische raamwerk nanodeeltjes ontworpen door het Gong-lab kunnen worden gebruikt om NAD(H) en antibiotica samen te leveren. Gong's laboratorium testte de NAD(H)-geladen nanodeeltjes in meerdere muismodellen, waaronder endotoxemie, multiresistente pathogeen-geïnduceerde polymicrobiële bacteriëmie, evenals een punctie-geïnduceerd sepsismodel met secundaire infectie door een veelvoorkomende ziekteverwekkende bacterie genaamd P. aeruginosa .
De behandeling met nanodeeltjes presteerde veel beter dan het gebruik van alleen NAD(H). In een muismodel voor endotoxemie stierven muizen zonder enige behandeling of behandeld met vrij NAD(H) binnen twee dagen. Daarentegen overleefden muizen die waren behandeld met NAD(H)-geladen nanodeeltjes allemaal. Deze dierstudies hebben aangetoond dat de NAD(H)-nanodeeltjes kunnen helpen een gezond immuunsysteem te behouden, de bloedvatenfunctie te ondersteunen en multi-orgaanschade te voorkomen.
Deze technologie kan de weg effenen voor de ontwikkeling van een nieuwe klinische therapie voor sepsis die ook kan worden toegepast in andere ontstekingsgerelateerde scenario's, zoals de behandeling van COVID-19. Een bijkomend voordeel van deze therapie is het vermogen om infecties te behandelen met lagere hoeveelheden antibiotica, waardoor overmatig gebruik wordt verminderd. Verder onderzoek in grotere diermodellen zal nodig zijn voordat klinische proeven bij mensen kunnen beginnen.
"De NAD(H)-nanodeeltjes hebben het potentieel om vele andere ziekten te behandelen, omdat NAD(H) betrokken is bij zoveel biologische routes. Er is sterk bewijs voor het gebruik van NAD(H) als interventie of hulpmiddel bij kritieke ziekten," zegt Gong. + Verder verkennen
Onderzoekers ontwikkelen IV-injectiebehandeling voor sepsis
 Eten voor je gezondheid is ook beter voor het milieu, studie toont
Eten voor je gezondheid is ook beter voor het milieu, studie toont Onderzoekers ontdekken hogere milieu-impact door uitstoot van kookfornuis
Onderzoekers ontdekken hogere milieu-impact door uitstoot van kookfornuis Het testen van de haalbaarheid van de VN-doelstellingen voor duurzame ontwikkeling op het gebied van water en sanitatie
Het testen van de haalbaarheid van de VN-doelstellingen voor duurzame ontwikkeling op het gebied van water en sanitatie Het beperken van de opwarming tot 1,5 graad C zou de meeste soorten wereldwijd redden van klimaatverandering
Het beperken van de opwarming tot 1,5 graad C zou de meeste soorten wereldwijd redden van klimaatverandering Methaanniveaus zijn gestegen in de regio Marcellus Shale ondanks een dip in de installatie van een put
Methaanniveaus zijn gestegen in de regio Marcellus Shale ondanks een dip in de installatie van een put
Hoofdlijnen
- Welke cellen kunnen door het menselijk oog worden gezien?
- Domme mensen zijn verrassend zelfverzekerd
- What Influences Phenotype?
- Dawn of fishes:vroeg-silurische kaken van gewervelde dieren van kop tot staart onthuld
- Cat Chromosome Information
- Door schadesporen in kaart te brengen, kunnen onderzoekers het water volgen in Photosystem II
- Hersenen van zombie-mieren intact gelaten door schimmelparasiet
- Wetenschappers ontdekken dat genen worden aangestuurd door nanovoetballen
- Onderzoekers ontdekken slecht begrepen bacteriële lijnen in de monden van dolfijnen
- Gouden nanodeeltjes voor gerichte kankerbehandeling

- De mogelijkheden van de nanowereld benutten

- Onderzoekers helpen om biovriendelijke materialen te gebruiken bij het ontwerpen van medicijnen voor neurologische aandoeningen
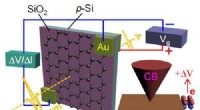
- Geëlektrificeerd grafeen een sluiter voor licht
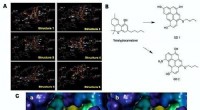
- Onderzoekers onderzoeken de volledige thermo-elektrische eigenschappen van een enkel molecuul

 Experimentele kosmologengroep lanceert zijn eerste iteraties van ruimtereizende wafercraft
Experimentele kosmologengroep lanceert zijn eerste iteraties van ruimtereizende wafercraft Studie onderzoekt obesitas en reproductieve status van dierentuinolifanten
Studie onderzoekt obesitas en reproductieve status van dierentuinolifanten Op kobalt gebaseerde katalysatoren kunnen de productie van waterstof uit water op industriële schaal versnellen
Op kobalt gebaseerde katalysatoren kunnen de productie van waterstof uit water op industriële schaal versnellen Wat is het gebruik van benzeen?
Wat is het gebruik van benzeen?  Onderzoekers maken ultragevoelige kankerdetector van 2D-materialen
Onderzoekers maken ultragevoelige kankerdetector van 2D-materialen  Beschrijf een evenwichtig ecosysteem
Beschrijf een evenwichtig ecosysteem  Molaire absorptie berekenen
Molaire absorptie berekenen  Wat zijn de functies van co-enzymen?
Wat zijn de functies van co-enzymen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

