
Wetenschap
Met epirubicine geladen nanogeneesmiddelen verslaan weerstand tegen blokkade van immuuncheckpoints bij glioblastoom
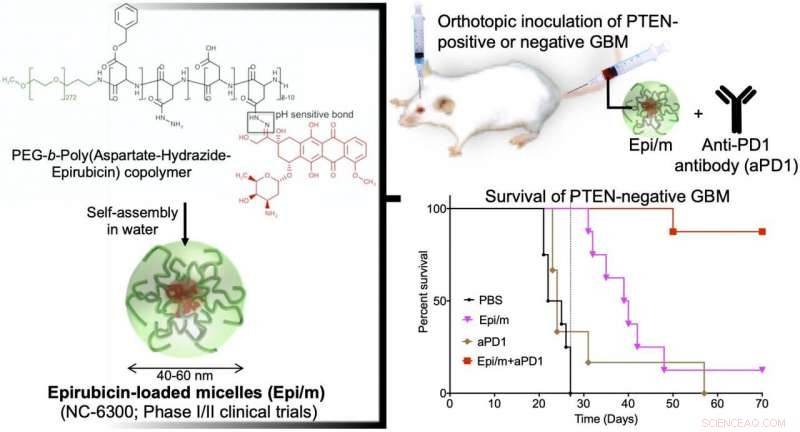
Links:Hydrofoob epirubisine is geconjugeerd aan één uiteinde van de hydrofiele polyethyleenglycol (PEG) keten met aspartaat-hydrazide als een linker. In water, dit molecuul is zelf-geassembleerd om nano-micellen (Epi/m) te vormen. Rechtsboven:PTEN(+) of PTEN(-) GBM werd getransplanteerd in de hersenen van muizen, en Epi/m en anti-PD1-antilichaam (aPD1) werden toegediend via de staartader om de overlevingsperiode te evalueren. Rechtsonder:Vergelijking overlevingsperiode bij PTEN(-)GBM. Aan de controlegroep werd PBS (fosfaatbufferoplossing) toegediend. Als resultaat, geen van de controlegroep (zwart) kon langer dan 30 dagen (8/8) overleven. Alleen de groep Epi/m (roze) stierf geleidelijk na 30 dagen, de helft (4/8) in 40 dagen, en 7/8 bij 50 dagen. aPD1 alleen (bruin) doodde 6/7 binnen 30 dagen. In tegenstelling tot, met Epi/m+aPD1 (rood), 1/8 stierf 50 dagen later, maar 7/8 waren zelfs na 3 maanden nog in leven. Krediet:2020 Innovatiecentrum van NanoMedicine
Een op nanogeneeskunde gebaseerde strategie voor chemo-immunotherapie (CIT) van glioblastoom (GBM), die de slechtste prognose heeft onder hersentumoren, succesvol is ontwikkeld. In vivo-experimenten hebben aangetoond dat het gecombineerde gebruik van epirubicine-inkapselende nano-micellen (Epi/m) met immuuncheckpointremmers (ICI) PTEN-negatieve GBM, die zeer resistent is tegen ICI alleen. Vanwege de synergetische effecten van de combinatie Epi/m plus ICI, het aantal tumor-infiltrerende T-cellen (TIL) en andere antitumor-immuuncellen nam significant toe om kankercellen effectief te doden.
Anderzijds, intratumorale beenmerg-afgeleide immunosuppressieve cellen (MDSC), die interfereren met de immuunrespons, aanzienlijk waren verminderd. Het CIT leverde ook robuuste immunologische geheugeneffecten tegen de tumoren, die effectief nieuw geïmplanteerde PTEN-negatieve GBM-cellen in de hersenen verwierp. Hoewel vrij epirubicine schade aan organen kan veroorzaken, met inbegrip van hematopoëtische organen in het bijzonder, onze nanogeneeskundestrategie verminderde deze bijwerkingen aanzienlijk, verbetering van de immuunrespons. Epi/m is al gevorderd in klinische proeven voor andere kankertypes, en deze CIT-strategie zal naar verwachting in de toekomst worden vertaald naar klinische evaluatie. Deze resultaten zijn gepubliceerd in ACS Nano op 6 augustus door de American Chemical Society.
Het Innovation Center of Nanomedicine (Directeur:Prof. Kazunori Kataoka, Locatie:Kawasaki-stad, Afkorting:iCONM) kondigde aan dat een nieuwe therapeutische optie voor glioblastoom (GBM) is aangetoond bij muizen, in een samenwerkingsstudie met de afdeling Bioengineering, Graduate School of Engineering, De Universiteit van Tokio. GBM is een hersentumor met een extreem snelle progressie en een slechte prognose (5-jaarsoverleving:10,1%). Hoewel verschillende verbindingen in klinische onderzoeken worden geëvalueerd, er is geen therapeutische optie om de overlevingsperiode significant te verbeteren. Vooral, patiënten met afwijkingen in het PTEN-gen, een van de kankersuppressorgenen, zijn zeer resistent tegen de momenteel beschikbare therapieën en hebben hoge medische behoeften.
In het algemeen, immuuncheckpointremmers (ICI's) worden als niet effectief beschouwd tegen GBM, aangezien GBM immunosuppressief is met lage T-celinfiltratie. In de methode die in dit artikel wordt gepresenteerd, iCONM's technologie voor het toedienen van nanodrugs maakt selectieve tumoraccumulatie van epirubicine mogelijk, die immunogene celdood (ICD) veroorzaakt, aan tumorweefsels, daarbij, lokaal veroorzaken van ICD voor synergie met ICI. Als resultaat, deze op nanomedicine gebaseerde chemo-immunotherapie (CIT) was effectief bij muizen die waren getransplanteerd met GBM in de hersenen (hierna GBM-muismodel genoemd), en slaagde erin de overleving van muizen aanzienlijk te verlengen. De combinatie van de met epirubicine beladen nano-micellen behandelde muizen vertoonde een hoge infiltratie van cytotoxische T-cellen (TIL) en verminderde beenmerg-afgeleide immunosuppressieve cellen (MDSC). Uiteindelijk werd onderdrukking van de immuuncheckpointfunctie waargenomen.
Mutaties in het PTEN-gen komen vaak voor in GBM, resulterend in immunosuppressieve routes die de resistentie tegen ICI's bevorderen. Dus, terwijl ICI's 40% van de tumoren hebben uitgeroeid in een muis GBM-model waarin het PTEN-gen normaal is, in een model waarin het PTEN-gen werd uitgeschakeld, ICI's waren niet in staat om de overleving van muizen te verlengen. Op cellulair niveau, er werd gevonden dat PTEN-deficiënte cellen (CT2A-luc) ongeveer 5 keer meer PDL1 tot expressie brachten dan die van normale cellen, wat waarschijnlijk verband houdt met de therapeutische resistentie bij ICI. Aangezien epirubicine het vermogen heeft getoond om PDL1-expressie in tumoren te onderdrukken, zoals borstkanker, het zou mogelijk zijn om de PDL1-niveaus van GBM te verlagen als er voldoende epirubicine kan worden afgegeven in GBM-laesies. Dus, CIT met nanocellen die epirubicine (Epi/m) bevatten in combinatie met ICI werden gebruikt om de antitumorwerking tegen GBM te versterken.
In een GBM-model met normale PTEN-expressie (GL261-luc), Epi/m2 (5 mg/kg op Epi-basis) plus anti-PD1-antilichamen (5 mg/kg) resulteerden in de overleving van alle muizen gedurende meer dan 70 dagen, met een opmerkelijke verlenging van de overlevingstijd. Bij dit model is Met PBS behandelde muizen stierven binnen 30 dagen, muizen behandeld met alleen anti-PD1-antilichamen (5 mg/kg) lieten 40% van de muizen ten minste 70 dagen overleven, en Epi/m (5 mg/kg Epi-basis) resulteerde in een overleving van 80% van de muizen gedurende meer dan 70 dagen. In tegenstelling tot, in het PTEN-deficiënte model (CT2A-luc), Epi/m2 (5 mg/kg op Epi-basis) plus anti-PD1-antilichamen (5 mg/kg) resulteerden in slechts 30% overleving van muizen gedurende meer dan 70 dagen, en voor de andere controlegroepen kon geen duidelijk overlevingseffect worden bevestigd. Wanneer de dosis werd verhoogd tot 15 mg/kg Epi/m2 (in Epi-basis) en gecombineerd met anti-PD1-antilichamen (5 mg/kg), 90% van de muizen kon meer dan 70 dagen overleven, opmerkelijk verlenging van de overleving van muizen.
 Onderzoek toont aan dat de oxidatietoestand van zink kan worden gemaakt +3, de elementenchemie fundamenteel veranderen
Onderzoek toont aan dat de oxidatietoestand van zink kan worden gemaakt +3, de elementenchemie fundamenteel veranderen 3D geordend kanaal verbetert elektrokatalyse
3D geordend kanaal verbetert elektrokatalyse Klimaatvriendelijke architectuur dankzij natuurlijke vouwmechanismen
Klimaatvriendelijke architectuur dankzij natuurlijke vouwmechanismen Nieuwe biosensoren detecteren snel coronaviruseiwitten en antilichamen
Nieuwe biosensoren detecteren snel coronaviruseiwitten en antilichamen Onderzoekers ontwerpen nieuwe moleculen die de brandstofefficiëntie verhogen
Onderzoekers ontwerpen nieuwe moleculen die de brandstofefficiëntie verhogen
Hoofdlijnen
- Groene Brexit laten werken voor landbouw en milieu
- Wat is Ceramide?
- Hoe converteert ADP naar ATP?
- Onderzoekers traceren de oorsprong van aardappelen, meer te weten komen over het onbenutte potentieel ervan
- Wat is vergelijkende biochemie?
Vergelijkende biochemie kan een vaag begrip zijn met meerdere betekenissen, alhoewel het boeiende interacties tussen organismen en hun biologieën kan onthullen. Op zijn minst noemen wetenschappers het een interdiscip
- DNA-onderzoek in de Stille Oceaan onthult een toename van 2000 procent in onze kennis van de biodiversiteit van weekdieren
- Wat zijn de functies van een levercel?
- Voelen planten pijn?
- Vissen hebben complexe persoonlijkheden, uit onderzoek blijkt
- Hoe reageren groene algen op koolstofnanobuisjes?
- Eerste blik op waterstof op het grensvlak van metaal-op-metaalhydride
- Het geheugen voor het vastleggen van ladingen in nanografeen kan de flits verder miniaturiseren

- Dendrimeertechnologie krijgt grip op celeiwitten, kan de kankerbehandeling verbeteren

- Onderzoekers onthullen hoogwaardige CNT-katalysator met betrekking tot zijn elektrogeleiding

 PV, wind, batterijen:onderzoek naar energievooruitzichten
PV, wind, batterijen:onderzoek naar energievooruitzichten Na EPA-flip, een duw om schadelijke pesticiden te blokkeren
Na EPA-flip, een duw om schadelijke pesticiden te blokkeren Dit draagbare apparaat camoufleert zijn drager, ongeacht het weer
Dit draagbare apparaat camoufleert zijn drager, ongeacht het weer Hogere-orde topologische supergeleiding in monolaag op ijzer gebaseerde supergeleider
Hogere-orde topologische supergeleiding in monolaag op ijzer gebaseerde supergeleider Natuurkundigen vangen licht in nanoresonatoren voor recordtijd
Natuurkundigen vangen licht in nanoresonatoren voor recordtijd Veranderende technologie en kijkgewoonten kunnen Super Bowl-reclame in gevaar brengen
Veranderende technologie en kijkgewoonten kunnen Super Bowl-reclame in gevaar brengen Voorgestelde houtkapwetten van NSW waarderen hout boven milieubescherming
Voorgestelde houtkapwetten van NSW waarderen hout boven milieubescherming Rassen- en genderdiscriminatie onder tieners die worden blootgesteld aan datinggeweld
Rassen- en genderdiscriminatie onder tieners die worden blootgesteld aan datinggeweld
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

