
Wetenschap
Waarom kan een geschudde frisdrank op de oceaanbodem ontploffen?
Vm/Getty-afbeeldingen
Het overkomt de besten van ons. Een blikje (of fles) frisdrank wordt geschud, en zodra je de dop opendoet, spuiten de drank en de bubbels eruit. Het kan een echte puinhoop veroorzaken op het aanrecht, op de vloer, op je kleding en op je handen. Als dat bovengronds gebeurt, heb je er dan ooit over nagedacht wat er zou gebeuren als je een frisdrankblikje op de oceaanbodem zou schudden en openen? Misschien ben je nieuwsgierig geweest naar frisdrank die explodeert in de vriezer of naar Mentos die frisdrank laat exploderen. Het openen van een geschud blik op de oceaanbodem is een veel meer niche-experiment, maar de beroemde Canadese astronaut kolonel Chris Hadfield heeft het antwoord.
In 2010 sloot Hadfield zich aan bij de 14e expeditie van NASA Extreme Environment Mission Operations in het Aquarius Laboratory, dat zich 19 meter (ongeveer 62 voet) onder het oppervlak van de kustwateren van Florida bevindt. Het doel was om ruimtemissies te simuleren, gedragsgezondheid te bestuderen, het immuunsysteem te beoordelen en meer. Maar het was niet alleen maar werk en geen spel. In een YouTube-video gepost door Rare Earth – een account onder toezicht van Hadfields zoon Evan – vertelt de astronaut het publiek om hun frisdrank thuis niet te schudden vanwege de dreigende explosie van pop. Hij schudt een blikje Coca-Cola terwijl hij praat en huivert terwijl hij het lipje naar voren trekt, en... er gebeurt niets. Hadfield neemt een slokje en zegt:"Ah, er zit een lekker bruisje in. Het is in orde. Alsjeblieft. Een van de voordelen van leven onder de oceaan."
Waarom een geschud blikje frisdrank niet onder water ontploft
Jonathan Knowles/Getty Images
Om te begrijpen waarom er niets gebeurde toen Hadfield de geschudde Coca-Cola opende terwijl hij op de oceaanbodem woonde, moet je weten waarom frisdrank explodeert als het boven water wordt geschud. Zoals u waarschijnlijk al weet, is het bruisend maken van frisdrank een van de toepassingen van kooldioxidegas. De blikjes (en flessen) worden onder druk gezet terwijl het gas wordt toegevoegd, waardoor de oplosbaarheid van het CO2 toeneemt en het in de vloeistof kan oplossen. Vervolgens bezinken het gas in de frisdrank en het resterende gas boven de frisdrank in een chemisch evenwicht, wat eenvoudigweg betekent dat de snelheid waarmee CO2 oplost in en vrijkomt uit de vloeistof gelijk is.
Omdat de druk in het blik (ongeveer 250 kPa) groter is dan de atmosferische druk (ongeveer 100 kPa), ontstaat er een onbalans bij het verbreken van de verzegeling. De drukval verlaagt de oplosbaarheid van het CO2, waardoor het uit de frisdrank bruist in de vorm van bruisende belletjes. Daarom gaat frisdrank na een tijdje leeg. Wanneer je het blikje schudt voordat je het opent, kan de CO2 boven de frisdrank nergens heen omdat de vloeistof al verzadigd is. In plaats van op te lossen in de vloeistof, vormen zich belletjes. Wanneer de verzegeling wordt verbroken, bruist het opgeloste CO2 uit het gehele beschikbare oppervlak, en het toegevoegde oppervlak binnen de bellen zorgt ervoor dat het opgeloste gas sneller kan ontsnappen. Deze reactie zorgt ervoor dat de frisdrank uit het blik "explodeert" in de vorm van schuim.
Op ongeveer 20 meter onder het oceaanoppervlak ervaart het Aquarius Laboratory echter een druk van ongeveer 2,5 atmosfeer, dus alles en iedereen in het laboratorium ervaart ongeveer 2,5 keer de druk van het zeeniveau. Deze hogere atmosferische druk, die ongeveer gelijk is aan de druk in het blikje, betekent dat er geen drukonevenwicht is wanneer het blikje wordt geopend. Daarom verandert de oplosbaarheid van het gas nooit, waardoor een explosie van schuim wordt voorkomen, zelfs na het schudden van de frisdrank. Een ander gelukkig gevolg van dit evenwicht in druk is dat het bruisen van de frisdrank ook langer aanhoudt.
 Noors fonds zet meer kolengroepen op de zwarte lijst vanwege klimaatproblemen
Noors fonds zet meer kolengroepen op de zwarte lijst vanwege klimaatproblemen Wat planten nodig hebben om droogte te weerstaan
Wat planten nodig hebben om droogte te weerstaan  Sri Lankaanse functionarissen zetten zich schrap voor olielek van zinkend schip
Sri Lankaanse functionarissen zetten zich schrap voor olielek van zinkend schip De aarde zal geen nieuw water krijgen, ook al regent het niet. Leg uit?
De aarde zal geen nieuw water krijgen, ook al regent het niet. Leg uit?  10 Oorzaken van luchtverontreiniging
10 Oorzaken van luchtverontreiniging
Hoofdlijnen
- Hoe lang tussen de evolutie van enkele versus meercellige organismen?
- Wat zijn de grenzen aan dingen die wetenschappers in hun werk kunnen bestuderen?
- Welke soorten moleculen kunnen door het plasmamembraan passeren via eenvoudige diffusie?
- Welk gebied van biologie vereist microscoop?
- Wat is de microscopische eenvoudige planten met één cellen, sommige zijn schadelijk nuttig geclassificeerd volgens vorm?
- Hoe sommige weefsels kunnen 'ademen' zonder zuurstof
- Wat doen wetenschappers om een hypothese te maken?
- Wat is het verschil tussen aerobe en een bacteriën?
- Wat is Speratogenese?
- Onderzoekers demonstreren veelbelovende methode voor het verbeteren van de verwerking van kwantuminformatie

- Nieuwe theorie legt verbanden tussen Planckiaanse metalen en zwarte gaten

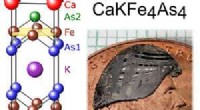
- Ontbrekende link naar nieuwe supergeleiding onthuld
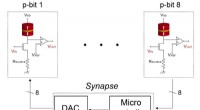
- Qubit van arme mensen kan kwantumproblemen oplossen zonder kwantum te gaan
- Recordbrekende laserverbinding zou de theorie van Einstein kunnen testen

 13 vissoorten met adembenemende tanden die wetenschappers verbazen
13 vissoorten met adembenemende tanden die wetenschappers verbazen  Wat is de naam voor zeven grote landmassa's?
Wat is de naam voor zeven grote landmassa's?  Wat is 1 deel schoner voor ons gallon water?
Wat is 1 deel schoner voor ons gallon water?  Is menselijke biologie hetzelfde als anatomie?
Is menselijke biologie hetzelfde als anatomie?  De beweging van een object dat in de hoek wordt gegooid, is welke beweging?
De beweging van een object dat in de hoek wordt gegooid, is welke beweging?  Hoe wordt energie overgedragen in de atmosfeer in de oceanen?
Hoe wordt energie overgedragen in de atmosfeer in de oceanen?  Welk organisme dat vandaag leeft, is gerelateerd aan de trilobiet?
Welk organisme dat vandaag leeft, is gerelateerd aan de trilobiet?  Moeten bedrijven kennis, componenten of systemen verkopen?
Moeten bedrijven kennis, componenten of systemen verkopen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

