
Wetenschap
Intermoleculaire krachten in vloeistof F2:de dispersiekrachten van Londen begrijpen
Dit is waarom:
* F₂ is een niet-polair molecuul: Fluoratomen hebben dezelfde elektronegativiteit, dus de F-F-binding is niet-polair. Het gehele F₂-molecuul mist een permanent dipoolmoment.
* Londense dispersiekrachten zijn aanwezig in alle moleculen: Deze krachten komen voort uit tijdelijke, onmiddellijke fluctuaties in de elektronenverdeling, waardoor tijdelijke dipolen ontstaan die dipolen in aangrenzende moleculen induceren. Hoewel F₂ niet-polair is, komen deze tijdelijke fluctuaties nog steeds voor.
* Andere krachten zijn afwezig: F₂ heeft geen waterstofbinding (geen waterstofatomen die rechtstreeks gebonden zijn aan zeer elektronegatieve atomen) of dipool-dipool-interacties (vanwege de niet-polaire aard ervan).
Daarom zijn de Londense dispersiekrachten de enige significante intermoleculaire kracht die aanwezig is in vloeibare F₂.
 De subeenheden van de lichte keten van therapeutische antilichamen hebben invloed op de prestaties en opbrengst van geneesmiddelen
De subeenheden van de lichte keten van therapeutische antilichamen hebben invloed op de prestaties en opbrengst van geneesmiddelen Verhaalt de dampdruk van een stof met een verhoogde temperatuur?
Verhaalt de dampdruk van een stof met een verhoogde temperatuur?  Wat zijn chemische kenmerken van seleniums?
Wat zijn chemische kenmerken van seleniums?  Wat is de juiste formule voor osmium VIII-sulfiet?
Wat is de juiste formule voor osmium VIII-sulfiet?  Wat is oppervlaktedruk?
Wat is oppervlaktedruk?
 Geologen vinden verloren fragment van het oude continent in het noorden van Canada
Geologen vinden verloren fragment van het oude continent in het noorden van Canada Hoe maak je een ecosysteem in een fles
Hoe maak je een ecosysteem in een fles Aangekapte inheemse bossen eindigen meestal op stortplaatsen, niet in gebouwen en meubels
Aangekapte inheemse bossen eindigen meestal op stortplaatsen, niet in gebouwen en meubels Geochemici meten nieuwe samenstelling van aardmantel
Geochemici meten nieuwe samenstelling van aardmantel Vernietigen waterscooters de planeet?
Vernietigen waterscooters de planeet?
Hoofdlijnen
- Hoe veranderde de evolutietheorie de manier waarop biologen over classificatie dachten?
- Celkern:structuur, functie en raadselantwoord
- Hoe wordt de wetenschap gebruikt in paleontologie?
- Welke twee gepaarde celstructuren worden gekopieerd voordat de mitose begint?
- Wat moet u doen als u het defecte gen heeft?
- Angst voor de dood is van invloed op de manier waarop we stemmen
- Protoplasma is al het levende materiaal waar?
- Wordt mitochondria functioneert om eiwitten te produceren?
- Hoe wordt polyploïdie gebruikt op het gebied van landbouw?
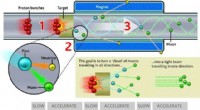
- Doorbraak gemaakt naar krachtigere deeltjesversnellers
- Natuurkundigen openen de deur naar de eerste directe meting van Berry-kromming in vaste materie
- Hoe maak je een beter beeld van atoomwolken? Spiegels—veel spiegels

- Onzichtbare tags:natuurkundigen schrijven, lezen en wissen met licht

- Topologie werpt nieuw licht op synchronisatie in netwerken van hogere orde

 Een precieze chemische vingerafdruk van de Amazone
Een precieze chemische vingerafdruk van de Amazone Is de zon de heetste plek in het universum?
Is de zon de heetste plek in het universum?  Wat is het geschatte percentage elektrische energie omgezet in licht in een gloeilamp?
Wat is het geschatte percentage elektrische energie omgezet in licht in een gloeilamp?  Wat zijn de uitgangsmaterialen voor een ster?
Wat zijn de uitgangsmaterialen voor een ster?  Wordt de zwaartekracht op raket minder naarmate deze stijgt?
Wordt de zwaartekracht op raket minder naarmate deze stijgt?  Is YouTube een motor voor sociale bewegingen als Occupy Wall Street?
Is YouTube een motor voor sociale bewegingen als Occupy Wall Street?  Hoe ondersteunt DNA -afdalingstheorie met modificatie?
Hoe ondersteunt DNA -afdalingstheorie met modificatie?  Hoe lockdown-afspeellijsten werden gebruikt om emoties te uiten tijdens de pandemie
Hoe lockdown-afspeellijsten werden gebruikt om emoties te uiten tijdens de pandemie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

