
Wetenschap
Wat is de gemiddelde snelheid van atomen?
* Temperatuur: Hoe heter het atoom, hoe sneller het beweegt.
* Atoomtype: Verschillende atomen hebben verschillende massa's en zwaardere atomen bewegen langzamer bij dezelfde temperatuur.
* Staat van materie: Atomen in een vaste stof zijn minder mobiel dan atomen in een gas.
Hier is een uitsplitsing:
* in een gas: Atomen bewegen vrij vrij en botsen vaak. Hun gemiddelde snelheid kan worden berekend met behulp van de root-mean-square (RMS) snelheid:
`` `
v_rms =√ (3kt/m)
`` `
Waar:
* K is de constante van Boltzmann (1.38 x 10^-23 J/K)
* T is de temperatuur in Kelvin
* M is de massa van het atoom
* in een vloeistof: Atomen bewegen minder vrij dan in een gas, maar hebben nog steeds aanzienlijke kinetische energie. Hun gemiddelde snelheid is lager dan in een gas, maar deze wordt nog steeds beïnvloed door temperatuur.
* in een vaste stof: Atomen zijn strak aan elkaar gebonden en trillen rond vaste posities. Hoewel ze een bepaalde hoeveelheid vibratie -energie hebben, is hun gemiddelde snelheid veel lager dan in vloeistoffen of gassen.
Voorbeelden:
* Bij kamertemperatuur (298 K) is de RMS -snelheid van een stikstofmolecuul (N2) ongeveer 515 m/s.
* De RMS -snelheid van een heliumatoom (HE) bij dezelfde temperatuur is ongeveer 1360 m/s, waaruit blijkt dat lichtere atomen sneller bewegen.
Samenvattend: De gemiddelde snelheid van atomen hangt af van het temperatuur, het atoomtype en de toestand van materie. Het concept van "gemiddelde snelheid" wordt vaak weergegeven door de wortelgemiddelde snelheid voor atomen in een gas.
 Wat is de formule van koper 1 sulfaat?
Wat is de formule van koper 1 sulfaat?  Nieuwe biomaterialen kunnen worden verfijnd voor medische toepassingen
Nieuwe biomaterialen kunnen worden verfijnd voor medische toepassingen Nieuwe topologische materialen kunnen meerdere elektrische eigenschappen hebben
Nieuwe topologische materialen kunnen meerdere elektrische eigenschappen hebben Atoombeeld van de verbazingwekkende moleculaire machines van de natuur aan het werk
Atoombeeld van de verbazingwekkende moleculaire machines van de natuur aan het werk Hoeveel ATP en NADPH zijn vereist om één CO2 -molecuul te repareren?
Hoeveel ATP en NADPH zijn vereist om één CO2 -molecuul te repareren?
 Fietssucces kan de sleutel zijn om vijfde van landbouwgrond vrij te maken
Fietssucces kan de sleutel zijn om vijfde van landbouwgrond vrij te maken Waarom is zolaogie belangrijk voor de islam?
Waarom is zolaogie belangrijk voor de islam?  Twee niet-levende delen van een ecosysteem
Twee niet-levende delen van een ecosysteem  Microben kunnen de poortwachters zijn van de grootste broeikasgasreserves van de planeet
Microben kunnen de poortwachters zijn van de grootste broeikasgasreserves van de planeet Expert zegt dat bosbranden aan de westkust waarschijnlijk jarenlang rokerige wijn zullen betekenen
Expert zegt dat bosbranden aan de westkust waarschijnlijk jarenlang rokerige wijn zullen betekenen
Hoofdlijnen
- Darmmicrobioom helpt beren met zeer verschillende diëten om dezelfde grootte te bereiken
- Verschillen tussen Protista & Monera
- Wat een groep bizar uitziende vleermuizen ons kan vertellen over de evolutie van zoogdieren
- Team ontdekt hoe microsporidiaanse parasieten sprinkhanenzwermgedrag voorkomen
- Waarom hebben wetenschappers een gemeenschappelijk meetsysteem nodig?
- Hoe Punnett Squares
- Welk ademhalingsmembraan bestaat voornamelijk uit wat?
- Wat zijn genetisch gemodificeerde organismen (GGO's)? Zijn ze veilig?
- Welk proces werken mRNA en TRNA samen om te voltooien?
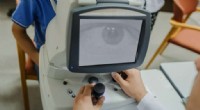
- Op laser gebaseerde technologie helpt artsen het volledige oog in 3D af te beelden
- Tweedimensionaal hybride metaalhalogenide-apparaat maakt controle van terahertz-emissies mogelijk

- Resistieve plaatkamers als neutronendetectoren

- Dunne films kunnen de vorticiteit in de oceaan verbeteren
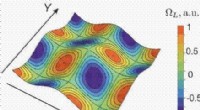
- Nieuwe laser voldoet aan hoge eisen voor het aansturen van geavanceerde attoseconde lichtbronnen

 Heeft Apollo 10 ooit op de maan geland?
Heeft Apollo 10 ooit op de maan geland?  Kun je me een exanple geven van slogan over chemie?
Kun je me een exanple geven van slogan over chemie?  Nieuw onderzoek om veilige locaties voor opslag van nucleair afval te helpen identificeren
Nieuw onderzoek om veilige locaties voor opslag van nucleair afval te helpen identificeren Hersenen-geïnspireerd algoritme helpt AI-systemen multitasken en onthouden
Hersenen-geïnspireerd algoritme helpt AI-systemen multitasken en onthouden Hoeveel kracht is er nodig om een vliegtuig van 9760 kg te versnellen met een snelheid van 3,9 ms2?
Hoeveel kracht is er nodig om een vliegtuig van 9760 kg te versnellen met een snelheid van 3,9 ms2?  Welk effect heeft wrijving wanneer u probeert een object in rust te verplaatsen?
Welk effect heeft wrijving wanneer u probeert een object in rust te verplaatsen?  Interstellaire ruimtevlucht:is het mogelijk?
Interstellaire ruimtevlucht:is het mogelijk?  Wat is Jupiter er van binnen en buiten?
Wat is Jupiter er van binnen en buiten?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

