
Wetenschap
In welk regel of principe stelt dat geen twee elektronen in hetzelfde orbitaal kunnen draaien?
De regel of principe waarnaar u op zoek bent, is het Pauli Exclusion Principle .
Het stelt dat geen twee elektronen in een atoom dezelfde set van vier kwantumnummers kunnen hebben. Een van deze kwantumnummers beschrijft de spin van het elektron, dat kan zijn spin-up (+1/2) of spin-down (-1/2).
Daarom, als twee elektronen hetzelfde orbitaal bezetten (dezelfde n, l en m l kwantumnummers), ze moeten tegengestelde spins hebben om het Pauli -uitsluitingsprincipe te vervullen.
 In de roos:de Golf bereidt zich voor op Laura om als orkaan te slaan
In de roos:de Golf bereidt zich voor op Laura om als orkaan te slaan Het smelten van de Groenlandse ijskap kan de subtropen afkoelen, klimaat veranderen
Het smelten van de Groenlandse ijskap kan de subtropen afkoelen, klimaat veranderen Twee doden als supercycloon de Fiji-dorpen egaliseert
Twee doden als supercycloon de Fiji-dorpen egaliseert Experts zeggen stedelijke wildgroei, klimaatverandering wandelen natuurbrandrisico
Experts zeggen stedelijke wildgroei, klimaatverandering wandelen natuurbrandrisico Jongen of meisje? Maki-geuren hebben het antwoord
Jongen of meisje? Maki-geuren hebben het antwoord
Hoofdlijnen
- Hoe vindt een mug menselijk lichaam?
- Zijn MHC 1 -eiwitten gevonden in de meeste cellen van het lichaam?
- Hoe kan één cel baby worden met al zijn organen?
- Hoe worden braamzaden verspreid door dieren?
- Op welk deel van de hersenen zijn evenwichtssignalen verzonden?
- Hoe gebruiken wetenschappers spectrografen?
- Hebben zowel dier- als plantencellen semipermeabele membranen?
- Wat is een prehistorische toolkit en hoe zou deze de menselijke geschiedenis kunnen herschrijven?
- Hoe biomimicry werkt
- Internationaal team ontwikkelt nieuwe methode om oorsprong van sterrenstof in meteorieten te bepalen

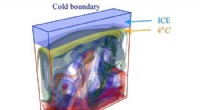
- Hoe de groei van ijs afhangt van de vloeistofdynamica eronder
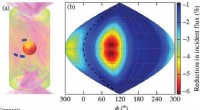
- Inertiële opsluiting fusie-implosies hebben significante 3D-asymmetrieën
- Team produceert unieke simulatie van magnetische herverbinding

- Hoe een nieuwe kwantumbenadering snellere algoritmen kan ontwikkelen om complexe netwerken af te leiden

 Wat zijn enkele chemische reacties waterstof?
Wat zijn enkele chemische reacties waterstof?  Wanneer een sinaasappel van een tafel rolt, wordt de potentiële energie omgezet in wat?
Wanneer een sinaasappel van een tafel rolt, wordt de potentiële energie omgezet in wat?  Onderzoek toont aan dat standaardkeuzes ertoe doen, vooral voor armere, lager opgeleide personen
Onderzoek toont aan dat standaardkeuzes ertoe doen, vooral voor armere, lager opgeleide personen Ontdekking over hoe oppervlaktegradiënten het druppelgedrag beïnvloeden, kan nieuwe oppervlakken mogelijk maken met anti-ijsvormingsmogelijkheden
Ontdekking over hoe oppervlaktegradiënten het druppelgedrag beïnvloeden, kan nieuwe oppervlakken mogelijk maken met anti-ijsvormingsmogelijkheden  Virtuele influencers zijn er, maar zou Meta echt de ethische grondregels moeten bepalen?
Virtuele influencers zijn er, maar zou Meta echt de ethische grondregels moeten bepalen? Welk koninkrijk heeft microscopische organismen met kenmerken van plantencellen?
Welk koninkrijk heeft microscopische organismen met kenmerken van plantencellen?  Welk type landvorm wordt gevormd door een mantelpluim?
Welk type landvorm wordt gevormd door een mantelpluim?  Wat zijn de effecten van warmte -energie in vaste stoffen?
Wat zijn de effecten van warmte -energie in vaste stoffen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

