
Wetenschap
Is een binding tussen waterstof en stikstofbinding?
Dit is waarom:
* elektronegativiteit: Stikstof is elektronegatiefer dan waterstof, wat betekent dat het een sterkere trek heeft op gedeelde elektronen.
* delen van elektronen: Zowel waterstof als stikstof moeten elektronen krijgen om een stabiele elektronenconfiguratie te bereiken. Ze bereiken dit door elektronen te delen en een covalente binding te vormen.
Voorbeelden:
* ammoniak (NH3): Dit molecuul bevat drie waterstofatomen die covalent worden gebonden aan een stikstofatoom.
* amides (r-conh2): Deze organische verbindingen bevatten een stikstofatoom dat is gebonden aan een koolstofatoom en twee waterstofatomen.
Laat het me weten als je nog meer vragen hebt!
 Hoe verschillen atomen en elementen?
Hoe verschillen atomen en elementen?  Zal 1 mol suiker hetzelfde effect hebben als tafelzout bij het verlagen van het vriespuntwater?
Zal 1 mol suiker hetzelfde effect hebben als tafelzout bij het verlagen van het vriespuntwater?  Welke van de volgende uitspraken beschrijft het meest nauwkeurig het verschil tussen ionische binding en covalente binding?
Welke van de volgende uitspraken beschrijft het meest nauwkeurig het verschil tussen ionische binding en covalente binding?  Hoeveel mol waterstof in 1G?
Hoeveel mol waterstof in 1G?  Groene waterstof:roest als fotoanode en zijn grenzen
Groene waterstof:roest als fotoanode en zijn grenzen
 Kleine hydro-elektrische dammen nemen wereldwijd toe met weinig onderzoek, voorschriften
Kleine hydro-elektrische dammen nemen wereldwijd toe met weinig onderzoek, voorschriften Hoe high-capacity papier werkt
Hoe high-capacity papier werkt  Hoe verplaatsen rondwormen?
Hoe verplaatsen rondwormen?  Waarom komt het sneeuwpakket van Colorado niet in de Colorado-rivier terecht? Uit onderzoek blijkt dat dit mogelijk te maken heeft met een gebrek aan regenval in de lente
Waarom komt het sneeuwpakket van Colorado niet in de Colorado-rivier terecht? Uit onderzoek blijkt dat dit mogelijk te maken heeft met een gebrek aan regenval in de lente  Mushroom Hunting in Colorado
Mushroom Hunting in Colorado
Hoofdlijnen
- Hoe een organisme eruit ziet, ongeacht de allelen van het type wordt gerefereerd als wat?
- Waarom plaatsten wetenschappers bacteriën in hun eigen koninkrijk de Moneta?
- Hoe doodt streptomycine bacteriecellen?
- Hoe schimmels een dodelijke onderwateraanval uitvoeren op Aedes-muggenlarven
- Planten kunnen de intensiteit van zoutstress meten
- De eigenschappen van steenzout
- Wat doen mutaties voor allelen?
- Hoe mangrovebossen geweldig zijn voor de planeet
- Onderzoek laat zien hoe een enkel enzym de productie van sojaolie kan stimuleren
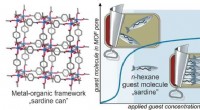
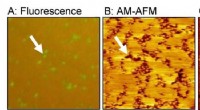
- Gastuitlijning en defectvorming tijdens porievulling in metaal-organische raamwerkfilms
- Octopus-geïnspireerde zelfklevende patch werkt onder water

- Een nieuw materiaal voor transparante en flexibele displays

- Assemblage van fluctuerende moleculen in kunstmatig celmembraan
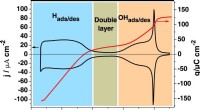
- Nieuw begrip van de belangrijkste brandstofcelkatalysator
 Wat is de diameter van Mars in wetenschappelijke notatie?
Wat is de diameter van Mars in wetenschappelijke notatie?  Wat zijn de rollen van organismen?
Wat zijn de rollen van organismen?  Google volgt je bewegingen, of je het nu leuk vindt of niet
Google volgt je bewegingen, of je het nu leuk vindt of niet Huawei 5G-problemen om de bandbreedte van Noordse concurrenten te testen
Huawei 5G-problemen om de bandbreedte van Noordse concurrenten te testen Wat een organisme ziet eruit als gevolg van zijn genen?
Wat een organisme ziet eruit als gevolg van zijn genen?  Nieuwe tools om risico's in gedeelde, augmented-reality-omgevingen
Nieuwe tools om risico's in gedeelde, augmented-reality-omgevingen Technologie vormt de reactie van verzekeringsmaatschappijen op bosbranden
Technologie vormt de reactie van verzekeringsmaatschappijen op bosbranden Wat is een derecho? Een atmosferische wetenschapper legt deze zeldzame maar gevaarlijke stormsystemen uit
Wat is een derecho? Een atmosferische wetenschapper legt deze zeldzame maar gevaarlijke stormsystemen uit
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

