
Wetenschap
Hoe verschillen de bewegingen van deeltjes tussen de toestand?
solide:
* deeltjesopstelling: Deeltjes in een vaste stof zijn strak in elkaar verpakt in een regelmatig, herhaaldelijk patroon (een kristalrooster).
* beweging: Deeltjes trillen in vaste posities, met slechts beperkte beweging. Ze hebben lage kinetische energie.
* Vorm en volume: Vaste stoffen hebben een duidelijke vorm en volume omdat de deeltjes in hun posities zijn gefixeerd.
vloeistof:
* deeltjesopstelling: Deeltjes in een vloeistof zijn dichter bij elkaar dan in een gas, maar niet zo strak gepakt of geordend als in een vaste stof. Ze kunnen zich om elkaar heen bewegen.
* beweging: Deeltjes in een vloeistof bewegen meer vrij dan in een vaste stof, maar ze zijn nog steeds relatief dicht bij elkaar. Ze hebben hogere kinetische energie dan vaste stoffen.
* Vorm en volume: Vloeistoffen hebben een duidelijk volume maar nemen de vorm van hun container omdat de deeltjes kunnen bewegen en stromen.
gas:
* deeltjesopstelling: Deeltjes in een gas liggen ver uit elkaar en bewegen willekeurig in alle richtingen. Er is geen vaste regeling.
* beweging: Deeltjes in een gas hebben de hoogste kinetische energie. Ze bewegen zeer snel en botsen vaak tegen elkaar en de wanden van hun container.
* Vorm en volume: Gassen hebben geen duidelijke vorm of volume, die de vorm en het volume van hun container nemen omdat de deeltjes vrij bewegen.
plasma:
* deeltjesopstelling: Vergelijkbaar met een gas, maar met een groot aantal ionen en vrije elektronen.
* beweging: Deeltjes in een plasma bewegen zeer snel en botsen regelmatig. Ze hebben nog hogere kinetische energie dan gassen, waarbij sommige deeltjes zelfs andere deeltjes ioniseren.
* Vorm en volume: Net als een gas, heeft plasma geen duidelijke vorm of volume.
Samenvattend:
* vaste stoffen: Deeltjes trillen in vaste posities met lage kinetische energie.
* vloeistoffen: Deeltjes bewegen om elkaar heen met hogere kinetische energie dan vaste stoffen.
* gassen: Deeltjes bewegen willekeurig en vrijelijk met zeer hoge kinetische energie.
* plasma: Vergelijkbaar met een gas, maar met geïoniseerde deeltjes en zelfs hogere kinetische energie.
De verschillen in deeltjesbeweging zijn de reden waarom de toestanden van materie verschillende eigenschappen hebben.
 Hoe zijn alkalische metalen in vergelijking met alkali -metalen?
Hoe zijn alkalische metalen in vergelijking met alkali -metalen?  Welke verbrandingswijzen vereist dat vloeibare of vaste brandstoffen worden omgezet. De gasfase verdampt?
Welke verbrandingswijzen vereist dat vloeibare of vaste brandstoffen worden omgezet. De gasfase verdampt?  Hoe zorgt de structuur van chloroplast in staat om een concentratiegradiëntprotonen op te bouwen?
Hoe zorgt de structuur van chloroplast in staat om een concentratiegradiëntprotonen op te bouwen?  Is ammoniummolybdate een groene chemische stof?
Is ammoniummolybdate een groene chemische stof?  Wat bepaalt de verhouding van ionen in een ionische verbinding?
Wat bepaalt de verhouding van ionen in een ionische verbinding?
Hoofdlijnen
- Klimaatverandering is de meest prominente bedreiging voor bestuivers, zo blijkt uit onderzoek
- Natuurbeschermers moeten het Hollywood-effect benutten om dieren in het wild te helpen
- Welke ondersteuning voor evolutie wordt geleverd door vergelijkende embryologie?
- Hoe vissen de zuurstofoorlog wonnen
- Waar zijn celmembraanporiën van gemaakt?
- Hoe komt stikstof uit organismen terug in de atmosfeer?
- Wat zijn vier soorten materie?
- Deze pijnbomen leunen bijna altijd naar de evenaar
- Waarom weet Wegener van uiteenlopende plaatgrenzen?
- Een nieuwe strategie om een high-fidelity mixed-species verstrengelingspoort te implementeren

- Natuurkundigen observeren de opkomst van collectief gedrag

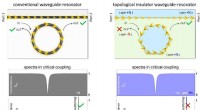
- Prestatiedoorbraak door topologische isolator in een golfgeleider-resonatorsysteem
- Om een machine ter grootte van een atoom te maken, je hebt een kwantummechanica nodig

- 2021:een jaar waarin natuurkundigen zich afvroegen:wat ligt er achter het standaardmodel?

 Wat zijn de 5 structurele zones van de aarde?
Wat zijn de 5 structurele zones van de aarde?  Wat zijn de vier stadia van een terrestrische planeet?
Wat zijn de vier stadia van een terrestrische planeet?  Hoe kunnen we de omgeving actief herstellen?
Hoe kunnen we de omgeving actief herstellen?  Hoe RPM te converteren naar Radians
Hoe RPM te converteren naar Radians Hoe beheerst de industrie de risico's van thermische weggelopen reacties?
Hoe beheerst de industrie de risico's van thermische weggelopen reacties?  Waarom moeten gelogen om een steen voor te bereiden om onder de microscoop te bekijken heel dun snijden?
Waarom moeten gelogen om een steen voor te bereiden om onder de microscoop te bekijken heel dun snijden?  Waar ligt de laag onder de lithosfeer?
Waar ligt de laag onder de lithosfeer?  Nieuwe studie suggereert dat we waarschijnlijk de toekomstige impact van PFAS op het milieu onderschatten
Nieuwe studie suggereert dat we waarschijnlijk de toekomstige impact van PFAS op het milieu onderschatten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

