
Wetenschap
Lost een vaste stof sneller op wanneer deze wordt gemalen omdat slijpen het oppervlak vermindert?
Dit is waarom:
* oppervlakte: Het oppervlak van een vaste stof is het totale oppervlak van de blootgestelde oppervlakken. Denk aan een suikerkubus versus kristalsuiker. De kristalsuiker heeft een veel groter oppervlak omdat deze in kleinere deeltjes is gebroken.
* ontbinding: Oplost omvat de interactie tussen de moleculen van de vaste stof en het oplosmiddel (meestal een vloeistof). Om deze interactie te laten optreden, moeten de oplosmiddelmoleculen in contact komen met het oppervlak van de vaste stof.
* Verhoogd oppervlak, verhoogd contact: Een groter oppervlak betekent meer contactpunten voor het oplosmiddel om te communiceren met de vaste stof, wat leidt tot snellere oplossing.
Zie het zo:stel je voor dat je een ijsblok hebt. Het gaat langzaam smelten omdat er slechts zes partijen aan de warme lucht zijn blootgesteld. Als u het ijs in kleinere stukken breekt, verhoogt u het blootgestelde oppervlak en het zal veel sneller smelten. Hetzelfde principe is van toepassing op het oplossen van vaste stoffen.
 Polystyreenafval is overal, en het is niet biologisch afbreekbaar. Wetenschappers hebben zojuist een manier gevonden om het af te breken.
Polystyreenafval is overal, en het is niet biologisch afbreekbaar. Wetenschappers hebben zojuist een manier gevonden om het af te breken. Nieuw goedkoop materiaal voor verlichting en diagnostiek produceert wit licht dat zonlicht imiteert
Nieuw goedkoop materiaal voor verlichting en diagnostiek produceert wit licht dat zonlicht imiteert Berekenen van alkaliteit als concentratie van CaCO3
Berekenen van alkaliteit als concentratie van CaCO3  Overzicht van recente ontwikkelingen in de elektrolyse van zout water
Overzicht van recente ontwikkelingen in de elektrolyse van zout water Wat is een oplossingstypen van materie?
Wat is een oplossingstypen van materie?
 Europese leiders:klimaatovereenkomst kan niet opnieuw worden onderhandeld
Europese leiders:klimaatovereenkomst kan niet opnieuw worden onderhandeld Hoe bosbranden en het weer de Portugese volksgezondheid beïnvloeden
Hoe bosbranden en het weer de Portugese volksgezondheid beïnvloeden  Nieuw onderzoek laat zien hoe hommels vogelnesten stelen
Nieuw onderzoek laat zien hoe hommels vogelnesten stelen  Wat zijn 4 voorbeelden van levende wezens?
Wat zijn 4 voorbeelden van levende wezens?  Kwikvervuiling van de afgelopen decennia is mogelijk opnieuw vrijgekomen door bosbranden in Tasmanië
Kwikvervuiling van de afgelopen decennia is mogelijk opnieuw vrijgekomen door bosbranden in Tasmanië
Hoofdlijnen
- Wat is bioclastische textuur?
- Welke van de volgende beschrijft de functies van de longen?
- Wanneer is een worm geen worm? het zijn kwallen...
- Kenmerken van nucleïnezuren
- Onderzoek naar factoren die ten grondslag kunnen liggen aan de manier waarop huiskatten in groepen kunnen leven
- Wat is het proces waarbij stoffen de cellen binnenkomen en verlaten en binnen de cellen worden verdeeld?
- Noem de modus van voeding in ronde worm en Plasmodium?
- Waar kan fosfor in een menselijke cel worden gevonden?
- Bioreactoren op een chip vernieuwen beloften voor algenbiobrandstoffen
- Led-materiaal schijnt onder spanning

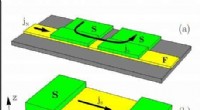
- Bewegende domeinwanden veroorzaken verliezen in supergeleider/ferromagneet hybride systemen
- Waterige verandering bij lage temperatuur van zirkoon van Mars tijdens de late Amazone-periode

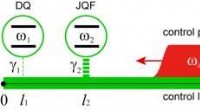
- Een filter voor schonere qubits
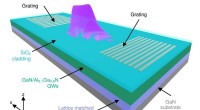
- Het bereiken van UV-niet-lineariteit met een halfgeleidergolfgeleider met brede bandgap
 Hebben ionische verbindingen of covalente verbindingen sterkere intermoleculaire krachten?
Hebben ionische verbindingen of covalente verbindingen sterkere intermoleculaire krachten?  Gevolgen van de zomerdroogte van 2018
Gevolgen van de zomerdroogte van 2018 De kracht van randomisatie:magnetische skyrmionen voor nieuwe computertechnologie
De kracht van randomisatie:magnetische skyrmionen voor nieuwe computertechnologie Verschillen tussen militaire, burgerleven bijdragen aan veteranen in het Amerikaanse strafrechtsysteem
Verschillen tussen militaire, burgerleven bijdragen aan veteranen in het Amerikaanse strafrechtsysteem Diep ademhalen? Wetenschappers meten ongewoon hoge zuurstofopname in de Labradorzee
Diep ademhalen? Wetenschappers meten ongewoon hoge zuurstofopname in de Labradorzee Hoeveel schillen hebben 20 elektronen nodig?
Hoeveel schillen hebben 20 elektronen nodig?  Hoe COVID het arbeidsrecht verandert
Hoe COVID het arbeidsrecht verandert Wat is de beschrijving voor Krakatoa -vulkaan?
Wat is de beschrijving voor Krakatoa -vulkaan?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

