
Wetenschap
Wat is het massale nummer van een element op periodieke tabel?
Hier is een uitsplitsing:
* protonen: Positief geladen deeltjes gevonden in de kern. Het aantal protonen bepaalt het atoomnummer van het element.
* neutronen: Neutraal geladen deeltjes ook gevonden in de kern.
* elektronen: Negatief geladen deeltjes die de kern draaien.
Sleutelpunten:
* Massienummer is een benadering: Het is geen exacte meting van de atoommassa omdat het geen rekening houdt met de massa elektronen of de bindende energie in de kern.
* isotopen: Elementen kunnen verschillende aantallen neutronen hebben, waardoor isotopen worden gecreëerd. Isotopen van hetzelfde element hebben hetzelfde aantal protonen maar verschillende massagummers.
Voorbeeld:
Carbon -12 heeft een massaal aantal van 12. Dit betekent dat het 6 protonen en 6 neutronen heeft (12 - 6 =6).
 Doorbraak in synthese van scheikundigen bevordert een krachtig middel tegen kanker
Doorbraak in synthese van scheikundigen bevordert een krachtig middel tegen kanker Waar wordt een chloorwaterfilter voor gebruikt?
Waar wordt een chloorwaterfilter voor gebruikt?  Wat is de chemische bahpo4?
Wat is de chemische bahpo4?  Een atoom verliest een elektron aan een ander, is dit een voorbeeld van fysische of chemische verandering?
Een atoom verliest een elektron aan een ander, is dit een voorbeeld van fysische of chemische verandering?  Twee eenvoudige bouwstenen produceren complex 3D-materiaal
Twee eenvoudige bouwstenen produceren complex 3D-materiaal
 Niet te rechtvaardigen:nieuw rapport laat zien hoe de gasexpansie van de natie Australiërs in gevaar brengt
Niet te rechtvaardigen:nieuw rapport laat zien hoe de gasexpansie van de natie Australiërs in gevaar brengt Afgelegen Kaap met 's werelds schoonste lucht biedt smogverademing
Afgelegen Kaap met 's werelds schoonste lucht biedt smogverademing Hoe de waterradfabriek knapt
Hoe de waterradfabriek knapt  Bent u een 'drukke ontdekkingsreiziger' of 'quality time-zoeker?' Onderzoek verdeelt reizigers op basis van gebruik en impact op het milieu
Bent u een 'drukke ontdekkingsreiziger' of 'quality time-zoeker?' Onderzoek verdeelt reizigers op basis van gebruik en impact op het milieu  Positieve effecten van mensen op het ecosysteem
Positieve effecten van mensen op het ecosysteem
Hoofdlijnen
- Welke soorten cellen en organismen ondergaan mitose en meiose?
- RNA-dynamiek gedeconstrueerd:Techniek biedt gedetailleerd inzicht in hoe niveaus veranderen
- Onderzoekers ontdekken nieuw signaal voor het opwekken van menselijke immuunrespons
- Trofische coherentie verklaart waarom netwerken weinig feedbacklussen en hoge stabiliteit hebben
- Waarom hebben cellen voedsel nodig?
- Welke mutatie beïnvloedt een nakomelingen?
- Vissen gebruiken doofheidsgen om waterbeweging waar te nemen
- Wat is ureum?
- Verplaatste haviken gedijen goed in Hispaniola
- Nieuwe LHCb-analyse levert nog steeds intrigerende resultaten op

- Nieuw begrip van metastabiliteit maakt de weg vrij voor materialen van de volgende generatie

- Nieuwe apparaten om röntgenstralen te controleren zijn goedkoper, sneller te maken

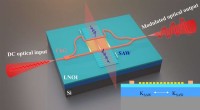
- Zeer efficiënte akoesto-optische modulatie met behulp van niet-gesuspendeerde dunne-film lithiumniobaat-chalcogenide hybride golfgeleiders
- Supergeleiding en ferromagnetisme vechten tegen een gelijke match

 Flexibele thermo-elektrische generatormodule:een wondermiddel om problemen met afvalenergie op te lossen
Flexibele thermo-elektrische generatormodule:een wondermiddel om problemen met afvalenergie op te lossen Het marktvoordeel van een vrouwelijke merknaam
Het marktvoordeel van een vrouwelijke merknaam Wiskundig raamwerk verandert elk vel materiaal in elke vorm met behulp van kirigami-sneden
Wiskundig raamwerk verandert elk vel materiaal in elke vorm met behulp van kirigami-sneden Hoe ultrasoon lassen werkt
Hoe ultrasoon lassen werkt  Recyclingonderzoek vindt een nieuw proces om glasvezelversterkt plastic om te zetten in siliciumcarbide
Recyclingonderzoek vindt een nieuw proces om glasvezelversterkt plastic om te zetten in siliciumcarbide  Wat is de maximale snelheid van een orkaan?
Wat is de maximale snelheid van een orkaan?  Volwassen analyse van sociale media
Volwassen analyse van sociale media Is er een magneet in een elektromagneet?
Is er een magneet in een elektromagneet?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

