
Wetenschap
Wat is het periodieke patroon van de atoomstraal?
Gedurende een periode :Naarmate het atoomnummer in de loop van de tijd toeneemt, worden er meer protonen aan de kern toegevoegd, waardoor de positieve lading van de kern en de aantrekkingskracht die op de elektronen wordt uitgeoefend toenemen. Dit zorgt ervoor dat de elektronen dichter bij de kern worden getrokken, waardoor de atoomstraal kleiner wordt.
Een groep lager :Naarmate je een groep afdaalt, worden er nieuwe elektronenschillen toegevoegd, waardoor de afstand tussen de buitenste elektronen en de kern groter wordt. De extra elektronenschillen fungeren als barrières die de buitenste elektronen beschermen tegen de positieve lading van de kern, waardoor de aantrekkingskracht wordt verminderd en de atoomstraal groter wordt.
Uitzonderingen:Er zijn enkele uitzonderingen op dit algemene patroon, voornamelijk vanwege het onregelmatige afschermende effect van de binnenste elektronenschillen. Zo zijn de atoomstralen van de overgangsmetalen in de vierde periode (Y, Zr, Nb, etc.) iets groter dan verwacht, terwijl de atoomstralen van de elementen uit groep 13 (B, Al, Ga, etc.) dat wel zijn. iets kleiner dan verwacht. Deze uitzonderingen kunnen worden toegeschreven aan specifieke elektronenconfiguraties en de interacties tussen elektronen binnen de atomen.
Samenvattend weerspiegelt het periodieke patroon van de atoomstraal de wisselwerking tussen het aantal protonen en elektronen in een atoom, evenals het afschermende effect van de binnenste elektronenschillen, wat leidt tot de waargenomen trends over perioden en neerwaartse groepen.
 Nieuw materiaal maakt koelapparaten energiezuiniger
Nieuw materiaal maakt koelapparaten energiezuiniger Wat is wolfraam staal?
Wat is wolfraam staal?
Staal, een legering van ijzer en koolstof, is er in veel verschillende soorten. Gemengd met andere metalen neemt het verschillende eigenschappen aan. Tungsten was een van de eerste metalen die werd gebruikt om staal te verbet
 Is de volgende vergelijking gebalanceerd CS2 plus 2Cl2 CCl4 S2Cl2?
Is de volgende vergelijking gebalanceerd CS2 plus 2Cl2 CCl4 S2Cl2?  Welk type verbinding kun je concluderen dat olie is?
Welk type verbinding kun je concluderen dat olie is?  Nieuw op metallo-enzymen gebaseerd systeem maakt selectieve targeting van kankercellen mogelijk
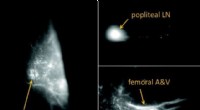
Nieuw op metallo-enzymen gebaseerd systeem maakt selectieve targeting van kankercellen mogelijk
 Verbergt de opwarming van de aarde zich onder water?
Verbergt de opwarming van de aarde zich onder water?  Afvalwaterslib omzetten in energie en minerale zouten
Afvalwaterslib omzetten in energie en minerale zouten Populair betekent niet invloedrijk onder Cambodjaanse boeren
Populair betekent niet invloedrijk onder Cambodjaanse boeren Beneden en vies:afvalwater van varkensboerderijen in Okinawa reinigen met microbiële brandstofcellen
Beneden en vies:afvalwater van varkensboerderijen in Okinawa reinigen met microbiële brandstofcellen Droogte zet aan tot extreme maatregelen om Wests wilde paarden te beschermen
Droogte zet aan tot extreme maatregelen om Wests wilde paarden te beschermen
Hoofdlijnen
- Wat zijn de structurele delen van de lange botten in het lichaam?
- Nieuw onderzoek laat zien hoe microscopisch kleine algen in de loop van de tijd uitzonderlijk voedzaam zijn geworden, waardoor de evolutie vooruit is gegaan
- Uit onderzoek blijkt dat eiwitten een sleutelrol spelen bij het helpen van cilium om signalen naar de rest van de cel over te brengen
- Onderzoekers tonen aan dat de besmetting met pesticiden verder gaat dan alleen de schil van de appel
- Wat is het belang van nucleïnezuren?
- De belangrijkste componenten van het skeletsysteem
- Hoe chromosomen van vorm veranderen tijdens celdifferentiatie
- Cytoplasma: definitie, structuur en functie (met diagram)
- Plant die 108 jaar geleden uit Vermont verdween, per ongeluk herontdekt, zeggen botanici
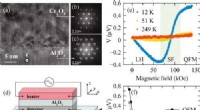
- Antferromagnetische hybriden bereiken belangrijke functionaliteit voor spintronische toepassingen
- Hoe onmogelijke kleuren werken

- Quantum-emitting antwoord zou in de oplossing kunnen liggen

- Een enkele fotonbron die je kunt maken met huishoudbleekmiddel
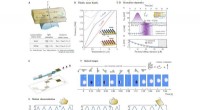
- Microschaal opto-thermo-mechanische activering in het droge lijmregime
 Schuldig plezier? Het zit allemaal in het geestesoog
Schuldig plezier? Het zit allemaal in het geestesoog  Zonnevlammen, bellen ringen, en inktkroonluchters
Zonnevlammen, bellen ringen, en inktkroonluchters Nanodeeltjes die worden gebruikt om de thermische eigenschappen van transformatorolie te verbeteren
Nanodeeltjes die worden gebruikt om de thermische eigenschappen van transformatorolie te verbeteren Wetenschappers tonen aan dat polaire polynya het zeeleven ondersteunde tijdens de laatste ijstijd
Wetenschappers tonen aan dat polaire polynya het zeeleven ondersteunde tijdens de laatste ijstijd Internationale academische Santa-enquête toont aan dat kinderen op achtjarige leeftijd niet meer in de kerstman geloven
Internationale academische Santa-enquête toont aan dat kinderen op achtjarige leeftijd niet meer in de kerstman geloven Nieuwe materialen ondergaan overgangen tussen vaste en vloeibare fasen bij kamertemperatuur
Nieuwe materialen ondergaan overgangen tussen vaste en vloeibare fasen bij kamertemperatuur Onze meren zitten vol met parasieten. Waarom dat goed is... en slecht
Onze meren zitten vol met parasieten. Waarom dat goed is... en slecht  Hersenschade bij vissen aangetast door plastic nanodeeltjes
Hersenschade bij vissen aangetast door plastic nanodeeltjes
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

