
Wetenschap
Hoe het massanummer van een element te bepalen
Door Chris Deziel | Bijgewerkt op 24 maart 2022
PollyW/iStock/GettyImages
TL;DR
Het massagetal van een element wordt direct onder het symbool in het periodiek systeem weergegeven. Het wordt uitgedrukt in atomaire massa-eenheden (amu), wat gelijk is aan gram per mol.
Atoomnummer versus massagetal
Elk element wordt gedefinieerd door zijn atoomnummer:het aantal positief geladen protonen in zijn kern. Waterstof heeft bijvoorbeeld één proton; zuurstof heeft er acht. Het periodiek systeem rangschikt de elementen door het atoomnummer te verhogen.
Het massagetal is echter het totale aantal protonen plus neutronen in de kern. Omdat neutronen ongeveer dezelfde massa hebben als protonen, maar geen lading hebben, moeten ze worden meegerekend bij de berekening van de massa van het element. De meest voorkomende isotoop van zuurstof heeft bijvoorbeeld acht protonen en acht neutronen, waardoor het een massagetal van 16 heeft.
Het massagetal in het periodiek systeem vinden
Kijk onder het symbool van een element in een gerenommeerd periodiek systeem:dit is het massagetal. Mogelijk ziet u een decimaalteken, wat feitelijk de relatieve atomaire massa is , het gewogen gemiddelde van alle in de natuur voorkomende isotopen. Omdat de meeste elementen meerdere isotopen hebben, is het gemiddelde zelden een geheel getal.
Het periodiek systeem vermeldt bijvoorbeeld de massa van waterstof als 1,008, die van koolstof als 12,011 en die van zuurstof als 15,99. Uranium (atoomnummer 92) heeft drie natuurlijke isotopen, waardoor het een relatieve massa heeft van 238.029. Bij routinematige berekeningen ronden wetenschappers af op het dichtstbijzijnde gehele getal.
Eenheden voor massa:de verenigde atomaire massa-eenheid (amu)
Sinds het begin van de 20e eeuw wordt de atomaire massa-eenheid (amu) gebruikt is de standaard geweest. Het wordt gedefinieerd als precies een twaalfde van de massa van een geïsoleerd koolstof-12-atoom. Bijgevolg is 1amu gelijk aan 1 gram per mol. Daarom weegt één mol waterstof 1 gram, één mol koolstof 12 gram en één mol uranium 238 gram.
Deze definities, aangenomen door IUPAC en gebruikt door NIST, zorgen voor consistentie in de wetenschappelijke literatuur en chemische berekeningen.
Referentie:IUPAC technisch rapport, 2021; NIST Scheikunde WebBook.
 Wat is reactie?
Wat is reactie?  Nieuwe waterdichtings- en aangroeiwerende materialen ontwikkeld
Nieuwe waterdichtings- en aangroeiwerende materialen ontwikkeld Hoe de dikke darm prioriteit geeft aan gasontgifting boven energieverbruik?
Hoe de dikke darm prioriteit geeft aan gasontgifting boven energieverbruik? Welke verschillen zijn er tussen verbindingen en mengsels?
Welke verschillen zijn er tussen verbindingen en mengsels?  Wat is de onoplosbare basis die kan worden gemengd met zwavelzuur om zinksulfaat te maken?
Wat is de onoplosbare basis die kan worden gemengd met zwavelzuur om zinksulfaat te maken?
 Verhelderend onderzoek onthult hoe planten reageren op licht
Verhelderend onderzoek onthult hoe planten reageren op licht  Volgens onderzoek heeft het Aralmeer Centraal-Azië aanzienlijk stoffiger gemaakt
Volgens onderzoek heeft het Aralmeer Centraal-Azië aanzienlijk stoffiger gemaakt  Waarom overleven sommige organismen extreme omgevingen?
Waarom overleven sommige organismen extreme omgevingen?  De huidige opwarming van Siberië is de krachtigste van de afgelopen 7.000 jaar
De huidige opwarming van Siberië is de krachtigste van de afgelopen 7.000 jaar Door de opwarming van de oceaan is de visserij in beweging, sommigen helpen maar meer pijn doen
Door de opwarming van de oceaan is de visserij in beweging, sommigen helpen maar meer pijn doen
Hoofdlijnen
- Hoe kan computertechnologie de toekomst van gensynthese voorspellen?
- Onderzoekers beschrijven voor het eerst hoe sommige bacteriën mannen doden:ze dringen de moeder binnen
- Wat zijn polymeren gemaakt van planten- en dierlijke producten?
- Welke functie werkt het lysosoom in een cel?
- De kleur van de evolutie:hoe één vis twee werd
- Welke vetzuren kan het lichaam niet produceren?
- De reproductieve hyfen die uit de schimmel groeit, wordt genoemd?
- Vocht gevulde zakjes omgeven door een membraan dat bijna identiek is aan de cel van menselijke cellen worden genoemd?
- Gefaciliteerde verspreiding uitgelegd:mechanismen, voorbeelden en belangrijkste beïnvloedende factoren
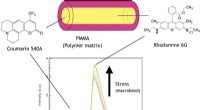
- Op polymeer gebaseerde optische vezel voor visualisatie van materiaalspanning
- Verbrandingsreacties begrijpen:hoe vuur brandstof omzet in energie

- Technische defecten in kristallijn materiaal verhogen de elektrische prestaties

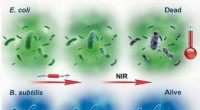
- Selectieve fotothermische therapie met supramoleculaire radicale anionen die in situ worden gegenereerd
- Molecuul uit de natuur zorgt voor volledig recyclebare polymeren

 Waar wordt Californië voor gebruikt?
Waar wordt Californië voor gebruikt?  Uit onderzoek blijkt waarom de zebra zijn strepen kreeg
Uit onderzoek blijkt waarom de zebra zijn strepen kreeg  Redoxreacties, verbranding, synthese, ontleding en dubbele verplaatsing:een uitgebreide gids
Redoxreacties, verbranding, synthese, ontleding en dubbele verplaatsing:een uitgebreide gids  Wat is een toename van de snelheid van snelheid?
Wat is een toename van de snelheid van snelheid?  Een glucoseoplossing bereiden
Een glucoseoplossing bereiden Waarom gaan leerlingen met een handicap naar 'speciale scholen' als onderzoek ons leert dat ze beter kunnen presteren in het reguliere systeem?
Waarom gaan leerlingen met een handicap naar 'speciale scholen' als onderzoek ons leert dat ze beter kunnen presteren in het reguliere systeem?  Wat is de snelheid van een auto van 2000 kg die 300 ms Monmentuem bezit?
Wat is de snelheid van een auto van 2000 kg die 300 ms Monmentuem bezit?  Twee objecten met dezelfde snelheid moeten in hetzelfde bewegen?
Twee objecten met dezelfde snelheid moeten in hetzelfde bewegen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

