
Wetenschap
Redoxreacties, verbranding, synthese, ontleding en dubbele verplaatsing:een uitgebreide gids
1. Redoxreacties:
* Definitie: Reacties waarbij elektronen worden overgedragen. De ene soort wordt geoxideerd (verliest elektronen), terwijl de andere wordt verkleind (elektronen wint).
* Voorbeeld: De verbranding van methaan (CH4) in zuurstof om koolstofdioxide (CO2) en water (H2O) te vormen.
2. Verbrandingsreacties:
* Definitie: Een snelle reactie tussen een stof en een oxidatiemiddel (meestal zuurstof), waarbij warmte en licht ontstaan.
* Voorbeeld: Het verbranden van hout.
3. Enkele vervangingsreacties:
* Definitie: Eén element vervangt een ander element in een verbinding.
* Voorbeeld: Zink (Zn) reageert met zoutzuur (HCl) en produceert zinkchloride (ZnCl2) en waterstofgas (H2).
4. Synthesereacties:
* Definitie: Twee of meer reactanten vormen samen één product.
* Voorbeeld: Natrium (Na) reageert met chloor (Cl2) om natriumchloride (NaCl) te vormen.
5. Ontbindingsreacties:
* Definitie: Eén enkele reactant valt uiteen in twee of meer producten.
* Voorbeeld: De ontleding van calciumcarbonaat (CaCO3) in calciumoxide (CaO) en kooldioxide (CO2).
6. Dubbele vervangingsreacties:
* Definitie: De positieve en negatieve ionen van twee reactanten wisselen van plaats.
* Voorbeeld: De reactie van zilvernitraat (AgNO3) en natriumchloride (NaCl) om zilverchloride (AgCl) en natriumnitraat (NaNO3) te vormen.
Het antwoord:
De twee reacties die voldoen aan de criteria om zowel redox- als verbrandingsreacties te zijn, zijn:
1. Verbrandingsreacties: Bij alle verbrandingsreacties is de overdracht van elektronen betrokken, waardoor het redoxreacties worden.
2. Enkele reacties op enkele vervanging: Bepaalde enkelvoudige vervangingsreacties kunnen worden beschouwd als redoxreacties en verbrandingsreacties als bij de reactie zuurstof betrokken is als de reactant die wordt vervangen. Bijvoorbeeld:
* 2Mg(s) + O2(g) → 2MgO(s) Hier reageert magnesium (Mg) met zuurstof (O2) om magnesiumoxide (MgO) te vormen, waarbij warmte en licht vrijkomen.
Belangrijke opmerking: Niet alle enkelvoudige vervangingsreacties zijn verbrandingsreacties. Bij verbranding gaat het specifiek om een snelle reactie met zuurstof.
 Hoe reproduceren de sprinkhanen?
Hoe reproduceren de sprinkhanen?  Hoe 'de ultieme zintuiglijke machines van de natuur' zicht en geur integreren
Hoe 'de ultieme zintuiglijke machines van de natuur' zicht en geur integreren  Manieren waarop gemeenschappen of de overheid water kunnen besparen
Manieren waarop gemeenschappen of de overheid water kunnen besparen Extreem weer veroorzaakte $ 65 miljard aan verliezen in de eerste helft van 2022
Extreem weer veroorzaakte $ 65 miljard aan verliezen in de eerste helft van 2022 Yellowstone verliest zijn sneeuw naarmate het klimaat warmer wordt, wijdverbreide problemen voorspellen voor water en dieren in het wild
Yellowstone verliest zijn sneeuw naarmate het klimaat warmer wordt, wijdverbreide problemen voorspellen voor water en dieren in het wild
Hoofdlijnen
- Welk belangrijk weefsel bekleedt de lichaamsholte en bedekt het buitenoppervlak?
- Wetenschappers maken een einde aan een vijftig jaar durend mysterie en onthullen hoe bacteriën zich kunnen verplaatsen
- Wat zijn enkele ziekten waar het lichaam zich niet tegen kan verdedigen?
- Wat vormt de Necleus of Antom?
- Genetische barcodes worden gebruikt om cruciale populaties in een ecosysteem van koraalriffen te kwantificeren
- Hoe is het milkweed belangrijk voor vlinders?
- Hebben zowel dier- als plantencellen semipermeabele membranen?
- Wat zijn de drie belangrijkste soorten wetenschap?
- Welke het dragen van de genetische code en het bepalen van een structuurfunctie zijn functies van DNA of RNA?
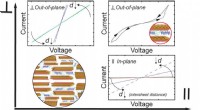
- Zelfmontage, biomimetische composieten hebben ongebruikelijke elektrische eigenschappen
- Supercomputers en het Archimedes-principe maken het mogelijk om de diffusie van nanobellen in nucleaire brandstoffen te berekenen

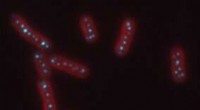
- Het membraan in membraanloze organellen begrijpen
- In batterijen turen:röntgenstralen onthullen lithium-ion-mysteries

- Lab-on-a-disc-technologie belooft te versnellen, DNA-analyse ter plaatse vereenvoudigen

 Botsing een oceanische bord botsen met een continentaal om de bergketen van Sierra Nevada te vormen?
Botsing een oceanische bord botsen met een continentaal om de bergketen van Sierra Nevada te vormen?  Voorbeelden van windbestoven bloemen
Voorbeelden van windbestoven bloemen Het principe achter het koffieringeffect gebruiken in kwantumdot-arrays
Het principe achter het koffieringeffect gebruiken in kwantumdot-arrays  Hoeveel kost een gallon gasgewicht?
Hoeveel kost een gallon gasgewicht?  Hoeveel mensen hebben Saturnus bezocht?
Hoeveel mensen hebben Saturnus bezocht?  Welke koolhydraat is een belangrijke energiebron voor de meeste organismen?
Welke koolhydraat is een belangrijke energiebron voor de meeste organismen?  Hoe mariene roofdieren voedselhotspots vinden in open oceaanwoestijnen
Hoe mariene roofdieren voedselhotspots vinden in open oceaanwoestijnen Wat is de uitgangskracht die wordt uitgeoefend door een beweegbare poelie als invoer 50N?
Wat is de uitgangskracht die wordt uitgeoefend door een beweegbare poelie als invoer 50N?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

