
Wetenschap
Factoren die de pH-niveaus in water, bodem en levende systemen beïnvloeden
Door Cassandra-stam | Bijgewerkt op 24 maart 2022
Het handhaven van het juiste pH-niveau – of het nu in zwembaden, aquariums, landbouwgronden of het menselijk lichaam is – vereist regelmatig testen en nauwkeurige aanpassingen. pH is de numerieke schaal die de balans van waterstofionen weergeeft, en meet in wezen hoe zuur of alkalisch een stof is. Als u de variabelen begrijpt die dit evenwicht verschuiven, kunt u uw omgeving stabiel en gezond houden.
Kooldioxide (CO₂)
Wanneer CO₂ oplost in water, reageert het onder vorming van koolzuur, waardoor de pH daalt. Bronnen van opgeloste CO₂ zijn onder meer de ademhaling van vissen en planten, de afbraak van organisch materiaal en bacteriële activiteit. In aquaria kan een hoge biologische belasting of onvoldoende ventilatie het CO₂-niveau snel verhogen, waardoor regelmatige CO₂-monitoring essentieel is.
Zuren en basen uit mineralen
Water dat over rotsen, grond, koraal of organisch afval stroomt, kan mineralen zoals calcium, magnesium en sulfiden uitlogen. Deze ionen combineren met opgelost CO₂ of andere bestanddelen om zwakke zuren of alkalische verbindingen te produceren, waardoor de pH in de loop van de tijd subtiel verandert. De specifieke impact hangt af van de lokale geologie en de samenstelling van het organische materiaal.
Natrium- en calciumhypochloriet
Zowel natriumhypochloriet (NaOCl) als calciumhypochloriet (Ca(OCl)₂) zijn veelgebruikte desinfectiemiddelen die worden gebruikt bij de behandeling van zwembaden en drinkwater. Ze geven hypochloorzuur af, dat de pH iets kan verlagen. Routinematig testen van de waterchemie helpt het optimale pH-bereik te behouden (doorgaans 7,2-7,8 voor zwembaden).
Chloorgas
Wanneer chloorgas (Cl₂) onbedoeld in de lucht vrijkomt, bijvoorbeeld door te veel vloeibaar bleekmiddel, reageert het met vocht en vormt zoutzuur, waardoor de pH-waarde van nabijgelegen water snel daalt. Een goede dosering en ventilatie zijn van cruciaal belang om deze plotselinge verschuiving te voorkomen.
In de lucht zwevende deeltjes
Stof, pollen en fijne industriële deeltjes kunnen oplossen in regenwater of afvoer van irrigatie, waardoor sporenzuren of basen worden geïntroduceerd. Hoewel elk deeltje een kleine hoeveelheid bijdraagt, kan het cumulatieve effect ervan de pH van de bodem of zoetwaterlichamen veranderen, vooral in stedelijke of agrarische omgevingen.
Luchtvervuiling
Industriële emissies en uitlaatgassen van voertuigen stoten stikstofoxiden (NOₓ) en zwaveldioxide (SO₂) uit. Wanneer deze gassen in contact komen met vocht uit de atmosfeer, vormen ze respectievelijk salpeterzuur en zwavelzuur. Zure regen is een goed gedocumenteerd fenomeen dat de pH van meren, beken en bodem verlaagt, wat gevolgen heeft voor ecosystemen over de hele wereld.
 De hogedruktransformatie van natrium kan ons iets vertellen over de binnenkant van sterren en planeten
De hogedruktransformatie van natrium kan ons iets vertellen over de binnenkant van sterren en planeten  IJzer(II) Carbide (FeC):formule, eigenschappen en uitleg
IJzer(II) Carbide (FeC):formule, eigenschappen en uitleg  Nanogestructureerde materialen op siloxaanbasis voor nieuwe kunststoffen en micro-elektronica
Nanogestructureerde materialen op siloxaanbasis voor nieuwe kunststoffen en micro-elektronica Hoe verander je koolmono -oxide in een nuttig gas?
Hoe verander je koolmono -oxide in een nuttig gas?  Malaria kaapt je genen om je lever binnen te dringen
Malaria kaapt je genen om je lever binnen te dringen
 Op patrouille met India's anti-plastic blauwe ploeg
Op patrouille met India's anti-plastic blauwe ploeg Wat zijn twee kenmerken van levende wezens?
Wat zijn twee kenmerken van levende wezens?  Tropische storm Humberto richt zich op door orkaan getroffen Bahama's
Tropische storm Humberto richt zich op door orkaan getroffen Bahama's IJzerrijke meteorieten tonen een record van kernkristallisatie in de oudste planetesimalen van systemen
IJzerrijke meteorieten tonen een record van kernkristallisatie in de oudste planetesimalen van systemen Wat is het verschil tussen witte en groene schimmels?
Wat is het verschil tussen witte en groene schimmels?
Hoofdlijnen
- In het ei leren Amerikaanse brulkikkers hoe ze kunnen voorkomen dat ze een lunch worden
- Nieuwe intermoleculaire oppervlaktekracht onthult actomyosine-aandrijfmechanisme
- Welke twee belangrijke verschillen scheiden prokaryotische cellen van eukaryotische cellen?
- De reis van jonge walvissen belicht de bedreigingen waarmee oceaandieren worden geconfronteerd
- Welke bloedcel heeft DNA?
- Welke cel wordt waargenomen als A de vorming van een contractiele ring vertoont net voorafgaand aan cytoplasmatische divisie?
- Welk orgaan waarin een embryo zich ontwikkelt?
- Vorm een hypothese over de massa en het volume van een mol spliterwten?
- Hoeveel bindingen bevatten de DNA -nucleotiden?
- Krimp beheersen:nauwkeurige berekening en preventietips

- Apparaatupdate maakt mobiel testen op virussen mogelijk, bacteriën en actieve toxines

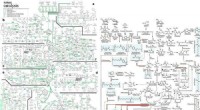
- Een uitgebreide metabole kaart voor de productie van biogebaseerde chemicaliën
- IJzerkatalysator kan belangrijke chemische reacties goedkoper en milieuvriendelijker maken
- Nano-roest:slim additief voor autonome temperatuurregeling

 Uit onderzoek blijkt hoeveel plastic afval er momenteel in de Middellandse Zee drijft
Uit onderzoek blijkt hoeveel plastic afval er momenteel in de Middellandse Zee drijft  Hoe verhoudt de voorwaartse kracht op een auto zich tot resistieve krachten wanneer deze constante snelheid handhaaft?
Hoe verhoudt de voorwaartse kracht op een auto zich tot resistieve krachten wanneer deze constante snelheid handhaaft?  Onderzoek toont aan dat een derde van de beschermde gebieden ter wereld is aangetast door menselijke activiteiten
Onderzoek toont aan dat een derde van de beschermde gebieden ter wereld is aangetast door menselijke activiteiten Hoekgraden berekenen
Hoekgraden berekenen Hoe de zebra aan zijn strepen kwam
Hoe de zebra aan zijn strepen kwam  Wat zijn de zeven stappen in lichtafhankelijke reacties?
Wat zijn de zeven stappen in lichtafhankelijke reacties?  Welk element in het periodiek systeem is een gekleurd gas?
Welk element in het periodiek systeem is een gekleurd gas?  Hoe toont hemoglobine de vier niveaus van eiwitstructuur?
Hoe toont hemoglobine de vier niveaus van eiwitstructuur?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

