
Wetenschap
Beheersing van het equivalentiepunt in titratie-experimenten
Door Claire Gillespie, bijgewerkt op 24 maart 2022
In de analytische chemie is een titratie een kwantitatieve techniek waarbij een oplossing met een bekende concentratie (de titrant) wordt toegevoegd aan een gemeten volume van een andere oplossing met een onbekende concentratie (de analyt). Het proces gaat door totdat de reactie tussen de twee oplossingen voltooid is. Op dit moment wordt dit het equivalentiepunt genoemd , is het aantal mol titrant gelijk aan het aantal mol analyt, waardoor u de concentratie van de analyt nauwkeurig kunt berekenen.
TL;DR
Het equivalentiepunt wordt bereikt wanneer de reagerende soorten stoichiometrisch in evenwicht zijn. Het wordt gedetecteerd door een duidelijke verandering in een indicator of een plateau op een pH-meter, wat aangeeft dat er geen verdere reactie is.
Typen titratie
- Zuur-base titraties – neutralisatie van een zuur door een base of omgekeerd, gewoonlijk gecontroleerd met een kleurindicator of pH-meter.
- Redox-titraties – overdracht van elektronen tussen soorten, vaak met behulp van een oxidatie- of reductiemiddel als titrant.
- Complexometrische titraties – vorming van een stabiel complex tussen de analyt en een ligand, nuttig voor analyse van metaalionen.
- Neerslagtitraties – er vormt zich een neerslag op het equivalentiepunt, zoals bij de titratie van een chloride-ion met zilvernitraat.
Essentiële uitrusting
- Erlenmeyerkolf of bekerglas (bij voorkeur 250 ml)
- Nauwkeurige buret (resolutie 0,01 ml) en standaard
- Analytische balans voor het meten van vaste stoffen
- Gedestilleerd water en pipet voor verdunning
- Indicatoroplossing (bijvoorbeeld fenolftaleïne, methyloranje) of een gekalibreerde pH-meter
- Glaswerk voor het spoelen van vaste stoffen in oplossing
Stapsgewijze procedure
- Weeg of meet de analyt nauwkeurig en breng deze over in de fles. Als de analyt vast is, spoelt u deze met gedestilleerd water in de kolf.
- Voeg gedestilleerd water toe totdat de analyt volledig is opgelost en noteer vervolgens het uiteindelijke volume.
- Als u een kleurindicator gebruikt, voeg dan een paar druppels toe en roer zachtjes om te mengen.
- Vul de buret met de titrant, zorg ervoor dat er geen luchtbellen zijn, en noteer het initiële volume.
- Plaats de kolf onder de buret, sluit de kraan en begin druppelsgewijs de titrant toe te voegen.
- Na elke toevoeging de kolf ronddraaien om een volledige menging te garanderen.
- Ga door met het toevoegen van de titrant totdat de indicator van kleur verandert en zo blijft, of totdat de pH-meter een plateau aangeeft dat het equivalentiepunt aangeeft.
- Registreer de uiteindelijke buretwaarde. Het verschil tussen het begin- en eindvolume, vermenigvuldigd met de titrantconcentratie, is gelijk aan het aantal mol analyt.
- Gebruik het aantal mol analyt en het bekende volume van de analytoplossing om de concentratie ervan te berekenen.
Voor een grotere nauwkeurigheid dient u ten minste twee titraties uit te voeren en de resultaten te middelen. Kalibreer uw buret altijd vóór elke run en houd de punt van de buret schoon en vrij van druppels.
Door deze best practices te volgen, kunt u vol vertrouwen het equivalentiepunt lokaliseren en concentraties bepalen met de precisie die vereist is voor rigoureuze chemische analyses.
 Het oplossingsvolume voor neutralisatie berekenen:een stapsgewijze handleiding
Het oplossingsvolume voor neutralisatie berekenen:een stapsgewijze handleiding  Hoe de mondiale stromen van giftig kwik de menselijke gezondheid beïnvloeden
Hoe de mondiale stromen van giftig kwik de menselijke gezondheid beïnvloeden  Beschrijf de structuur van een algemeen atoom met behulp van drie basale subatomaire deeltjes?
Beschrijf de structuur van een algemeen atoom met behulp van drie basale subatomaire deeltjes?  Hoeveel waterstofmoleculen zijn er nodig om 525 gram ammoniak te produceren?
Hoeveel waterstofmoleculen zijn er nodig om 525 gram ammoniak te produceren?  Bananenschillen maken suikerkoekjes beter voor je
Bananenschillen maken suikerkoekjes beter voor je
 Klimaatvoorspellingen moeten de effecten van CO2 op het leven omvatten
Klimaatvoorspellingen moeten de effecten van CO2 op het leven omvatten Land om te drogen of koud te laten groeien veel planten?
Land om te drogen of koud te laten groeien veel planten?  Waarom zijn niet-native soorten gevaarlijk voor ecosystemen?
Waarom zijn niet-native soorten gevaarlijk voor ecosystemen?  Jongeren gaan de straat op voor het klimaat:wie zijn ze?
Jongeren gaan de straat op voor het klimaat:wie zijn ze? De meest actieve vulkaan van IJsland is waarschijnlijk op weg naar een nieuwe uitbarsting
De meest actieve vulkaan van IJsland is waarschijnlijk op weg naar een nieuwe uitbarsting
Hoofdlijnen
- Wat denk je dat cellen gebruiken als hun ontwerpplannen voor eiwitten?
- Celcontractie drijft de initiële vorming van menselijke embryo's aan, zo blijkt uit onderzoek
- Wat is een gele bacterie?
- Middel dat de groei van bacteriën vertraagt of stopt?
- Wetenschappers identificeren sleutelfactoren die microben helpen gedijen in ruwe omgevingen
- Onderzoekers laten zien hoe sommige genen evolueerden van een immuunfunctie naar een reukrol bij zoogdieren
- Hebben schimmelachtige protisten een celwand?
- Zodra een organisme een wetenschappelijke naam heeft, kan het niet worden gewijzigd?
- Chimpansees zijn geen huisdieren, ongeacht wat sociale media je vertellen
- De geur van oude boeken zou kunnen helpen ze te bewaren

- Elektrische draadeigenschappen van DNA gekoppeld aan kanker

- Nieuwe lijm plakt gemakkelijk, houdt sterk, en is een gas om uit elkaar te trekken

- Neutronen schilderen atomair portret van prototypisch celsignaleringsenzym
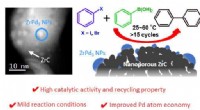
- Een gecombineerde strategie in katalysatorontwerp voor Suzuki kruiskoppelingen
 Wat US Baptisim?
Wat US Baptisim?  Wat is de hernieuwbare bron gevormd uit organisch materiaal?
Wat is de hernieuwbare bron gevormd uit organisch materiaal?  Is de verticale beweging van een projectiel afhankelijk van zijn horizontale beweging?
Is de verticale beweging van een projectiel afhankelijk van zijn horizontale beweging?  Hoe ruimtevaartuig om de aarde rondom de aarde?
Hoe ruimtevaartuig om de aarde rondom de aarde?  Hoe zou het zijn zonder licht?
Hoe zou het zijn zonder licht?  Wat is de afstand tot de zon in astronomische eenheden?
Wat is de afstand tot de zon in astronomische eenheden?  Wat is het verschil tussen oceanen en land absorberen energie?
Wat is het verschil tussen oceanen en land absorberen energie?  Kenmerken van samengestelde vulkanen
Kenmerken van samengestelde vulkanen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

