
Wetenschap
Berekening van het dissociatiepercentage van zwakke zuren – een praktische gids
Wanneer een sterk zuur aan water wordt toegevoegd, dissocieert het volledig:HA → H + + A − . Zwakke zuren dissociëren daarentegen slechts gedeeltelijk.
De mate van dissociatie wordt gekwantificeerd door de zuurdissociatieconstante, Ka :
Ka =([H + ][A − ]) / [HA]
waarbij de haakjes de molaire concentraties aangeven.
Ka is essentieel voor het bepalen van het percentage van een zwak zuur dat bij een bepaalde pH is gedissocieerd.
Ka, pKa en pH verbinden
De pH wordt gedefinieerd als de negatieve logaritme (grondtal 10) van de protonconcentratie:
pH =–log10 [H + ] ⇒ [H + ] =10 –pH
Op dezelfde manier is de relatie tussen Ka en zijn logaritmische tegenhanger, pKa,:
pKa =–log10 Ka ⇒ Ka =10 –pKa
Als zowel de pKa als de pH bekend zijn, kan het percentage dissociatie direct worden berekend.
Voorbeelddissociatieberekening
Beschouw een zwak zuur HA met een pKa van 4,756. Bepaal in een oplossing met een pH van 3,85 het percentage HA dat wordt gedissocieerd.
- Convert pKa naar Ka en pH naar [H
+
]:
- Ka =10 –4,756 =1,754 × 10 –5 M
- [H + ] =10 –3,85 =1,413 × 10 –4 M
- Omdat het zuur zwak is, [H
+
] ≈ [A
−
]. Voeg deze waarden in de Ka-expressie in:
Ka = ([H+][A−]) / [HA] = (1.413 × 10–4 M)(1.413 × 10–4 M) / [HA]
Het oplossen van [HA] levert 0,0011375M op. - Percentage dissociatie =([H + ] / [HA]) × 100% =(1,413 × 10 –4 M / 0,0011375M) × 100% =12,42%.
Fotocredit:stevanovicigor/iStock/GettyImages
 Wat staat er bekend om zware metaalvergiftiging?
Wat staat er bekend om zware metaalvergiftiging?  Hoe wordt zuurstof vervangen?
Hoe wordt zuurstof vervangen?  IJsbestendige coating voor grote constructies is afhankelijk van een prachtige demonstratie van mechanica
IJsbestendige coating voor grote constructies is afhankelijk van een prachtige demonstratie van mechanica Is natriumhypochloriet vrij chloor?
Is natriumhypochloriet vrij chloor?  Als zoutzuur wordt toegevoegd aan natriumhydroxide, neemt de temperatuur toe, maar er is geen zichtbare verandering opgetreden?
Als zoutzuur wordt toegevoegd aan natriumhydroxide, neemt de temperatuur toe, maar er is geen zichtbare verandering opgetreden?
 Beroemde Deltalandforms
Beroemde Deltalandforms Klimaatverandering eist tol van Franse oesterkwekers
Klimaatverandering eist tol van Franse oesterkwekers Netwerkanalyse toepassen op natuurlijke historie:techniek gepopulariseerd via sociale media rangschikt impact van uitsterven
Netwerkanalyse toepassen op natuurlijke historie:techniek gepopulariseerd via sociale media rangschikt impact van uitsterven Het water testen door de lucht in te gaan
Het water testen door de lucht in te gaan Onderzoek vindt dat verzuring van de oceaan koraalrifsystemen bedreigt
Onderzoek vindt dat verzuring van de oceaan koraalrifsystemen bedreigt
Hoofdlijnen
- Wanneer vormden bacteriën?
- Wat is vergelijkbaar met het weefsel van de planten?
- Wat zijn de enzymen die in speeksel worden gevonden en zijn substraatproducten vermelden?
- Welk deel van de cel bevat ribosomen?
- Wat betekent wetenschappelijk idee?
- Wetenschappers duiken diep in hoe haaien de oceaan gebruiken
- Wat is een voorbeeld van vertakte evolutie?
- De Goliath Birdeater:de grootste tarantula die je ten koste van alles moet vermijden
- Wetenschappers verdelen dieren in twee groepen op basis van het feit of een dier een ruggengraat heeft. Waar onwaar.?
- Cyborg-technologie kan nieuwe diagnostiek mogelijk maken, samensmelting van mens en AI
- Het produceren van ethaan uit methaan met behulp van een fotochemische lusstrategie

- Nieuw kristallijn oxide kan het probleem van oververhitting in composietmaterialen oplossen

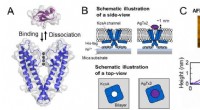
- Mechanisme van remming van schorpioentoxine van K+-kanaal opgehelderd met behulp van snelle AFM
- Mobiel apparaat kan het gemakkelijker maken om schadelijke algenbloei te voorspellen en te beheersen

 Waarom is windenergie een hernieuwbare energiebron?
Waarom is windenergie een hernieuwbare energiebron?  Hebben plantencellen een cyto -skelet?
Hebben plantencellen een cyto -skelet?  Roept op tot einde aan Mexico's vangst van bedreigde bruinvis
Roept op tot einde aan Mexico's vangst van bedreigde bruinvis Wanneer de basis van een gletsjer smelt en opnieuw verreezen, zal dit waarschijnlijk sommige rotsen oppakken, dan wordt dit proces genoemd?
Wanneer de basis van een gletsjer smelt en opnieuw verreezen, zal dit waarschijnlijk sommige rotsen oppakken, dan wordt dit proces genoemd?  Hoe werkt een parachute?
Hoe werkt een parachute?  Wat creëert zonwind?
Wat creëert zonwind?  Wat is de versnelling van een massa van 10 kg als kracht 98N?
Wat is de versnelling van een massa van 10 kg als kracht 98N?  Strengere verkrachtingswetten verkleinen de kans dat een land te maken krijgt met een burgeroorlog, studie vondsten
Strengere verkrachtingswetten verkleinen de kans dat een land te maken krijgt met een burgeroorlog, studie vondsten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

