
Wetenschap
Bereken het exacte gewicht van koper(II)sulfaat-pentahydraat voor nauwkeurige oplossingen
Door Jennifer Yadav Bijgewerkt op 24 maart 2022
iwka/iStock/GettyImages
Koper (II) sulfaatpentahydraat is een gehydrateerd blauw kristal. Het wordt veel gebruikt als algicide en fungicide. Om een oplossing van koper(II)sulfaat te bereiden, wordt de gewenste molariteit gebruikt om het benodigde aantal mol koper(II)sulfaat te berekenen. Dit getal wordt vervolgens omgerekend naar een hoeveelheid grammen die in een laboratorium gemeten kan worden.
Gramformulemassa berekenen
Stap 1
Schrijf de volledige chemische formule voor koper(II)sulfaat-pentahydraat op. Het Romeinse cijfer II, voor 2, geeft aan dat de lading van het koper (Cu) in deze verbinding plus 2 is. Het sulfaation (SO4) heeft een lading van min 2. De formule van koper (II)sulfaat is dus CuSO4 en de verbinding is neutraal. Het pentahydraatgedeelte van de naam betekent dat de verbinding vijf (penta) watermoleculen (hydraat) heeft. Daarom is de volledige formule CuSO4*5H2O. De stip in het midden geeft aan dat de vijf watermoleculen fysiek gebonden zijn aan de koper(II)sulfaatverbinding.
Stap 2
Zoek de atoommassa van elk element op in het periodiek systeem. Dit nummer bevindt zich meestal boven het elementsymbool. Controleer de sleutel op uw periodiek systeem om er zeker van te zijn dat u naar de juiste informatie kijkt. Om berekeningen eenvoudiger te maken, rondt u de atoommassa af op het dichtstbijzijnde gehele getal:koper (Cu) is 64 g/mol, zwavel (S) is 32 g/mol, zuurstof (O) is 16 g/mol en waterstof (H) is 1 g/mol.
Stap 3
Voeg de massa van alle atomen in de chemische formule toe. Omdat de formule slechts één mol koperatomen bevat, hoeft u slechts één keer 64 g toe te voegen. Voor zuurstof bepaalt u echter het totale aantal mol atomen in de formule en vermenigvuldigt u dat aantal met 16 g om de totale massa zuurstof in de verbinding te krijgen. De vergelijkingen zijn:Cu:64g x 1 =64 S:32g x 1 =32 O:16g x 4 =64 H:1g x 10 =10 ("5 H2O" betekent dat er 10 H en 5 O bij betrokken zijn.) O:16g x 5 =80
Het totaal is:64 + 32 + 64 + 10 + 80 =250 g/mol =gram formulemassa CuSO4*5H2O.
Het aantal mol bepalen
Stap 1
Schrijf de molariteitsformule op. Molariteit, of concentratie, is gelijk aan het aantal mol opgeloste stof per liter oplossing. Vereenvoudigd is de formule M =mol/L.
Stap 2
Voer uw gewenste molariteit en volume in de molariteitsformule in. Als je bijvoorbeeld 1 liter van een oplossing van 0,2 M wilt bereiden, vul dan deze waarden in de formule in om het aantal mol op deze manier op te lossen:M =mol/l en 0,2 M =x mol/1 l.
Stap 3
Bereken het aantal benodigde molen koper(II)sulfaat-pentahydraat. Deze bewerking vereist een eenvoudige kruisvermenigvuldiging:x =(0,2 M) (1L) =0,2 mol.
In dit voorbeeld heb je 0,2 mol koper(II)sulfaat-pentahydraat nodig om 1 liter oplossing te maken.
Mollen omrekenen naar gram
Stap 1
Schrijf de formule voor de molberekening op. Het kan worden gebruikt om mollen van een stof om te zetten in grammen van een stof en omgekeerd. Omdat de gramformulemassa het aantal grammen in 1 mol van een stof vertegenwoordigt, kunt u de vereiste massa voor uw oplossing verkrijgen door het aantal mol te vermenigvuldigen met de gramformulemassa. Vereenvoudigd is de formule:Aantal gram =(aantal mol) (massa van de gramformule).
Stap 2
Voer de gramformulemassa die u eerder hebt berekend en het eerder berekende aantal mol in de formule voor molberekeningen in. Als we het eerdere voorbeeld gebruiken, zijn er 0,2 mol koper(II)sulfaat-pentahydraat nodig:Aantal gram =(aantal mol) (massa van de gramformule) Aantal gram =(0,2 mol) (250 g/mol)
Stap 3
Bereken het benodigde aantal gram koper(II)sulfaat-pentahydraat. Een voorbeeld is:(0,2 mol) (250g/mol) =50g.
In dat voorbeeld zou u 50 g vast koper(II)sulfaat-pentahydraat in het laboratorium moeten afmeten en water moeten toevoegen om 1 liter oplossing te maken.
Dingen die nodig zijn
- Periodiek Systeem
- Rekenmachine
TL;DR (te lang; niet gelezen)
De atoommassa op het periodiek systeem vertegenwoordigt het aantal grammen in 1 mol van een element. Eén mol is gelijk aan 6,02 x 1023 atomen. Een hydraat is een vaste stof waaraan water fysiek aan de kristalstructuur is gehecht. Koper (II) sulfaatpentahydraat wordt vaak gebruikt als bestanddeel in medicijnen tegen schimmels, batterijen, mijnbouw, het verven van textiel en galvaniseren, evenals als pesticide. Koper (II) sulfaatpentahydraat kan via verschillende online winkels worden verkregen.
Waarschuwing
Bij het berekenen van de massa van koper(II)sulfaatpentahydraat in gramformule moet u de massa van het water (5 H2O) opnemen dat fysiek aan de verbinding is gebonden. Er kunnen verzendbeperkingen van toepassing zijn bij het bestellen van koper(II)sulfaat-pentahydraat, omdat dit geclassificeerd is als een milieutoxine.
 Toename van de uitstoot van ondergrondse CO2-emissies in Italië als gevolg van aardbevingen
Toename van de uitstoot van ondergrondse CO2-emissies in Italië als gevolg van aardbevingen Hoe bosbranden werken
Hoe bosbranden werken  Voor het gewone riet is bloed dikker dan water. Dat is tenminste wat de aarde ons vertelt
Voor het gewone riet is bloed dikker dan water. Dat is tenminste wat de aarde ons vertelt  De beschikbaarheid van water is veranderd, en de mens is de schuldige
De beschikbaarheid van water is veranderd, en de mens is de schuldige GPM analyseert tropische depressie Kajikis-regenval boven Vietnam en Laos
GPM analyseert tropische depressie Kajikis-regenval boven Vietnam en Laos
Hoofdlijnen
- Hoe kunnen mensen vleugels op natuurlijke wijze laten groeien?
- Een DNA -molecuul bevat duizenden waar?
- Wat gebeurt ertoe dat een hoofdreeksster zijn evenwicht verliest en in de volgende fase in evolutie gaat?
- Welke technologische vooruitgang leidde tot de ontwikkeling van de celtheorie?
- Deze boom is het oudste levende organisme van Europa - een soort van,
- Hoe verschillen algen van andere planten?
- Kunnen eukaryotische cellen genexpressie regelen met behulp van transcriptiefactoren?
- Welke organel bevat genetische informatie in het Molecule DNA?
- Wat onderhoudt de celvorm en verankert organellen op hun plaats en beweegt celbewegingen?
- Verbetering van de hulpmiddelen van de natuur voor het verteren van plastic

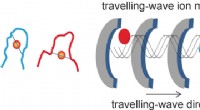
- Travelling-wave ion mobility massaspectrometrie verheldert structuren van gouden vingers
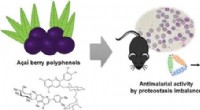
- Aaí bessenextracten bestrijden malaria bij muizen
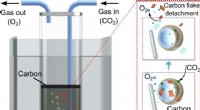
- Vloeibaar metaal bewezen goedkope en efficiënte CO2-converter
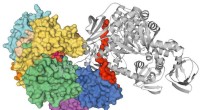
- Een nieuwe generatie antimalariamiddelen
 MUSE onderzoekt onbekende diepten van Hubble Ultra Deep Field
MUSE onderzoekt onbekende diepten van Hubble Ultra Deep Field Facebook-CEO verschijnt voor congres over valutaplan
Facebook-CEO verschijnt voor congres over valutaplan Wat is de functie van mitose?
Wat is de functie van mitose?  Is de overdracht van temperatuur van de ene substantie naar de andere genaamd convectie?
Is de overdracht van temperatuur van de ene substantie naar de andere genaamd convectie?  Onderzoekers ontwikkelen blauwdruk voor toekomstige Indiase steden
Onderzoekers ontwikkelen blauwdruk voor toekomstige Indiase steden Wat is elektroforese in klonen?
Wat is elektroforese in klonen?  Zal iemand u antwoorden Wat is de kracht die lucht uitgeeft op een bepaald gebied?
Zal iemand u antwoorden Wat is de kracht die lucht uitgeeft op een bepaald gebied?  Welke factoren helpen om de hoogte van een golf te bepalen?
Welke factoren helpen om de hoogte van een golf te bepalen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

