
Wetenschap
Hoe u kunt bepalen of een stof een reductie- of oxidatiemiddel is met behulp van het periodiek systeem
Door John Brennan
Bijgewerkt op 24 maart 2022
In de redoxchemie wordt de elektronenoverdracht gevolgd via oxidatiegetallen. Wanneer het oxidatiegetal van een element stijgt – of minder negatief wordt – is het geoxideerd; een afname, of een beweging naar negatiever, duidt op een afname. Denk aan het geheugensteuntje OILRIG (Oxidatie is verlies, reductie is winst) om de richting recht te houden. Een oxidatiemiddel accepteert elektronen en wordt zelf gereduceerd, terwijl een reductiemiddel elektronen doneert en wordt geoxideerd.
Stap 1
Schrijf de uitgebalanceerde chemische vergelijking voor de reactie. De verbranding van propaan wordt bijvoorbeeld weergegeven als:
C3 H8 (g) + 5O2 → 3CO2 (g) + 4H2 O(l)
Stap 2
Wijs oxidatiegetallen toe aan elk element met behulp van deze kernregels:
- Elementen in hun elementaire vorm hebben een oxidatiegetal van0 (bijvoorbeeld O2 , N2 ).
- Fluor is altijd –1 in verbindingen. Zuurstof is –2, behalve in peroxiden of wanneer gebonden aan fluor.
- Waterstof is +1 bij binding aan niet-metalen en –1 bij binding aan metalen.
- Halogenen (groep 17) zijn –1, tenzij ze gepaard gaan met zuurstof of een meer elektronegatief halogeen, in welk geval ze +1 zijn.
- Groep1-metalen zijn +1; metalen uit groep 2 zijn +2.
- De som van de oxidatiegetallen in een neutraal molecuul is gelijk aan 0; in een ion is dit gelijk aan de lading van het ion.
Bijvoorbeeld het sulfaation, SO4 2– , heeft een netto lading van –2, dus de oxidatiegetallen van S en O moeten optellen tot –2.
Stap 3
Vergelijk de oxidatiegetallen aan de kant van de reactanten met die aan de productkant. Een soort waarvan het aantal daalt (of negatiever wordt) heeft minder elektronen gekregen. Een soort waarvan het aantal stijgt (of minder negatief wordt) heeft elektronen verloren – geoxideerd.
In het voorbeeld van propaanverbranding begint zuurstof bij 0 en eindigt bij –2 in zowel CO2 en H2 O, dus zuurstof wordt verminderd. De koolstofatomen van propaan gaan van –3 (in C3 H8 ) tot +4 (in CO2 ), wat oxidatie aangeeft.
Stap 4
Identificeer de oxidatie- en reductiemiddelen:
- De stof die een ander oxideert, is het oxidatiemiddel .
- De stof die een ander reduceert is het reductiemiddel .
Bij de propaan-zuurstofreactie dus O2 is het oxidatiemiddel en C3 H8 is het reductiemiddel.
Stap 5
Houd er rekening mee dat een verbinding beide rollen kan spelen, afhankelijk van de partnersoort. Sommige stoffen verliezen gemakkelijk elektronen en worden doorgaans gezien als reductiemiddelen; anderen blinken uit in het accepteren van elektronen en fungeren als oxidatiemiddelen. De feitelijke rol wordt bepaald door de specifieke reactiecontext.
Dingen die nodig zijn
- Periodiek systeem
- Potlood
- Papier
TL;DR
Het beheersen van oxidatiegetallen vergt oefening. Probeer getallen toe te wijzen aan verschillende samenstellingen totdat de patronen intuïtief worden.
Referenties
- "Chemische principes, de zoektocht naar inzicht, 4e editie"; Peter Atkins en Loretta Jones; 2008.
 Waarom wordt zuurstof een oxidatiemiddel genoemd?
Waarom wordt zuurstof een oxidatiemiddel genoemd?  Hoe regelde de Russen wetenschapper voor het eerst elementen?
Hoe regelde de Russen wetenschapper voor het eerst elementen?  Heeft water zich uitgezet of krimpt bij verhitting?
Heeft water zich uitgezet of krimpt bij verhitting?  Het identificeren van toestanden van materie in chemische formules:een praktische gids
Het identificeren van toestanden van materie in chemische formules:een praktische gids  Is koken een chemische verandering of een psychische verandering?
Is koken een chemische verandering of een psychische verandering?
Hoofdlijnen
- Hoe huilen werkt
- Mitzi en de gigantische haarbal
- Wat is een meercellige massa die het embryo voedt totdat het zelfondersteunende zaailingen wordt?
- Wat zijn de drie belangrijkste divisies van de wetenschap?
- Eiwitten in haaientanden kunnen duiden op wat ze eten
- Wat is de oorsprong van de evolutie van theorie?
- Waarom Twitter president Donald Trump niet zal verbieden
- Wat zijn 3 soorten aseksuele plantreproductie?
- Structuur van het spierstelsel
- Onderzoek vindt ernstige problemen met forensische software

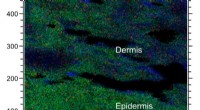
- Nieuwe methode brengt chemicaliën in de huid in kaart
- Belangrijkste eigenschappen van natuurlijk versus synthetisch rubber – een technisch overzicht

- Geldruppels voor regeneratieve geneeskunde
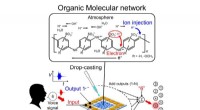
- Intelligentie die voortkomt uit willekeurige polymeernetwerken
 Geluidsgolven sturen deeltjes om zichzelf te assembleren, zelfgenezing
Geluidsgolven sturen deeltjes om zichzelf te assembleren, zelfgenezing Welk organisme komt als laatste in de voedselketen?
Welk organisme komt als laatste in de voedselketen?  Welk type reacties vormen zout?
Welk type reacties vormen zout?  Wat is de volledige set genetische informatie een organisme?
Wat is de volledige set genetische informatie een organisme?  Welk deel van het organisme worden materialen gevormd uit synthese?
Welk deel van het organisme worden materialen gevormd uit synthese?  Het aantal van welke basis is gelijk aan de guanine in een DNA -molecuul?
Het aantal van welke basis is gelijk aan de guanine in een DNA -molecuul?  Foxconn zegt dat het op zoek is naar flexibiliteit met Wisconsin
Foxconn zegt dat het op zoek is naar flexibiliteit met Wisconsin Britneys conservatorium laat zien hoe de erfenis van eugenetica in de VS het leven van gehandicapte vrouwen blijft beïnvloeden
Britneys conservatorium laat zien hoe de erfenis van eugenetica in de VS het leven van gehandicapte vrouwen blijft beïnvloeden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

