
Wetenschap
Hoe het percentage ionisatie van zwakke zuren en basen te berekenen
Door Donny Quinn, bijgewerkt op 24 maart 2022
Afbeelding tegoed:kirisa99/iStock/GettyImages
Sterke zuren en basen dissociëren volledig in een waterige oplossing, wat betekent dat elk zuur molecuul een proton afstaat en dat elk alkalisch molecuul een hydroxide-ion afgeeft. Zwakke zuren, zoals fluorwaterstofzuur, en zwakke basen, zoals ammoniak, dissociëren slechts gedeeltelijk. Het berekenen van het dissociatiepercentage (de fractie van moleculen die ioniseren) geeft inzicht in hun gedrag.
Stap 1:Bepaal de hoeveelheid gedissocieerde soorten
Bij veel problemen wordt deze waarde direct geleverd. In meer geavanceerde contexten moet u dit mogelijk afleiden uit evenwichtsuitdrukkingen of experimentele gegevens.
Stap 2:delen door de initiële concentratie
Neem het aantal mol per liter van de gedissocieerde soorten en deel dit door het aanvankelijke aantal mol per liter van het zuur of de base. De initiële concentratie wordt doorgaans vermeld op het reagensetiket of in de probleemstelling.
Stap 3:Converteren naar een percentage
Vermenigvuldig het resultaat met 100 om de ionisatiegraad in procenten uit te drukken.
TL;DR
Als de directe dissociatiewaarde niet wordt gegeven, moet je evenwichtsuitdrukkingen gebruiken, vaak met behulp van de zure dissociatieconstante (Ka ) – om het percentage dissociatie te berekenen.
Door deze berekening te begrijpen, kunnen scheikundigen voorspellen hoe zwakke zuren en basen zich in oplossing gedragen.
 Zeldzame tropische storm gedegradeerd na het raken van het noordoosten van de VS
Zeldzame tropische storm gedegradeerd na het raken van het noordoosten van de VS Onderzoekers gebruiken AI om prioriteitsgebieden te definiëren voor actie om ontbossing in de Amazone tegen te gaan
Onderzoekers gebruiken AI om prioriteitsgebieden te definiëren voor actie om ontbossing in de Amazone tegen te gaan Onderzoekers onderzoeken hoe planten zich aanpassen aan het klimaat
Onderzoekers onderzoeken hoe planten zich aanpassen aan het klimaat  Facebook, Google en Amazon te groot? Waarom die vraag steeds weer opduikt
Facebook, Google en Amazon te groot? Waarom die vraag steeds weer opduikt  Klimaatactie zal de gezondheid verbeteren en levens redden, nu en in de toekomst
Klimaatactie zal de gezondheid verbeteren en levens redden, nu en in de toekomst
Hoofdlijnen
- Wat is het voedselweb van een toucan?
- Welke wetenschapper heeft bijgedragen aan de evolutietheorie door de studie van natuurlijke selectie?
- Wat is het verschil tussen de chromosomen van het sperma en het ei?
- Hoe eiwitreceptoren op cellen in- en uitschakelen
- Welk genotype illustreert codominantie van allelen die het bloedgroep bij mensen regelen?
- Officiële vishandel onderschat wereldwijde vangsten enorm
- 98% van de keizerspinguïnkolonies zou in 2100 uitgestorven kunnen zijn. Kan de bescherming van de Endangered Species Act hen helpen?
- Wat wordt geproduceerd door mitose bij mensen?
- Wat wordt bedoeld met de term atrofie?
- Je gelooft het maar:caloriearme spread voornamelijk gemaakt van water

- Onderzoekers ontdekken C-H-bindingsactiveringsreacties bij lage temperatuur door foto-geïnduceerde middelen
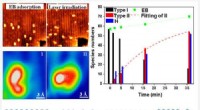
- Groen materiaal voor koeling geïdentificeerd

- Onderzoek suggereert dat polymeercomposiet kan dienen als lichter, niet-giftige stralingsafscherming

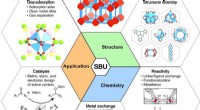
- Secundaire bouweenheden (SBU's) - het keerpunt in de ontwikkeling van metaal-organische raamwerken (MOF's)
 Een noordelijke circumpolair sterrenbeeld dat eruit ziet als een M?
Een noordelijke circumpolair sterrenbeeld dat eruit ziet als een M?  Hoe gendernormen en baanverlies de relatiestatus beïnvloeden
Hoe gendernormen en baanverlies de relatiestatus beïnvloeden Wat zijn de kenmerken van een vijfhoek, zeshoek & octagon?
Wat zijn de kenmerken van een vijfhoek, zeshoek & octagon?  Totale zonsverduisteringen bieden de mogelijkheid om met wetenschap, cultuur en geschiedenis in aanraking te komen
Totale zonsverduisteringen bieden de mogelijkheid om met wetenschap, cultuur en geschiedenis in aanraking te komen  Bewijs gevonden voor regionale anomalie van magnetische velden in Zuidoost-Azië 800 jaar geleden
Bewijs gevonden voor regionale anomalie van magnetische velden in Zuidoost-Azië 800 jaar geleden Welke energieverandering vindt plaats in een constant versnellend object?
Welke energieverandering vindt plaats in een constant versnellend object?  Structuur van gesteenten uit fossiele brandstoffen is eindelijk gedecodeerd
Structuur van gesteenten uit fossiele brandstoffen is eindelijk gedecodeerd MAXI J1348-630 is een zwart gat X-ray binaire, observaties suggereren:
MAXI J1348-630 is een zwart gat X-ray binaire, observaties suggereren:
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

