
Wetenschap
Waarom bepaalde stoffen niet in water oplossen:belangrijke wetenschappelijke principes
Door Claire Gillespie Bijgewerkt op 24 maart 2022
showcake/iStock/GettyImages
Water wordt vaak het ‘universele oplosmiddel’ genoemd, omdat het een breed scala aan stoffen kan oplossen. Wanneer een opgeloste stof volledig oplost in een oplosmiddel, wordt het resulterende homogene mengsel een oplossing genoemd. Ondanks de opmerkelijke solvabiliteit van water, lossen sommige materialen er eenvoudigweg niet in op.
TL;DR
Olie, paraffinewas en zand zijn klassieke voorbeelden van stoffen die onopgelost blijven in water. Zelfs zeer oplosbare verbindingen bereiken een verzadigingslimiet waarboven extra opgeloste stoffen als vast residu achterblijven.
Aantrekkelijke krachten en oplosbaarheid
De oplosbaarheid hangt af van de relatieve sterkte van de aantrekkingskrachten tussen opgeloste deeltjes, oplosmiddeldeeltjes en tussen opgeloste stof en oplosmiddel. Glucose lost bijvoorbeeld gemakkelijk op omdat de waterstofbruggende interacties met water zwaarder wegen dan zowel de glucose-glucose- als de water-water-interacties.
Vermengbaarheid versus niet-mengbaarheid
Wanneer twee vloeistoffen zich volledig vermengen, zijn ze mengbaar; anders zijn ze niet mengbaar. Olie (koolwaterstoffen) en water zijn voorbeelden van onmengbaarheid. De lagere dichtheid van olie zorgt ervoor dat olie blijft drijven en dat de oliedruppeltjes nooit in de waterfase integreren.
Polariteit is belangrijk
De polariteit van water – gedeeltelijk positieve lading op waterstofatomen en gedeeltelijk negatieve lading op zuurstof – maakt het zeer selectief. Polaire of ionische opgeloste stoffen worden aangetrokken door water, terwijl niet-polaire stoffen zoals paraffinewas (lange ketens van C en H) worden afgestoten, waarbij de regel ‘het gelijke oplost het gelijke’ wordt nageleefd.
Ontbinding, erosie en opschorting
Het is essentieel om ontbinding te onderscheiden van erosie en opschorting. Zand lost bijvoorbeeld niet op omdat de interne aantrekkingskracht van water de interacties tussen water en zand domineert. Door roeren blijft het zand hangen, waardoor een troebel mengsel ontstaat; als het roeren stopt, bezinkt het zand en wordt het water erboven helder. Langdurig watercontact kan rotsoppervlakken eroderen, waardoor fijne deeltjes stroomafwaarts worden getransporteerd, maar dit is eerder een fysieke verwijdering dan een chemische oplossing.
Verzadigingslimieten
Zelfs opgeloste stoffen die zeer oplosbaar zijn, zoals suiker of natriumchloride, vertonen een verzadigingspunt. Bij evenwicht is de oplossnelheid gelijk aan de herkristallisatiesnelheid, dus het toevoegen van meer opgeloste stof verhoogt de concentratie niet; in plaats daarvan blijft het overschot als onopgeloste vaste stof.
Deze principes verklaren waarom bepaalde alledaagse materialen niet oplossen in water en onderstrepen het genuanceerde samenspel van moleculaire krachten in de waterige chemie.
 Is het endo- of exo -thermisch wanneer u loodkabel II -nitraat mengt, wordt gemengd met kaliumjodide?
Is het endo- of exo -thermisch wanneer u loodkabel II -nitraat mengt, wordt gemengd met kaliumjodide?  Wat zijn III-groepselementen in het periodiek systeem?
Wat zijn III-groepselementen in het periodiek systeem?  Hoe de eerste ionisatie-energie van het waterstofatoom te berekenen met betrekking tot de Balmer-serie
Hoe de eerste ionisatie-energie van het waterstofatoom te berekenen met betrekking tot de Balmer-serie Wat is het vloeibare medium van een oplossing?
Wat is het vloeibare medium van een oplossing?  Hoe de eindconcentratie van een oplossing met verschillende concentraties te berekenen
Hoe de eindconcentratie van een oplossing met verschillende concentraties te berekenen
 Stedelijke hitte en koude eilandeffecten gecontroleerd door landbouw en irrigatie
Stedelijke hitte en koude eilandeffecten gecontroleerd door landbouw en irrigatie Een school met nieuwe gegevens over hoe het klimaat de visserij beïnvloedt
Een school met nieuwe gegevens over hoe het klimaat de visserij beïnvloedt  Omgevingsstress veroorzaakt nu al de dood:deze chaoskaart laat zien waar
Omgevingsstress veroorzaakt nu al de dood:deze chaoskaart laat zien waar Inheems eigendom van de Trans Mountain-pijpleiding zou het milieu beschermen
Inheems eigendom van de Trans Mountain-pijpleiding zou het milieu beschermen Nieuwe NASA-missie om het gebruik van plantwater vanuit de ruimte te detecteren
Nieuwe NASA-missie om het gebruik van plantwater vanuit de ruimte te detecteren
Hoofdlijnen
- Waarom gebruikten biologen classificatie?
- Wat is de rol van diffusie in een cel?
- Hoe adhesief eiwit malaria veroorzaakt
- Wetenschappers classificeren dieren door gedeeld wat?
- Een kolonie bacteriën is afkomstig van hoeveel bacteriën?
- Wat zijn aminozuren en hoeveel daar?
- 'Freeze-frame'-eiwitten laten zien hoe kanker evolueert:onderzoekers leggen ongrijpbare aanwijzingen vast over het pad van cellen naar
- Waarom veranderden soorten organismen in de loop van de tijd?
- Waar is de Gene ST2 voor verantwoordelijk voor?
- Team gebruikt heet water om fotokatalysator te vormen
- Cellulaire stress verdediging
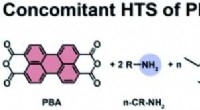
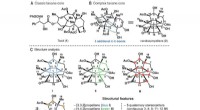
- Eindelijk synthetisch canataxpropellane:een van de meest complexe producten van de natuur reproduceren
- Nieuwe methode biedt stabieler, efficiënte elektrokatalytische reacties
- Video:Is het echt alleen chemisch reinigen?

 Indonesië gaat 49 containers met afval terug naar Europa ons
Indonesië gaat 49 containers met afval terug naar Europa ons Wat is eenmicroscoop met één cel eenvoudige planten sommigen worden schadelijk gegeten die nuttig zijn geclassificeerd om te vormen?
Wat is eenmicroscoop met één cel eenvoudige planten sommigen worden schadelijk gegeten die nuttig zijn geclassificeerd om te vormen?  Welke geologische periode duurde bijna 7 8e geschiedenis?
Welke geologische periode duurde bijna 7 8e geschiedenis?  Vrouwen schaars in de ene procent:Glazen plafond is groter dan gedacht studie toont
Vrouwen schaars in de ene procent:Glazen plafond is groter dan gedacht studie toont Wanneer gingen de astronauten naar de maan?
Wanneer gingen de astronauten naar de maan?  Hoe experimenteer je in de wetenschap?
Hoe experimenteer je in de wetenschap?  Ironii chloride aq zilvernitraat ironii s?
Ironii chloride aq zilvernitraat ironii s?  Wat is nodig om stikstof te combineren met zuurstof?
Wat is nodig om stikstof te combineren met zuurstof?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

