
Wetenschap
Ionen gevormd wanneer zilvernitraat oplost in water
Door Michael Judge
Bijgewerkt op 24 maart 2022
Ionische dissociatie van zilvernitraat
Zilvernitraat (AgNO₃) is een klassiek voorbeeld van een ionische verbinding die gemakkelijk in water oplost. Bij oplossing scheidt het rooster zich in de samenstellende ionen:het zilverkation (Ag⁺) en het nitraatanion (NO₃⁻). Dit proces wordt aangedreven door de sterke elektrostatische aantrekkingskracht tussen de tegengesteld geladen soorten.
Zilverkation (Ag⁺)
Het zilverion heeft een enkele positieve lading en heeft één elektron verloren. Kationen zoals Ag⁺ staan bekend om hun antimicrobiële activiteit; Zo heeft een onderzoek van het Finse Nationale Volksgezondheidsinstituut aangetoond dat Ag⁺ de groei van Legionella effectief kan remmen. bacteriën. Deze eigenschappen hebben geleid tot medische toepassingen, hoewel zilverionen giftig blijven voor een breed scala aan microben.
Nitraatanion (NO₃⁻)
Het nitraation is een driewaardige groep bestaande uit één stikstofatoom gebonden aan drie zuurstofatomen, met een netto negatieve lading. NO₃⁻ is van nature aanwezig in voedingsmiddelen zoals spinazie en is een belangrijk onderdeel van veel meststoffen. Hoewel het in gematigde hoeveelheden essentieel is, kan een overmatige inname van nitraat gezondheidsrisico's met zich meebrengen. Daarom wordt de concentratie ervan in de voedsel- en watervoorziening gereguleerd.
Extra ionen in oplossing
Zelfs in ultrapuur water ontstaan er sporen van ionen door de auto-ionisatie van watermoleculen:
- Hydroniumionen (H₃O⁺) worden gevormd wanneer H⁺ zich associeert met water.
- Hydrooxide-ionen (OH⁻) worden gelijktijdig geproduceerd.
 Wat zijn de limieten voor bepalingchloride volgens de Volhard -methode?
Wat zijn de limieten voor bepalingchloride volgens de Volhard -methode?  Welke van deze zijn bronstead-basen - HCl NH3 NaOH?
Welke van deze zijn bronstead-basen - HCl NH3 NaOH?  Hoe schaadt zure neerslagomgeving?
Hoe schaadt zure neerslagomgeving?  Hoeveel procent van de lucht bestaat uit stikstof en zuurstof samen?
Hoeveel procent van de lucht bestaat uit stikstof en zuurstof samen?  Welke van de volgende is de naam gegeven aan een situatie waarin ene splijtingsreactie precies meer reactie innam?
Welke van de volgende is de naam gegeven aan een situatie waarin ene splijtingsreactie precies meer reactie innam?
 Het is tijd om het verstoorde Amerikaanse voedselsysteem van de grond af aan te heroverwegen
Het is tijd om het verstoorde Amerikaanse voedselsysteem van de grond af aan te heroverwegen Waarom wordt geografie beschouwd als de koningin van de wetenschap?
Waarom wordt geografie beschouwd als de koningin van de wetenschap?  Boaty McBoatface-missie geeft nieuw inzicht in opwarmende oceaanafgrond
Boaty McBoatface-missie geeft nieuw inzicht in opwarmende oceaanafgrond Hoe observeren wetenschappers het binnenlandse interieur?
Hoe observeren wetenschappers het binnenlandse interieur?  Conclusie van natuurlijke hulpbronnen voor uitputtingbehoud?
Conclusie van natuurlijke hulpbronnen voor uitputtingbehoud?
Hoofdlijnen
- Wiskundige modellen laten zien hoe organismen de som van hun genen overstijgen
- Wat betekent de STEM Anthro?
- Welke virus infecteren bacteriën?
- Waarom kiezen de X- en Y -chromosomen geslachten?
- Wat is een voorbeeld van een levend wezen met slechts één cel?
- Wat is biologische stressor?
- Dochtercellen geproduceerd wanneer ze mitose ondergaan, zijn genetisch en dochter meiosis.?
- Waarom kameleontongen werken in de kou (met video)
- Wat is het deel van een streng -DNA met regulerende sequenties?
- Leveren van hoogwaardige kankerbeeldvormende isotopen

- Onderzoek zou assemblagelijnsynthese van veelvoorkomende aminebevattende medicijnen mogelijk kunnen maken

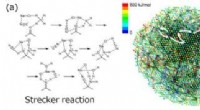
- Terugspoelen indrukken om chemische reacties in meerdere stappen te voorspellen
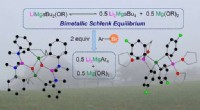
- Lithium-magnesium alkyl-alkoxy tussenproducten in Br-Mg uitwisseling
- Ingenieurs pionieren met het vormingsproces van platinagranaten, eerste waarneming ooit bereiken

 Identificatie van dierensporen in Pennsylvania
Identificatie van dierensporen in Pennsylvania Wat zou er gebeuren met deze streng DNA tijdens transcriptie TACGCGCATTGTCGTCTAGGTTTCGATATATTAGCTACG?
Wat zou er gebeuren met deze streng DNA tijdens transcriptie TACGCGCATTGTCGTCTAGGTTTCGATATATTAGCTACG?  Hoe te spelen Math Bingo
Hoe te spelen Math Bingo Wat gebeurt er met de frequentie van golf als u de golflengte verhoogt die snelheid constant houdt?
Wat gebeurt er met de frequentie van golf als u de golflengte verhoogt die snelheid constant houdt?  Onderzoek onthult nieuwe inzichten in excitonbindende energieën in organische halfgeleiders
Onderzoek onthult nieuwe inzichten in excitonbindende energieën in organische halfgeleiders  Shanghai krijgt geautomatiseerde bank met VR, robots, gezicht scannen
Shanghai krijgt geautomatiseerde bank met VR, robots, gezicht scannen Wanneer het licht in een oppervlak weken dat het heter wordt, wordt het heet?
Wanneer het licht in een oppervlak weken dat het heter wordt, wordt het heet?  De amfotere aard van water:zuur-base-gedrag begrijpen
De amfotere aard van water:zuur-base-gedrag begrijpen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

