
Wetenschap
Wat is het energieprofiel van een chemische reactie, inclusief activering vrije verandering en overgangstoestand?
Energieprofiel van een chemische reactie
Het energieprofiel van een chemische reactie is een grafische weergave van de energieveranderingen die optreden tijdens de reactie. Het toont meestal de energie van de reactanten, de producten en de overgangstoestand langs de reactiecoördinaat.
Sleutelcomponenten:
* reactanten: De uitgangsmaterialen van de reactie, gelegen aan het begin van het profiel.
* Producten: De stoffen gevormd door de reactie, gelegen aan het einde van het profiel.
* overgangstoestand: Het hoogste energiepunt in het reactieprofiel, dat een onstabiel, kortstondig tussenproduct vertegenwoordigt. Het is het punt waar bindingen tegelijkertijd breken en zich vormen.
* Activatie -energie (EA): Het energieverschil tussen de reactanten en de overgangstoestand. Het is de minimale hoeveelheid energie die nodig is om de reactie te laten optreden.
* Vrije energieverandering (ΔG): Het verschil in vrije energie tussen de reactanten en de producten. Een negatieve Ag duidt op een energetisch gunstige (spontane) reactie.
Energieprofieldiagram:
Het diagram ziet er meestal zo uit:
[Voeg een diagram in dat een reactieprofiel weergeeft met reactanten, producten, overgangstoestand, activeringsenergie en vrije energieverandering.]
Verklaring:
* De reactie begint met reactanten op een bepaald energieniveau.
* De reactanten moeten de activeringsenergiebarrière overwinnen om de overgangstoestand te bereiken.
* In de overgangstoestand bevinden de moleculen zich in een zeer onstabiele configuratie, klaar om te herschikken om de producten te vormen.
* Na het oversteken van de overgangstoestand neemt de energie van het systeem af naarmate de producten zich vormen.
* Het verschil in energie tussen reactanten en producten is de vrije energieverandering (ΔG).
Relatie tussen activeringsenergie, vrije energieverandering en reactiesnelheid:
* Activatie -energie (EA): Hogere activeringsenergie leidt tot een langzamere reactiesnelheid. Er is meer energie voor nodig voor reactanten om de overgangstoestand te bereiken.
* Vrije energieverandering (ΔG): Een negatieve Ag duidt op een spontane reactie die productvorming bevordert. Een positieve Ag geeft een niet-spontane reactie aan die vereist dat energie-input doorgaat.
* reactiesnelheid: De snelheid waarmee reactanten worden omgezet in producten. Snellere reacties hebben lagere activeringsenergieën en zijn energetisch gunstiger (negatieve ΔG).
Samenvattend:
Het energieprofiel van een chemische reactie biedt waardevolle informatie over de energetica van het proces en helpt de factoren te begrijpen die de reactiesnelheid beïnvloeden. De activeringsenergie en vrije energieverandering zijn cruciale parameters die de haalbaarheid en snelheid van een reactie bepalen.
Hoofdlijnen
- Wetenschappers laten zien hoe parasieten bruine schaaldieren in moerassen in neonzombies veranderen
- Hoe het verbod op positieve discriminatie selectieve hogescholen en de beroepsbevolking minder divers maakt
- Hoe reproduceert het verkoudheidsvirus zich?
- Wat zijn de organen in het juiste iliacale gebied?
- Wat moet ik doen als ik een eenzame, gezellige walvisachtigen tegenkom?
- Vangstvissen kan temperatuurpieken veroorzaken bij haaien
- Biologische klok gevonden in schimmelparasiet werpt meer licht op het fenomeen zombiemieren
- Hoe geven de overblijfselstructuren aan dat de huidige organismen verschillen van hun oude voorouders?
- DNA-ontdekking kan licht werpen op zeldzame kinderziekte
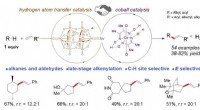
- Nieuwe methode voor functionalisering van koolstof-waterstofbindingen in een laat stadium
- Vissen naar één slechte cel uit triljoenen goede

- Verrode fluorescerende zijde kan schadelijke bacteriën doden als biomedische en milieuremedie
- De DNA-smeltcurve nauwkeuriger maken

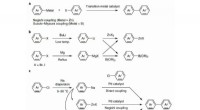
- Chemici tonen aan dat natrium veilig kan worden gebruikt voor kruiskoppelingsreacties
 Veranderende gemeenschappen kunnen het succes van de evacuatierichtlijnen van IJsland beïnvloeden
Veranderende gemeenschappen kunnen het succes van de evacuatierichtlijnen van IJsland beïnvloeden Facebook AI geeft kaarten de mogelijkheid om robots te helpen de weg te vinden
Facebook AI geeft kaarten de mogelijkheid om robots te helpen de weg te vinden Hoe beschrijf je het landschap dat door alpine gletsjers is gemaakt in vergelijking met continentale gletsjers?
Hoe beschrijf je het landschap dat door alpine gletsjers is gemaakt in vergelijking met continentale gletsjers?  Wat zijn de effecten van opname- en verlieswater in dierlijke cellen?
Wat zijn de effecten van opname- en verlieswater in dierlijke cellen?  Goed nieuws? Groenland smelt, maar minder snel dan voorspeld
Goed nieuws? Groenland smelt, maar minder snel dan voorspeld  Hoe tarwestro-afval om te zetten in groene chemicaliën?
Hoe tarwestro-afval om te zetten in groene chemicaliën? Water splitsen voor de prijs van een nikkel
Water splitsen voor de prijs van een nikkel Astronomen zien een gasreus groeien, recht voor hun ogen
Astronomen zien een gasreus groeien, recht voor hun ogen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


