
Wetenschap
De mol begrijpen:een sleutelconcept in de chemie

Wanneer de meeste mensen het woord ‘mol’ horen, stellen ze zich een harig ondergronds knaagdier voor. In de scheikunde is een mol echter een fundamentele eenheid die wetenschappers in staat stelt atomen en moleculen nauwkeurig te tellen.
TL;DR (te lang; niet gelezen)
Een chemische mol is de hoeveelheid van een stof die hetzelfde aantal atomen of moleculen bevat als 12 gram koolstof-12. Dit getal (de constante van Avogadro) is 6,022×10 23 (ongeveer 602 hexillion).
Meting in het Scheikundig Laboratorium
Atomen zijn oneindig klein, dus conventionele eenheden zoals gram of liter zijn niet geschikt om ze te kwantificeren. Een mol biedt een handige, grootschalige eenheid – net zoals een dozijn twaalf items vertegenwoordigt – waardoor scheikundigen op hanteerbare schaal met getallen kunnen werken. 500.000 koolstofatomen zouden bijvoorbeeld ongeveer de breedte van een mensenhaar hebben; een mol bevat 6,022×10 23 zulke atomen.
Wetenschapsgeschiedenis:Avogadro
Het concept van de mol is afkomstig van de 19e-eeuwse Italiaanse wetenschapper Amedeo Avogadro, die voorstelde dat gelijke volumes gassen bij dezelfde temperatuur en druk gelijke aantallen moleculen bevatten. Hoewel zijn ideeën aanvankelijk over het hoofd werden gezien, werden ze later de basis voor de constante van Avogadro, een hoeksteen van de moderne chemie.
Atomen tellen
De constante van Avogadro is gelijk aan het aantal atomen in 12 gram van de meest voorkomende isotoop van koolstof (koolstof-12). Eén mol van welke stof dan ook bevat precies zoveel atomaire of moleculaire entiteiten. Eén mol water, één mol ijzer of zelfs één mol van een hypothetische olifant bevatten dus allemaal 6,022×10 23 deeltjes.
Mollen en metingen
Voor elementaire stoffen weegt één mol hetzelfde aantal gram als het atoomgewicht van het element (gemakkelijk te vinden in het periodiek systeem). Voor moleculen is de molaire massa de som van de atoomgewichten van alle samenstellende atomen. Bijvoorbeeld water (H2 O) heeft een molaire massa van 18,016 g/mol (2 x 1,008 g voor waterstof + 16,00 g voor zuurstof). De eenheid wordt afgekort als mol .Het begrijpen van de mol is essentieel voor het berekenen van reactie-stoichiometrie, het bepalen van empirische formules en het omrekenen tussen massa, mol en deeltjes - allemaal essentiële vaardigheden voor elke scheikundige of scheikundestudent.
 Welke elementen vormen het meest waarschijnlijk een ionische verbinding met kalium A.NA B.CA C.C D.O?
Welke elementen vormen het meest waarschijnlijk een ionische verbinding met kalium A.NA B.CA C.C D.O?  Wat wordt overgebracht tussen een geconjugeerd zuur basepaar?
Wat wordt overgebracht tussen een geconjugeerd zuur basepaar?  Wat is een samengestelde fout?
Wat is een samengestelde fout?  Wat is de pH van 10 mol per liter natriumhydroxide -oplossing?
Wat is de pH van 10 mol per liter natriumhydroxide -oplossing?  Wetenschappers ontdekken unieke rekbare geleider
Wetenschappers ontdekken unieke rekbare geleider
 Het eigendom van licht dat we nodig hebben om de meeste dingen te zien?
Het eigendom van licht dat we nodig hebben om de meeste dingen te zien?  Hoe planten omgaan met ijzertekort
Hoe planten omgaan met ijzertekort  Welke belangrijke attitudes bezitten een succesvolle wetenschapper?
Welke belangrijke attitudes bezitten een succesvolle wetenschapper?  Wat betekent onzichtbaar in de wetenschap?
Wat betekent onzichtbaar in de wetenschap?  La Nina-achtige oceaankoelingspatronen intensiveren tropische cyclonen in het noordwesten van de Stille Oceaan
La Nina-achtige oceaankoelingspatronen intensiveren tropische cyclonen in het noordwesten van de Stille Oceaan
Hoofdlijnen
- Wat helpt kleine plantachtige organismen te groeien op het oppervlak van de oceaan?
- Moleculaire eenheden die samenvoegen om DNA te vormen?
- Darwin en theorie van gemeenschappelijke afkomst stelt dat alle organismen?
- Wat eet microscopische organismen?
- Leg uit waarom planten op cellulaire niveau meer gemeen hebben met dieren dan bacteriën?
- Wat betekent filter in de wetenschap?
- Voelen planten pijn? Een inleiding over plantenneurobiologie
- Uit onderzoek blijkt dat alle Afrikaanse carnivoren risico lopen op verlies van hun bereik
- Is RNA koolhydraateiwitlipide of nucleïnezuur?
- Wetenschappers persen katalysatoren in gastheermaterialen zoals een schip in een fles

- Geautomatiseerde optimalisatie en synthese van geneesmiddelen in de cloud

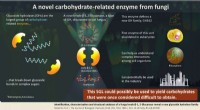
- Nieuwe familie in de buurt:een nieuwe groep glycosidische enzymen
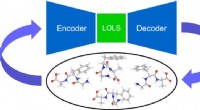
- Nieuwe machine learning-benadering vergemakkelijkt het zoeken naar moleculaire conformeren in complexe moleculen
- Een potentieel goedkope, efficiënt en milieuvriendelijk systeem voor het zuiveren van aardgas

 Wie was de eerste schrijver van het fysica -boek?
Wie was de eerste schrijver van het fysica -boek?  Planeten maken in een raket
Planeten maken in een raket Regeneratie kan voor oudere mensen isolatie veroorzaken, studie vondsten
Regeneratie kan voor oudere mensen isolatie veroorzaken, studie vondsten Wat is -67F in Celsius?
Wat is -67F in Celsius?  Compact Muon Solenoid op zoek naar nieuwe fysica
Compact Muon Solenoid op zoek naar nieuwe fysica Wat was het eerste ruimtevaartuig dat de donkere kant van de maan observeerde?
Wat was het eerste ruimtevaartuig dat de donkere kant van de maan observeerde?  Welke term verklaart een objectensnelheid is in de loop van de tijd toegenomen of verlaagd?
Welke term verklaart een objectensnelheid is in de loop van de tijd toegenomen of verlaagd?  Genderkloven in de financiering van onderzoek zijn te wijten aan een minder gunstige beoordeling van vrouwen, niet hun wetenschap
Genderkloven in de financiering van onderzoek zijn te wijten aan een minder gunstige beoordeling van vrouwen, niet hun wetenschap
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

