
Wetenschap
Berekening van de hydroniumionconcentratie op basis van de hydroxideconcentratie
De relatie begrijpen
* Waterauto-ionisatie: Watermoleculen kunnen met elkaar reageren, waarbij hydroniumionen (H₃O⁺) en hydroxide-ionen (OH⁻) ontstaan. Dit wordt weergegeven door het evenwicht:
2H₂O ⇌ H₃O⁺ + OH⁻
* Kw: Het product van de hydronium- en hydroxide-ionconcentraties is een constante genaamd Kw, die gelijk is aan 1,0 x 10⁻¹⁴ bij 25°C.
Kw =[H₃O⁺] [OH⁻] =1,0 x 10⁻¹⁴
Berekening
1. Ken de hydroxideconcentratie: Je krijgt [OH⁻] =0,0000125 M, wat kan worden geschreven als 1,25 x 10⁻⁵ M.
2. Los de hydroniumconcentratie op: Met behulp van de Kw-vergelijking:
[H₃O⁺] =Kw / [OH⁻] =(1,0 x 10⁻¹⁴) / (1,25 x 10⁻⁵) =8,0 x 10⁻¹⁰ M
Antwoord: De hydroniumionconcentratie in de oplossing is 8,0 x 10⁻¹⁰ M.
Hoofdlijnen
- Is nucleair membraan in een plant- of dierlijke cel?
- Evolutie van parasietvirussen geeft aan hoe Leishmania voor het eerst gewervelde dieren heeft geïnfecteerd
- Cilia en Flagella bewegen door energie die wordt geboden door de enzymatische afbraak van ATP Wat?
- Wat is het voorbeeld van seksuele organismen?
- Welke kenmerken van het meest single celled organisme stellen hen in staat om hun levensactiviteiten voort te zetten en homeostase te behouden?
- Hoe heeft de evolutietheorie de wetenschap geholpen?
- Waar wordt vergelijkende genomics voor gebruikt?
- Wat overwinterende eekhoorns astronauten kunnen leren
- Vrijgen van genetische parasieten kan leiden tot nieuwe verdediging tegen gevaarlijke bacteriën
- Ontwikkeling van een 3D-deeltjesmodel voor afzonderlijke deeltjes in batterij-elektroden
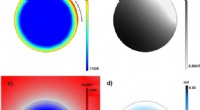
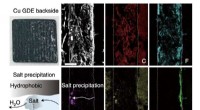
- Bifunctionele ionomeren gebruiken als elektrolyten om ethyleen uit koolstofdioxide te synthetiseren
- Hoeveel protonen bevat een neutraal atoom?
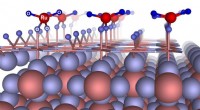
- Wetenschappers verklaren het fenomeen pseudocapaciteit in supercondensatoren
- Dichtheid van zoutwater versus zoetwater:het verschil begrijpen

 Onderzoekers vinden de dynamiek achter de opmerkelijke Groenlandse polynya-formatie in augustus 2018
Onderzoekers vinden de dynamiek achter de opmerkelijke Groenlandse polynya-formatie in augustus 2018 Wanneer zijn er twee verschillende allelen voor een eigenschap?
Wanneer zijn er twee verschillende allelen voor een eigenschap?  Hacks dwarsbomen door te denken als de mensen erachter
Hacks dwarsbomen door te denken als de mensen erachter Zet je schrap, ontkenners van klimaatverandering:het coronavirus maakt de overgang naar een koolstofarme economie urgenter
Zet je schrap, ontkenners van klimaatverandering:het coronavirus maakt de overgang naar een koolstofarme economie urgenter Is de waterstofbinding afhankelijk van de pH?
Is de waterstofbinding afhankelijk van de pH?  Waarom COVID-19 een les is voor Afrika om sociale bijstand te financieren
Waarom COVID-19 een les is voor Afrika om sociale bijstand te financieren Waarom slaan cellen grote hoeveelheden ATP op?
Waarom slaan cellen grote hoeveelheden ATP op?  Brandweerlieden bestrijden nieuwe branden in Californië
Brandweerlieden bestrijden nieuwe branden in Californië
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


