
Wetenschap
Waarom alcoholen hoger koken dan alkanen met een vergelijkbare molaire massa
Molar massa en kookpunt
Het kookpunt stijgt over het algemeen met toenemende molmassa omdat grotere moleculen sterkere Londense dispersiekrachten bezitten. Bij het vergelijken van moleculen met een vrijwel identieke molaire massa kunnen structurele verschillen echter domineren.
Structurele verschillen:alcoholen versus alkanen
Alcoholen bevatten een hydroxylgroep (–OH) gehecht aan een koolstofatoom, terwijl alkanen uitsluitend uit koolstof-waterstofbindingen bestaan. De hydroxylgroep introduceert polariteit en het vermogen om waterstofbruggen te vormen, een kenmerk dat bij alkanen ontbreekt.
Intermoleculaire krachten in het spel
De hiërarchie van intermoleculaire aantrekkingen, van sterk naar zwak, is:ionisch> waterstofbinding> dipool-dipool> Londense dispersie. Alcoholen profiteren van waterstofbruggen, terwijl alkanen alleen afhankelijk zijn van dispersiekrachten.
- Alcoholen:hydroxylgroep → waterstofbruggen (sterk, directioneel)
- Alkanen:geen heteroatomen → alleen London-dispersie (zwak, niet-directioneel)
Invloed op kookpunt
Koken vindt plaats wanneer kinetische energie deze intermoleculaire krachten overwint. Waterstofbruggen vereisen aanzienlijk meer energie om te breken dan dispersiekrachten, dus alcoholen met dezelfde molaire massa als alkanen zullen hogere kookpunten hebben. Ethanol (C₂H₅OH) kookt bijvoorbeeld bij 78 °C, terwijl het isomere alkaanbutaan (C₄H₁₀) kookt bij –0,5 °C, ondanks vergelijkbare molecuulgewichten.
BenchBo/iStock/GettyImages
Hoofdlijnen
- Is een chromosoomlevende dingen?
- Welke dieren zijn circadiane ritmes?
- Waarom vallen sommige mensen flauw bij het zien van bloed? Een klinisch perspectief
- De elektronentransportketens van cellulaire ademhaling bevinden zich?
- Theorie van de evolutie van geslachten getest met algen
- Leg uit hoe het ene eiwit verschilt van een ander eiwit?
- Wat is een organisme in een vroeg stadium van ontwikkeling geroepen?
- Waarom zijn strikte aërobe oxidase positief?
- Hoe is het produceren van een GM -plant anders dan dieren?
- Nieuw ontwerp van bioactieve peptide-nanovezels die zowel de temperatuuromkeerbaarheid als de stijfheid onder controle houden

- Wetenschappers maken kunstmatige katalysatoren geïnspireerd door levende enzymen

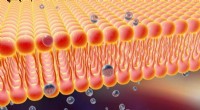
- Fluorescerende sondes bewijzen het bestaan van celmembraanstructuren van lipidenvlotten
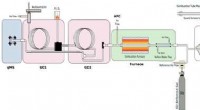
- SmartFarm-apparaat oogst luchtvochtigheid voor autonoom, zelfvoorzienende stadslandbouw

- Echte truffels opsnuiven
 Een eclips is wanneer zonlicht is?
Een eclips is wanneer zonlicht is?  Welke onderwerpen worden bestudeerd in de natuurkunde?
Welke onderwerpen worden bestudeerd in de natuurkunde?  Welke factoren hielpen atomair onderzoek vooruit?
Welke factoren hielpen atomair onderzoek vooruit?  Een snel uitbreidende Type Ia supernova explodeerde in NGC 474, studie vondsten
Een snel uitbreidende Type Ia supernova explodeerde in NGC 474, studie vondsten Hoe wordt Ignite Rock gevormd?
Hoe wordt Ignite Rock gevormd?  Veranderingen van effectieve temperatuur en koude/warme dagen boven China
Veranderingen van effectieve temperatuur en koude/warme dagen boven China Baanbrekende metingen van trillende atomen in nanostructuren luidt nieuwe technologieklasse in
Baanbrekende metingen van trillende atomen in nanostructuren luidt nieuwe technologieklasse in Leeftijdsverificatie voor toegang tot pornografie? Onderzoek toont aan dat het op veel niveaus faalt
Leeftijdsverificatie voor toegang tot pornografie? Onderzoek toont aan dat het op veel niveaus faalt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


