
Wetenschap
Elementclassificatie op het periodiek systeem begrijpen
Door Mary MacIntosh Bijgewerkt op 30 augustus 2022
Het periodiek systeem is de hoeksteen van de scheikunde en catalogiseert elk bekend chemisch element – van in de natuur voorkomende soorten tot synthetische creaties. De moderne opstelling ervan, ontwikkeld door de Russische scheikundige Dmitri Mendelejev in 1869, plaatst elementen in een raster dat wordt gedefinieerd door het atoomnummer, in plaats van de oudere ordening van het atoomgewicht.
Periodieke organisatie
In deze lay-out neemt elk element een unieke positie in op het snijpunt van een verticale groep (kolom) en een horizontale periode (rij). De zeven perioden komen overeen met opeenvolgende uitbreidingen van de elektronenschil, terwijl de 18 groepen gedeelde valentie-elektronconfiguraties weerspiegelen die analoog chemisch gedrag aandrijven.
Wetenschappelijke reden
In het hart van elk element ligt een atoom:een positief geladen kern omgeven door een wolk van elektronen. Het aantal protonen (het atoomnummer) bepaalt de identiteit van het element. Elektronen bevolken discrete schillen; de buitenste of valentieschil bepaalt hoe een element reageert. Elementen binnen dezelfde groep hebben een identiek aantal valentie-elektronen, wat hun parallelle reactiviteitspatronen verklaart. Terwijl je een periode van links naar rechts doorloopt, vullen de valentieschillen zich opeenvolgend, wat de geleidelijke verandering in eigenschappen verklaart.
Alkali- en aardalkalimetalen
Helemaal links van de tafel staan de zeer reactieve alkalimetalen (Groep 1) en daarnaast de iets minder reactieve aardalkalimetalen (Groep 2). Met uitzondering van waterstof bezitten alkalimetalen één valentie-elektron dat gemakkelijk wordt gedoneerd, waardoor ze explosief worden in lucht of water. Aardalkalimetalen, met twee valentie-elektronen, zijn iets harder, maar worden nog steeds zelden in hun elementaire vorm in de natuur aangetroffen.
Overgangsmetalen
Het centrale gebied van de grafiek (Groepen 3–12) wordt gedomineerd door overgangsmetalen. Deze elementen zijn vast bij kamertemperatuur (kwik is de enige vloeistof), vertonen een metaalachtige glans en zijn kneedbaar. Hun gedeeltelijk gevulde d-orbitalen maken een reeks oxidatietoestanden mogelijk, waardoor ze veelzijdig zijn in de katalyse en materiaalkunde. De lanthanide- en actinidereeksen, die de f-elektronenvulling vertegenwoordigen, worden traditioneel onder de hoofdtabel weergegeven.
Metalloïden en niet-metalen
Een diagonale grens scheidt het metalen blok van het niet-metalen blok. Metalloïden zoals germanium en arseen, die langs deze lijn zijn gepositioneerd, vertonen tussenliggende eigenschappen. Rechts liggen de niet-metalen:van gassen als waterstof en stikstof tot elementen als zuurstof en fluor. Deze soorten hebben doorgaans een hoge elektronegativiteit en hebben de neiging elektronen te verkrijgen om volledige valentieschillen te bereiken.
Edelgassen
Groep 18 herbergt de edelgassen:helium, neon, argon, krypton, xenon en radon. Hun buitenste schillen zijn compleet, waardoor ze extreme chemische inertie hebben. Bijgevolg blijven ze vrijwel uitsluitend in elementaire vorm en verschijnen ze als kleurloze, geurloze gassen bij standaardtemperatuur en -druk.
 430 Vs. 304 Stainless Steel
430 Vs. 304 Stainless Steel Zuren en waterstof:zure eigenschappen van water begrijpen
Zuren en waterstof:zure eigenschappen van water begrijpen  Elementen kunnen worden onderverdeeld in hoeveel blokken op basis van hun aantal elektronenorbitalen?
Elementen kunnen worden onderverdeeld in hoeveel blokken op basis van hun aantal elektronenorbitalen?  Wat is het uiterlijk van een metaal- en koolstofcombinatie?
Wat is het uiterlijk van een metaal- en koolstofcombinatie?  Wat is een verbinding die hyroniumionen in water produceert?
Wat is een verbinding die hyroniumionen in water produceert?
Hoofdlijnen
- Welke vroege vorm van een organisme waaruit latere vormen dalen?
- Een betere pinda op je bord? Nieuwe bevindingen onthullen potentieel voor gewasverbetering
- Wordt de ontwikkeling van een echte coelom tussen ectoderm en mesoderm vertegenwoordigt evolutionaire vooruitgang ten opzichte van pseudocoelomaat lichaamsplan?
- Wat is de definitie van Gregor Mendel?
- Hoe worden dieren die organellen gebruiken?
- Waarom leven sommige planten snel en sterven ze jong?
- Welke organismen die externe spijsverteringsenzymen afscheiden om dood biologisch voedsel te verteren worden genoemd?
- Paramecium is een eencellige consument Welke functies moet het uitvoeren dat multicellular niet zou uitkomen?
- Waarom hebben organismen moleculen nodig?
- Nieuw productieproces voor polymeren bespaart 10 ordes van energie

- Hoe papieren handdoeken water absorberen:de wetenschap achter hun effectiviteit

- Wetenschappers ontwikkelen kunstmatig fotosyntheseapparaat voor groenere ethyleenproductie

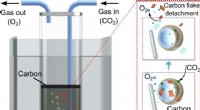
- Vloeibaar metaal bewezen goedkope en efficiënte CO2-converter
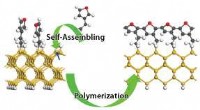
- Nieuwe route naar moleculaire draden geschikt voor gebruik in miniatuurelektronica
 Bacteriële harpoengeweer van nanoformaat werkt als een boormachine
Bacteriële harpoengeweer van nanoformaat werkt als een boormachine 5 gered van overstromingen terwijl orkaan Hawaï met regen bekogeld
5 gered van overstromingen terwijl orkaan Hawaï met regen bekogeld Welke gassen bevinden zich in de atmosfeer?
Welke gassen bevinden zich in de atmosfeer?  Wanneer werd het ruimtepak uitgevonden?
Wanneer werd het ruimtepak uitgevonden?  Tools gebruikt om materie te meten
Tools gebruikt om materie te meten  Wat zijn de apparatuur die worden gebruikt om nagelverbetering te doen?
Wat zijn de apparatuur die worden gebruikt om nagelverbetering te doen?  Een stap in de richting van metaal-organische raamwerksynthese
Een stap in de richting van metaal-organische raamwerksynthese Wat is het maximale aantal elektronen dat het derde energieniveau kan bezetten?
Wat is het maximale aantal elektronen dat het derde energieniveau kan bezetten?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

