
Wetenschap
Zuren en waterstof:zure eigenschappen van water begrijpen
Dit is waarom:
* Zuren worden gedefinieerd door hun vermogen om protonen (H+) in oplossing te doneren. Hoewel veel zuren waterstof bevatten, is dit niet de enige bepalende factor.
* Veel verbindingen die waterstof bevatten doneren geen protonen in water en zijn niet zuur. Methaan (CH4) bevat bijvoorbeeld waterstof, maar is geen zuur.
* De aanwezigheid van een zeer elektronegatief atoom (zoals zuurstof of chloor) gebonden aan waterstof is cruciaal voor de vorming van een zuur. Het elektronegatieve atoom trekt de elektronendichtheid weg van de waterstof, waardoor het waarschijnlijker wordt dat het als een proton dissocieert.
Voorbeelden:
* Zoutzuur (HCl): Bevat waterstof en is een zuur.
* Methanol (CH3OH): Bevat waterstof maar is geen zuur.
Samengevat: Hoewel veel zuren waterstof bevatten, garandeert de aanwezigheid van waterstof alleen niet dat een verbinding zuur zal zijn wanneer deze in water wordt opgelost.
 Als het verschil 0,5 is in elektronegativiteitswaarden van twee atomen, bindt dan polair of niet -polair?
Als het verschil 0,5 is in elektronegativiteitswaarden van twee atomen, bindt dan polair of niet -polair?  Wat is het enige deel van een atoom dat kan worden verwijderd of toegevoegd?
Wat is het enige deel van een atoom dat kan worden verwijderd of toegevoegd?  Hoe ziet Iron Sulphur eruit?
Hoe ziet Iron Sulphur eruit?  Leg het principe en de werking van een nucleaire reactor uit met een netjes diagram?
Leg het principe en de werking van een nucleaire reactor uit met een netjes diagram?  Gerichte evolutie om enzymen te ontwerpen die beeldvormende middelen maken voor medische diagnose
Gerichte evolutie om enzymen te ontwerpen die beeldvormende middelen maken voor medische diagnose
 Nieuwe COVID-relevante richtlijnen voor brandveiligheid en noodevacuatie voor intensive care-afdelingen voor 2021 gelanceerd
Nieuwe COVID-relevante richtlijnen voor brandveiligheid en noodevacuatie voor intensive care-afdelingen voor 2021 gelanceerd We schatten dat er tot 14 miljoen ton microplastics op de zeebodem ligt. Het is erger dan we dachten
We schatten dat er tot 14 miljoen ton microplastics op de zeebodem ligt. Het is erger dan we dachten Om droogte te voorspellen, kijk niet naar de lucht. Kijk in de grond... vanuit de ruimte
Om droogte te voorspellen, kijk niet naar de lucht. Kijk in de grond... vanuit de ruimte Rechter om argumenten te horen over pijpleidingwerk in Dakota Access
Rechter om argumenten te horen over pijpleidingwerk in Dakota Access Licht werpen op het chemische raadsel van zwaveltrioxide in de atmosfeer
Licht werpen op het chemische raadsel van zwaveltrioxide in de atmosfeer
Hoofdlijnen
- Wetenschappers maken een einde aan een vijftig jaar durend mysterie en onthullen hoe bacteriën zich kunnen verplaatsen
- Is algenvernietigerzuur of basis?
- Heeft het virus gespecialiseerde structuren of interne compartimenten?
- Wat is de volledige naam voor DNA en RNA?
- Waarom pure bacteriekweek verkrijgen uit een gemengde kweek?
- Wat wordt gesynthetiseerd door RNA -polymerase?
- Welk plantenweefsel transporteert suikeroplossing?
- Hoe je de biomassa van planten kunt stimuleren:Biologen ontdekken het moleculaire verband tussen de beschikbaarheid van voedingsstoffen en de groei
- Kunnen insecten dik worden?
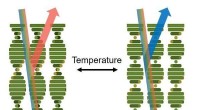
- Kleurveranderende coatings geactiveerd door temperatuurveranderingen
- Is azijn een betrouwbaar spinnenafweermiddel? Inzichten uit recent onderzoek

- Chemici ontwikkelen een nieuw milieuvriendelijk materiaal voor afvalwaterzuivering

- Microcapsules voor gerichte toediening van medicijnen, geïnspireerd op Russische pelmeni

- Verbeteren van de samenstelling van stralingsbeschermingsbrillen

 Wat is de lengte van Saturn tot zon?
Wat is de lengte van Saturn tot zon?  Beschrijf de noordelijke locatie op aarde.?
Beschrijf de noordelijke locatie op aarde.?  Hoe verandert de wetenschap de wereld?
Hoe verandert de wetenschap de wereld?  Wat is de waarde van G?
Wat is de waarde van G?  Op een dag zal onze zon stollen tot een gigantische kristallen bol
Op een dag zal onze zon stollen tot een gigantische kristallen bol Wat veroorzaakt de opbouw van elektrische lading?
Wat veroorzaakt de opbouw van elektrische lading?  Wat doet een luchtpijpcel?
Wat doet een luchtpijpcel?  Hoe wiegen werken
Hoe wiegen werken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

