
Wetenschap
Berekening van geïsoleerde opbrengst bij chemische reacties
Door Robert Schrader – Bijgewerkt op 30 augustus 2022
In de scheikunde opbrengst kwantificeert de hoeveelheid product die in een reactie wordt geproduceerd. Er wordt rekening gehouden met twee hoofdopbrengsten:de theoretische opbrengst, de maximale hoeveelheid die wordt voorspeld door de stoichiometrie, en de werkelijke of geïsoleerde opbrengst, de hoeveelheid product die u uit het reactievat terugwint. Het vergelijken van de geïsoleerde opbrengst met de theoretische opbrengst levert het percentage opbrengst op, een belangrijke maatstaf voor het evalueren van de reactie-efficiëntie.
Stap1 – Breng de vergelijking in evenwicht
Voordat u met berekeningen begint, moet u de reactie in evenwicht brengen om ervoor te zorgen dat het aantal atomen van elk element aan beide kanten hetzelfde is. De ontleding van koper(II)nitraat, Cu(NO₃)₂, kan bijvoorbeeld worden geschreven als:
2Cu(NO₃)₂→2CuO+4NO₂+O₂
In deze uitgebalanceerde vergelijking verschijnt elk element in dezelfde hoeveelheid aan de reactant- en productzijde.
Stap2 – Bepaal de molmassa
Bereken de molaire massa van de relevante vaste stoffen. Voor Cu(NO₃)₂ bedraagt de molaire massa 187,56gmol⁻¹; voor CuO is dit 79,55 gmol⁻¹. Gassen worden buiten beschouwing gelaten bij de opbrengstberekening omdat deze niet bijdragen aan de geïsoleerde massa.
Stap3 – Zet de startmassa om in mol
Als je begint met 250,04 g Cu(NO₃)₂, is het aantal mol:
250,04 g ÷ 187,56 gmol⁻¹=1,33 mol
Stap4 – Bereken het theoretische rendement
Volgens de uitgebalanceerde vergelijking produceert 2 mol Cu(NO₃)₂ 2 mol CuO. Dus 1,33 mol Cu(NO₃)₂ zou 1,33 mol CuO moeten opleveren, wat overeenkomt met:
1,33mol × 79,55gmol⁻¹=105,80g CuO (theoretische opbrengst)
Stap5 – Meet de werkelijke opbrengst en bereken het percentage opbrengst
Stel dat het experiment 63,41 g CuO oplevert. Het percentage opbrengst wordt als volgt berekend:
63,41g ÷ 105,80g=0,5993→59,93%
Benodigde materialen
- Periodiek systeem der elementen
- Wetenschappelijke rekenmachine
- Reagentia en reactieapparatuur
- Elektronische balans
TL;DR
Om de geïsoleerde opbrengst te berekenen, brengt u eerst de reactie in evenwicht, bepaalt u vervolgens de molaire massa, converteert u de uitgangsmassa naar mol, berekent u de theoretische opbrengst op basis van stoichiometrie en vergelijkt u ten slotte de gemeten massa van het product met de theoretische massa om het opbrengstpercentage te verkrijgen.
 Satelliet toont aan dat tropische storm Greg zijn vorm verliest
Satelliet toont aan dat tropische storm Greg zijn vorm verliest Centraal-Europa:droge aprilmaanden maken de weg vrij voor zomerdroogte
Centraal-Europa:droge aprilmaanden maken de weg vrij voor zomerdroogte $ 1 miljoen dode zone-wedstrijd:5 finalisten uit AUS, Californië, Ziek, New York
$ 1 miljoen dode zone-wedstrijd:5 finalisten uit AUS, Californië, Ziek, New York Gekweekte zeevruchten en vee stapelen zich anders op met behulp van alternatieve voerefficiëntiemaatregelen
Gekweekte zeevruchten en vee stapelen zich anders op met behulp van alternatieve voerefficiëntiemaatregelen Het lot van plastic in de oceanen
Het lot van plastic in de oceanen
Hoofdlijnen
- Wat zijn de functies van eiwitten in het lichaam?
- Gameten worden geproduceerd door meiose in plaats van mitose omdat?
- Welke moleculen die oplosbaar zijn, kunnen door het vetzuurgedeelte van celmembraan zonder ondersteunde celmembraan gaan?
- Wat heeft dezelfde functie als een celmembraan?
- Welke structuur van de plant is de primaire locatie van fotosynthese?
- Hoe zou jij het menselijk skelet definiëren?
- Wanneer een organisme de interne omgeving reguleert, is het dat?
- Is bacteriën een producent of consument?
- Welke dominante allelen worden beide volledig uitgedrukt in een fenotype?
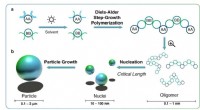
- Serendipiteitsexperiment in de achtertuin werpt licht op de productie van polymeren
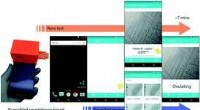
- Onderzoekers ontwikkelen op smartphone gebaseerde ovulatietest
- Bufferoplossingen beheersen:stapsgewijze handleiding voor stabiele pH-omgevingen

- Wetenschappers ontwikkelen efficiënter katalytisch materiaal voor brandstofceltoepassingen

- Koelere katalysatoren:schonere lucht voor iedereen

 Vreemde ontdekkingen kunnen helpen theorieën over de vorming van planeten te verfijnen
Vreemde ontdekkingen kunnen helpen theorieën over de vorming van planeten te verfijnen  Nieuwe tijdlijn voorgesteld voor platentektoniek
Nieuwe tijdlijn voorgesteld voor platentektoniek Verlenging van de levensduur van siliciumelektroden met hoge capaciteit in oplaadbare lithiumbatterijen
Verlenging van de levensduur van siliciumelektroden met hoge capaciteit in oplaadbare lithiumbatterijen Hoeveel structuren zijn mogelijk voor een vierkant vlakke molecuul met formule van AX2Y2?
Hoeveel structuren zijn mogelijk voor een vierkant vlakke molecuul met formule van AX2Y2?  Bekritiseert of prijst u uw collega's? Het kan afhangen van de sociale positie
Bekritiseert of prijst u uw collega's? Het kan afhangen van de sociale positie  Wat is de netto ionische vergelijking van ascorbinezuur (H2C6H6O6) en natriumhydroxide?
Wat is de netto ionische vergelijking van ascorbinezuur (H2C6H6O6) en natriumhydroxide?  Omgaan met de reproduceerbaarheidscrisis:wat kunnen ECR's eraan doen?
Omgaan met de reproduceerbaarheidscrisis:wat kunnen ECR's eraan doen? Wanneer 430 J werk wordt gedaan op een systeem, verloor het 120 energie als warmte de waarde van de waarde berekent voor dit proces?
Wanneer 430 J werk wordt gedaan op een systeem, verloor het 120 energie als warmte de waarde van de waarde berekent voor dit proces?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

