
Wetenschap
Bufferoplossingen beheersen:stapsgewijze handleiding voor stabiele pH-omgevingen
Door Carla Boulianne Bijgewerkt op 24 maart 2022
Bufferoplossingen zijn bestand tegen veranderingen in de pH omdat ze zwakke zuur-base-conjugaten bevatten die H+- en OH--ionen neutraliseren. Bufferoplossingen bestaan uit zwakke zuren of basen en het zout van dat zuur of die base. De keuze van een geschikt buffersysteem hangt af van het pH-bereik voor buffering. De meeste biologische reacties vinden plaats bij een pH-bereik van 6 tot 8. Fosfaatbuffers bufferen in het pH-bereik van 6,5 tot 7,5. Carbonzuurbuffers zijn bruikbaar bij pH 3 tot 6. Boraatbuffers functioneren van pH 8,5 tot 10. Aminozuurbuffers zoals glycine en histidine presteren over een verscheidenheid aan pH-bereiken. Tris-buffer is een van de meest gebruikte buffersystemen in biologielaboratoria. In het volgende voorbeeld worden berekeningen voor een Tris-bufferoplossing gebruikt, maar de methodologie is van toepassing op elke bufferoplossing.
Stap 1
Gebruik het product van de molariteit en het volume van de uiteindelijke oplossing om het benodigde aantal mol base te bepalen. Als er bijvoorbeeld 2 liter van een 0,1 M oplossing van Tris-buffer nodig is, dan is het benodigde aantal mol Tris:
0,1 mol/liter x 2 liter =0,2 mol Tris-base
Stap 2
Bereken de benodigde hoeveelheid buffer door het aantal benodigde mol te vermenigvuldigen met het molecuulgewicht van de base. De massa van 0,2 mol Tris-base is bijvoorbeeld gelijk aan:
0,2 mol Tris x 121,1 g/mol Tris =24,22 g Tris
Stap 3
Meet de juiste massa van de basis op een schaal.
Stap 4
Los de basis op in gedestilleerd water met behulp van een magnetische roerstaaf en een roerplaat. Los het op in een volume water dat slechts iets kleiner is dan het volume van de uiteindelijke oplossing (950 tot 975 ml voor elke liter eindoplossing). De pH van Tris-buffer verandert met de concentratie en moet opnieuw worden aangepast als een te klein aanvankelijk volume wordt gebruikt. Het is ook het beste om de buffer te bereiden op dezelfde temperatuur als tijdens de test of het experiment, aangezien Tris grote temperatuurafhankelijke pH-veranderingen heeft.
Stap 5
Titreer de waterige Tris-oplossing met 1 M zoutzuur met behulp van een pH-meter.
Stap 6
Breng de oplossing met gedestilleerd water in een maatkolf op het eindvolume.
Dingen die nodig zijn
- Gedestilleerd water
- Basispoeder of kristal
- Zoutzuur (HCl)
- Gegradueerde cilinder
- Maatkolf
- Magnetische roerstaaf
- Roerplaat
- pH-meter met sonde
- Schaal
- Rekenmachine
TL;DR (te lang; niet gelezen)
Om tijd te besparen bij het bereiden van een bufferoplossing, kunt u kant-en-klare bufferconcentraten met de vereiste pH gebruiken en verdunnen tot de gewenste molariteit en het gewenste volume.
Bereid de bufferoplossing voor op dezelfde temperatuur als deze zal worden gebruikt om aanzienlijke pH-veranderingen te voorkomen.
Vermijd tijdrovende pH-aanpassingen; titreer pas na verdunning tot de gewenste concentratie. Oplossen in een te klein volume zal leiden tot herhaalde titraties.
Waarschuwing
Wees voorzichtig bij het omgaan met zuren en basen.
Draag een veiligheidsbril.
 Welke brandwonden heter: ethanol of methanol?
Welke brandwonden heter: ethanol of methanol?  Waar wordt boor voor gebruikt?
Waar wordt boor voor gebruikt?  Wat is de uitvinding die vloeistoffen gebruikt, zijn erg koud en absorberen warmte?
Wat is de uitvinding die vloeistoffen gebruikt, zijn erg koud en absorberen warmte?  Heb je twee valentie -elektronen en ga je naar een stabiele elektronenconfiguratie met behulp van elektronen?
Heb je twee valentie -elektronen en ga je naar een stabiele elektronenconfiguratie met behulp van elektronen?  Wat zijn voorbeelden van condensatie?
Wat zijn voorbeelden van condensatie?
 Een manier om groene infrastructuur in uw stad te promoten
Een manier om groene infrastructuur in uw stad te promoten Wetenschappers gebruiken 3D-geprinte stenen, machine learning om onverwachte aardbevingen te detecteren
Wetenschappers gebruiken 3D-geprinte stenen, machine learning om onverwachte aardbevingen te detecteren Onderzoek laat zien hoe monarchvlinders het noordelijke broedgebied herkoloniseren
Onderzoek laat zien hoe monarchvlinders het noordelijke broedgebied herkoloniseren  Leg uw observatie uit in de natuur reden voor de afwezigheid van geen groene planten Diepte oceaan waar het altijd donker is?
Leg uw observatie uit in de natuur reden voor de afwezigheid van geen groene planten Diepte oceaan waar het altijd donker is?  Hoe promoot de VS onderzoek naar schone energie?
Hoe promoot de VS onderzoek naar schone energie?
Hoofdlijnen
- Welke apparatuur is nodig om micro -organismen te zien?
- Een plantencelmodel maken met een schoenendoos
- Waarom definiëren wetenschappers systemen?
- Hibiscusbestuiving:het proces en de bestuivers begrijpen
- Hoe kwantitatieve observatie is beter in de biologische methode?
- Wat is een andere naam voor een plant die zoogdier eet dat onder de zee leeft?
- Doorbraak laat zien hoe DNA wordt 'bewerkt' om genetische ziekten te corrigeren
- Wat waren Louis -bijdragen aan de microbiologie?
- Welke beschrijft hoe mRNA wordt gebruikt door een cel?
- Onder druk:eiwit-nabootsende moleculen manipuleren met hydrostatische druk
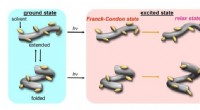
- Giftige PFAS detecteren met een sensor ter grootte van een chip

- Het aantal atomen in elk monster berekenen:een duidelijke, stapsgewijze handleiding
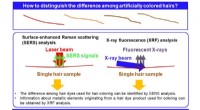
- Binnen een haarbreedte - forensische identificatie van enkel geverfde haarstreng nu mogelijk
- Onderzoekers doen nieuwe ontdekking van mechanisme voor ladingopslag

 Wanneer is snelheid belangrijk?
Wanneer is snelheid belangrijk?  Welk pH -niveau werkt catecholoxidase het beste?
Welk pH -niveau werkt catecholoxidase het beste?  Wat begint in het proces van de vorming van het zonnestelsel?
Wat begint in het proces van de vorming van het zonnestelsel?  Hoe reageren de deeltjes van materie op temperatuur?
Hoe reageren de deeltjes van materie op temperatuur?  Molariteit berekenen:bepaling van de concentratie van een LiNO3-oplossing
Molariteit berekenen:bepaling van de concentratie van een LiNO3-oplossing  Wat kunt u verwachten als u elektrisch vervoer verwacht?
Wat kunt u verwachten als u elektrisch vervoer verwacht?  Wat zijn de vijf krachten die jij gebruikt?
Wat zijn de vijf krachten die jij gebruikt?  Hoe lang was de eerste reis naar de maan?
Hoe lang was de eerste reis naar de maan?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

