
Wetenschap
Gibbs vrije energie begrijpen:de richting van de chemische reactie voorspellen
Door Andrea Becker | Bijgewerkt op 30 augustus 2022
michaeljung/iStock/Getty Images
In de meeste inleidende scheikundecursussen worden reacties weergegeven met een enkele pijl, wat een eenrichtingsproces impliceert. In werkelijkheid zijn chemische reacties omkeerbaar, en de richting die zij bevoordelen hangt af van de Gibbs-vrije energie (AG) van het systeem. Door ΔG te evalueren kunnen wetenschappers voorspellen of een reactie voorwaarts of achterwaarts zal verlopen of een evenwicht zal bereiken.
Enthalpie (ΔH)
Enthalpie vertegenwoordigt de totale energie die in een systeem is opgeslagen en die grotendeels voortkomt uit de willekeurige beweging van moleculen. Het is niet hetzelfde als potentiële energie van bindingen of kinetische energie van bulkbeweging. Enthalpie verandert wanneer warmte of arbeid wordt toegevoegd of verwijderd, en wordt beïnvloed door druk en volume, vooral in gassen.
Entropie (ΔS)
Entropie meet de mate van wanorde of willekeur in een systeem. Wanneer een systeem warmte verliest, zoals water dat tot ijs bevriest, neemt de entropie ervan af omdat de moleculen een meer geordende opstelling aannemen. Op universele schaal neemt de entropie nooit af; het heeft altijd de neiging toe te nemen.
De rol van de temperatuur
Zowel enthalpie als entropie zijn temperatuurafhankelijk. Het toevoegen van warmte verhoogt zowel ΔH als ΔS. De verandering in de vrije energie van Gibbs wordt berekend als ΔG =ΔH – TΔS, waarbij T de absolute temperatuur in Kelvin is. Omdat temperatuur de entropieterm vermenigvuldigt, kan het de balans tussen enthalpie en entropie doen doorslaan, waardoor de spontaniteit van de reactie verandert.
Implicaties voor chemische reacties
Door ΔG te onderzoeken, kunnen scheikundigen de haalbaarheid van een reactie bepalen:
- ΔG < 0 – de reactie is spontaan en verloopt in voorwaartse richting.
- ΔG > 0 – de reactie is niet-spontaan en heeft de neiging om te keren.
- ΔG = 0 – het systeem is in evenwicht; voorwaartse en achterwaartse koersen zijn gelijk.
Wanneer enthalpie en entropie tegengestelde richtingen begunstigen, wordt temperatuur de beslissende factor. Een endotherme reactie (ΔH > 0) met positieve ΔS kan bijvoorbeeld spontaan worden bij hoge temperaturen omdat de TΔS-term zwaarder weegt dan ΔH.
Door de vrije energie van Gibbs te begrijpen, kunnen onderzoekers efficiënte processen ontwerpen, reactiepaden voorspellen en industriële synthese controleren.
 Hoe het verschil tussen alligators en krokodillen te voorspellen
Hoe het verschil tussen alligators en krokodillen te voorspellen  Kopen, lenen of leasen:kunnen we heroverwegen hoe en wanneer we toegang krijgen tot huishoudelijke producten om de klimaatverandering aan te pakken?
Kopen, lenen of leasen:kunnen we heroverwegen hoe en wanneer we toegang krijgen tot huishoudelijke producten om de klimaatverandering aan te pakken?  Klimaatverandering kan derde landingsbaan Wenen niet stoppen:rechtbank
Klimaatverandering kan derde landingsbaan Wenen niet stoppen:rechtbank Wat is de setting van Sees Behind Trees?
Wat is de setting van Sees Behind Trees?  Planten en dieren in een gebied dat samen met hun omgeving functioneert?
Planten en dieren in een gebied dat samen met hun omgeving functioneert?
Hoofdlijnen
- Waar bevindt zich het grootste deel van het DNA in een eukaryotische cel?
- Hoe kun je een kern identificeren door naar cel door microscoop te kijken?
- Welke micro -organismen vereisten speciale cultuurprocedures?
- Hoe worden de afgeplatte membranen die chroloplasten worden genoemd?
- Een vasculaire plant die zich voortplant met sporen is een varen?
- Genotype uitgelegd:definitie, allelen en sleutelvoorbeelden
- Leg uit hoe water verloren gaat aan de abiotische delen van de biosfeer uit biotische delen?
- Wie is de grootste wetenschapper die ooit heeft geleefd?
- Wat wordt gevormd in rood beenmerg en zijn het meest voorkomende type witte bloedcellen?
- Een lasergestuurde programmeerbare contactloze transferdruktechniek

- Nieuw zuurvrij magneetrecyclingproces

- Nieuwe technologie heeft tot doel de levensduur van lithium-metaalbatterijen te verbeteren, veiligheid
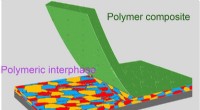
- Een nieuwe manier om lichtgevoelige medicijnen te leveren om het probleem van antibioticaresistentie te bestrijden

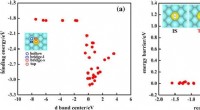
- AI zocht naar single-atom-alloy katalysatoren, 200 veelbelovende kandidaten gevonden
 Onderzoeken hoe CRISPR-Cas9 werkt:onderzoek onderzoekt de DNA-targetingdynamiek in levende cellen
Onderzoeken hoe CRISPR-Cas9 werkt:onderzoek onderzoekt de DNA-targetingdynamiek in levende cellen  DC Generator Vs. dynamo
DC Generator Vs. dynamo  Waarom wordt een plant genaamd producent en een dierlijke consument?
Waarom wordt een plant genaamd producent en een dierlijke consument?  Wat is meer vloeistof 750 ml of 1.5L?
Wat is meer vloeistof 750 ml of 1.5L?  Hoe verschilt de levenscyclus van een ster met een lage massa van de sterren van de levenscyclus met hoge massa?
Hoe verschilt de levenscyclus van een ster met een lage massa van de sterren van de levenscyclus met hoge massa?  Cephalization of Earthworms
Cephalization of Earthworms  astronomen onthullen nieuwe en raadselachtige functies van mysterieuze snelle radioflitsen
astronomen onthullen nieuwe en raadselachtige functies van mysterieuze snelle radioflitsen 5G kan digitale mensen er echt laten uitzien en echte mensen in hologrammen veranderen
5G kan digitale mensen er echt laten uitzien en echte mensen in hologrammen veranderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

