
Wetenschap
Converteer mollen naar massa in de scheikunde:een stapsgewijze handleiding
Door David Chandler
Bijgewerkt op 30 augustus 2022
In het dagelijks leven gebruiken we vaak woorden als ‘dozijn’ of ‘paar’ om hoeveelheden te beschrijven. In de scheikunde bestaat een soortgelijk concept:de mol (mol). Deze eenheid vertegenwoordigt 6,022×10 23 entiteiten, een waarde afgeleid van het exacte aantal atomen in 12 g van de isotoop koolstof-12. Met behulp van de mol kan het molecuulgewicht van een verbinding dienen als een directe conversiefactor tussen mol en gram.
Stap 1
Schrijf de chemische formule op, gevolgd door het aantal mol. De formule somt de atomen op waaruit één molecuul bestaat, bijvoorbeeld H₂O voor water. Plaats de molhoeveelheid vóór de formule en laat de eenheid weg als de waarde één is. Zo wordt 2molH₂O geschreven als 2H₂O, terwijl 1,8molH₂O wordt geschreven als 1,8molH₂O.
Stap 2
Bereken het molecuulgewicht door de atoomgewichten van alle atomen in de formule bij elkaar op te tellen. Atoomgewichten worden gegeven in het periodiek systeem. Voor water:2×1,008(⁴H)+16,00(⁸O)=18,02gmol⁻¹.
Stap 3
Vermenigvuldig het molecuulgewicht met het aantal mol om de massa te verkrijgen. Bijvoorbeeld:1molH₂O×18,02gmol⁻¹=18,02g. 2molH₂O×18,02gmol⁻¹=36,04g. Een fractie van een hoeveelheid, zoals 1,8 mol H₂O, levert 32,44 g op.
Dingen die nodig zijn
- Periodiek systeem der elementen
- Potlood
- Papier
 Onderzoekers dagen de grenzen van het moleculaire geheugen uit en openen de deur voor de ontwikkeling van moleculaire chips
Onderzoekers dagen de grenzen van het moleculaire geheugen uit en openen de deur voor de ontwikkeling van moleculaire chips  Zwavelbinding:covalente bindingen en allotropen begrijpen
Zwavelbinding:covalente bindingen en allotropen begrijpen  Wat is de elektrische geleidbaarheid van benzine?
Wat is de elektrische geleidbaarheid van benzine?  Is een verbrandingsmethode om het componentenmengsel te scheiden?
Is een verbrandingsmethode om het componentenmengsel te scheiden?  Team ontwikkelt innovatieve, ideale vloeistofafstotende oppervlakken
Team ontwikkelt innovatieve, ideale vloeistofafstotende oppervlakken
Hoofdlijnen
- Hoe reproduceren de meeste bacteriën?
- Hebben dierencellen en planten een celmembraan?
- Hebben genetische verbanden met moderne ziekten eeuwenoude voordelen opgeleverd?
- Een wetenschapper scheidt een specifiek eiwit van alle andere componenten van gistcellen. Vervolgens zoekt ze naar een klein molecuul dat bindt aan het geïsoleerde eiwit. Welk type experimenteel ontwerp is?
- Waar vindt anaërobe ademhaling plaats?
- Waar worden vezels gefermenteerd in het spijsverteringskanaal van het varken?
- Welke celafkorting voor een plaatsreacties en lipidenproducties?
- Wat is de anaërobe pot in de microbiologie?
- Wat zijn de 4 structuren die alle cellen moeten overleven?
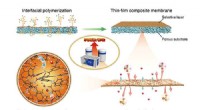
- Wetenschappers maken doorbraak in ionengeleidende composietmembranen
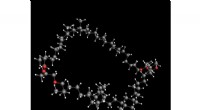
- Synthese van een van de meest voorkomende organische lipiden verheldert de structuur ervan
- Belangrijke chemische elementen in biologische cellen:de grote vier en verder

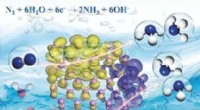
- Ammoniaksynthese door elektroreductie van stikstof op zwarte fosfor nanosheets
- Gebruik van licht voor een chemische industrie op zonne-energie

 Zijn zinkende bodems in de Everglades gerelateerd aan klimaatverandering?
Zijn zinkende bodems in de Everglades gerelateerd aan klimaatverandering? Is een glanzende substantie -metaal of niet -metaal?
Is een glanzende substantie -metaal of niet -metaal?  Waarom is de lucht blauw?
Waarom is de lucht blauw?  Hoe werken seismometers?
Hoe werken seismometers?  Waarom tandpasta en cement na verloop van tijd uitharden?
Waarom tandpasta en cement na verloop van tijd uitharden? Een negatief geladen deeltje dat vrijkomt tijdens radioactief verval?
Een negatief geladen deeltje dat vrijkomt tijdens radioactief verval?  Hoe afstanden te meten tussen hemelse lichamen?
Hoe afstanden te meten tussen hemelse lichamen?  Magnetisch met een snufje waterstof:onderzoeksteam ontwikkelt nieuw idee om de eigenschappen van ultradunne materialen te verbeteren
Magnetisch met een snufje waterstof:onderzoeksteam ontwikkelt nieuw idee om de eigenschappen van ultradunne materialen te verbeteren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

