
Wetenschap
Zwavelbinding:covalente bindingen en allotropen begrijpen
Dit is waarom:
* Elektronegativiteit: Zwavel heeft een elektronegativiteit van 2,58. Dit betekent dat het elektronen niet sterk genoeg aantrekt om ionische bindingen te vormen.
* Elektronen delen: In plaats daarvan delen zwavelatomen elektronen met elkaar om een stabiel octet (8 elektronen) in hun buitenste schil te bereiken. Deze gedeelde elektronenrangschikking creëert een covalente binding.
Zwavel bestaat in verschillende allotropen (verschillende vormen van hetzelfde element) met verschillende structuren:
* S8 (Octasulfur): De meest voorkomende vorm, bestaande uit een ring van acht zwavelatomen, verbonden door enkele covalente bindingen.
* S6 (hexazwavel): Een minder stabiele ring van zes zwavelatomen.
* S2 (Disulfur): Een diatomisch molecuul zoals zuurstof, gevormd bij hoge temperaturen.
Belangrijke opmerking: Hoewel zwavel covalente bindingen met zichzelf vormt, kan het ook covalente bindingen vormen met andere niet-metalen, zoals zuurstof in zwaveldioxide (SO2) of waterstof in waterstofsulfide (H2S).
Hoofdlijnen
- Wat neemt een organisme uit het milieu tijdens aerobe ademhaling?
- Heeft bot het zuur verlicht bij vroege landcrawlers?
- 9 Responsieve evolutie omvat organismen die evolueren in combinatie om de kansen op overleving te verbeteren Een voorbeeld van dit type is?
- Het ontsluiten van de geheimen van hoe cellen communiceren biedt inzichten in de behandeling van ziekten
- Wat is het functie -eiwit ingebed in celmembraan?
- Wat is Cellulouse?
- Welk macromolecuul wordt geassembleerd en uitgescheiden door het gladde endoplasmatisch?
- Actief transportmechanisme dat het potentiaalverschil van het membraan in stand houdt?
- Hoe passen sommige cellen in bladeren en wortels zich aan aan hun werk?
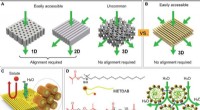
- Zelf-geassembleerd membraan met water-continue transportroutes voor nauwkeurige nanofiltratie
- Nieuwe cellulaire beeldvorming maakt de weg vrij voor kankerbehandeling
- Oorzaak van kathodedegradatie geïdentificeerd voor nikkelrijke materialen

- High-speed FM-AFM en simulatie onthullen atomaire oplossingsprocessen van calciet in water

- Onderzoekers produceren goedkope handdesinfecterende middelen uit afval

 Is mijn merkimago groen of gezond? Geen dure enquêtes nodig, vraag het maar aan Twitter
Is mijn merkimago groen of gezond? Geen dure enquêtes nodig, vraag het maar aan Twitter  Wat gebeurt er met warmtestraling wanneer het niet door een materiaal gaat, noch wordt weerspiegeld?
Wat gebeurt er met warmtestraling wanneer het niet door een materiaal gaat, noch wordt weerspiegeld?  Wat is een mogelijk voordeel van genetisch gemodificeerde gewassen?
Wat is een mogelijk voordeel van genetisch gemodificeerde gewassen?  Welke biologiewoorden beginnen met de letter y?
Welke biologiewoorden beginnen met de letter y?  Foutblock-bergen vormen zich wanneer grote blokken korst worden en gekanteld langs normale fouten?
Foutblock-bergen vormen zich wanneer grote blokken korst worden en gekanteld langs normale fouten?  Wat wordt gebruikt om calciumcarbonaat in mineralen te detecteren?
Wat wordt gebruikt om calciumcarbonaat in mineralen te detecteren?  Hoeveel voet per seconde reis je met 38 mph?
Hoeveel voet per seconde reis je met 38 mph?  Chemici creëren het eerste 2D zware fermion met zwaarder dan normale elektronen
Chemici creëren het eerste 2D zware fermion met zwaarder dan normale elektronen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


