
Wetenschap
Atomen in een diamant berekenen:een eenvoudige handleiding
* Diamanten zijn gemaakt van pure koolstof: Elke diamant is samengesteld uit koolstofatomen.
* Diamanten zijn er in verschillende maten: Een kleine diamant zal veel minder atomen hebben dan een grote diamant.
Om het aantal atomen in een diamant te berekenen, heb je het volgende nodig:
1. De massa van de diamant: Gebruik het gewicht van de diamant in gram (g).
2. De molaire massa van koolstof: Koolstof heeft een molaire massa van 12,01 g/mol. Dit betekent dat 12,01 gram koolstof 6,022 x 10^23 atomen bevat (het getal van Avogadro).
3. Een eenvoudige berekening:
* Verdeel de massa van de diamant door de molaire massa koolstof om het aantal mol koolstof te vinden.
* Vermenigvuldig het aantal mol met het getal van Avogadro om het totale aantal atomen te vinden.
Voorbeeld:
Stel dat u een diamant van 1 karaat (0,2 gram) heeft.
1. Massa: 0,2 gram
2. Molariteit van koolstof: 12,01 g/mol
3. Berekening:
* Mol koolstof =0,2 g / 12,01 g/mol =0,0167 mol
* Aantal atomen =0,0167 mol * 6,022 x 10^23 atomen/mol =1,01 x 10^22 atomen
Daarom bevat een diamant van 1 karaat ongeveer 1,01 x 10^22 koolstofatomen.
 Kun je de natuur dwingen om te sneeuwen?
Kun je de natuur dwingen om te sneeuwen?  Stormwaterbankieren kan Texas helpen overstromingen en droogtes te beheersen
Stormwaterbankieren kan Texas helpen overstromingen en droogtes te beheersen Wetenschappers onthullen nieuwe aanwijzingen over hoe de aarde aan zuurstof kwam
Wetenschappers onthullen nieuwe aanwijzingen over hoe de aarde aan zuurstof kwam Opwarming van de aarde vermindert de betrouwbaarheid van weersvoorspellingstools
Opwarming van de aarde vermindert de betrouwbaarheid van weersvoorspellingstools Satellieten leveren cruciale gegevens over gewassen tijdens COVID-19
Satellieten leveren cruciale gegevens over gewassen tijdens COVID-19
Hoofdlijnen
- Voor het eerst hebben wetenschappers levende bacteriën rechtstreeks waargenomen in poolijs en sneeuw
- Wat is de definitie van enzym?
- Wat is de stabilisatie van een enzym?
- Is het waar dat willekeurige paring tot micro-evolutie leidt?
- Noem de organisatieniveaus in de ecologie, te beginnen met de biosfeer?
- Welke biomen leven rode vossen?
- Hoe rifvissen de cyclus van de maan kunnen gebruiken om het geslacht van hun nakomelingen te manipuleren
- Hoe wordt een cultuur bijgedragen aan de moderne wetenschap?
- Chemici laten zien dat de natuur verschillende eiwitbouwstenen had kunnen gebruiken
- Onderzoekers introduceren snelle diagnostische test voor Listeria

- Vocht uit aardgas verwijderen:een technisch overzicht

- Onderzoeken naar enkelvoudige deeltjes wijzen de weg naar lichtschermen van de volgende generatie

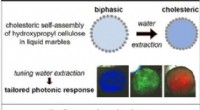
- Zelfassemblage van responsieve fotonische biobased materialen in vloeibare knikkers
- Door in een rockster-materiaal te knijpen, kan het stabiel genoeg worden voor zonnecellen

 Landbouw moet watergebruik verder laten gaan:experts
Landbouw moet watergebruik verder laten gaan:experts Egypte zegt oude begraafplaats gevonden bij beroemde piramides van Gizeh
Egypte zegt oude begraafplaats gevonden bij beroemde piramides van Gizeh Wat is de sterkte van een stroombron die gemeten is in volt?
Wat is de sterkte van een stroombron die gemeten is in volt?  Zou een CO2-belasting helpen om efficiënter energiegebruik te innoveren?
Zou een CO2-belasting helpen om efficiënter energiegebruik te innoveren? Wat voor soort energie is een transportband?
Wat voor soort energie is een transportband?  Waarom neemt potentiële energie toe hoe hoger je gaat?
Waarom neemt potentiële energie toe hoe hoger je gaat?  Afbeelding:De zon in 2020
Afbeelding:De zon in 2020 Heeft een substraatmolecuul nodig en enzymmolecuul?
Heeft een substraatmolecuul nodig en enzymmolecuul?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

