
Wetenschap
De PO-obligatie begrijpen:covalente binding uitgelegd
Dit is waarom:
* Elektronegativiteit: Zuurstof is elektronegatiever dan fosfor. Dit betekent dat zuurstof een sterkere aantrekkingskracht heeft op gedeelde elektronen.
* Elektronen delen: Zowel zuurstof als fosfor moeten elektronen winnen om een stabiele elektronenconfiguratie te bereiken. Ze bereiken dit door elektronen te delen in een covalente binding.
* Polaire covalente binding: Vanwege het verschil in elektronegativiteit brengen de gedeelde elektronen in een P-O-binding meer tijd dichter bij het zuurstofatoom door. Hierdoor ontstaat een licht negatieve lading op de zuurstof en een licht positieve lading op de fosfor, waardoor de binding polair wordt.
Voorbeelden van verbindingen waarin u P-O-obligaties kunt vinden, zijn onder meer:
* Fosforzuur (H3PO4): Dit zuur bevat drie P-O-bindingen.
* Fosfaat-ionen (PO4^3-): Deze ionen hebben vier P-O-bindingen.
* Fosfolipiden: Dit zijn belangrijke componenten van celmembranen en hebben P-O-bindingen in hun structuren.
 Stoffen met alleenstaande paren op Central Atom?
Stoffen met alleenstaande paren op Central Atom?  Wat is de chemische vergelijking voor chloorgas reageert met vaste lithiumbromide om chloride -oplossing en vloeibare broom te produceren?
Wat is de chemische vergelijking voor chloorgas reageert met vaste lithiumbromide om chloride -oplossing en vloeibare broom te produceren?  Reageert waterstof met zoutzuur?
Reageert waterstof met zoutzuur?  Kan een veelgebruikt ingrediënt in wasmiddel helpen bij het bevorderen van diabetesonderzoek?
Kan een veelgebruikt ingrediënt in wasmiddel helpen bij het bevorderen van diabetesonderzoek? Waarom veranderen vloeistoffen van volume maar gassen kunnen?
Waarom veranderen vloeistoffen van volume maar gassen kunnen?
 Hoe een doelstelling voor een project te schrijven
Hoe een doelstelling voor een project te schrijven  Vingerafdruk van oude abrupte klimaatverandering gevonden in Noordpoolgebied
Vingerafdruk van oude abrupte klimaatverandering gevonden in Noordpoolgebied Hoge niveaus van zwarte koolstof gevonden op afgelegen locatie in Siberië
Hoge niveaus van zwarte koolstof gevonden op afgelegen locatie in Siberië Bomen in de uiterwaarden van de Amazone stoten evenveel methaan uit als alle oceanen van de aarde samen
Bomen in de uiterwaarden van de Amazone stoten evenveel methaan uit als alle oceanen van de aarde samen Hoeveelheid koolstof opgeslagen in bossen neemt af naarmate het klimaat warmer wordt
Hoeveelheid koolstof opgeslagen in bossen neemt af naarmate het klimaat warmer wordt
Hoofdlijnen
- Hoe wordt de wetenschap gebruikt in een arts -baan?
- Waarom leven de meeste organismen in de netzone?
- Kill-schakelaars voor gemanipuleerde microben die schurkenstaten zijn geworden
- Hoe maakt taxonomie de biologie gemakkelijker?
- Wat is een eigenschap die wordt bestuurd door een enkel gen met twee allelen?
- Wat zijn de basisvoorwaarden die alle organismen nodig hebben om te groeien?
- Welke wetenschapper toonde aan dat planten zuurstof produceren?
- Welke microscoop zou u nodig hebben om de details in een bacterie te zien?
- Welke moleculen komt het meest voor in het menselijk lichaam?
- Op weg naar autonome materialen, onderzoekers ontwerpen patronen in zelfrijdende vloeibare kristallen

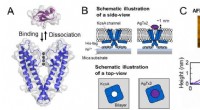
- Mechanisme van remming van schorpioentoxine van K+-kanaal opgehelderd met behulp van snelle AFM
- Nieuwe biosensor stimuleert zweet terwijl de patiënt koel is en rust

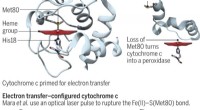
- Energetische kosten van de entatische toestand van cytochroom c gekwantificeerd
- Kleine moleculen kunnen de sleutel zijn tot het verbeteren van de efficiëntie van organische zonnecellen

 Nieuwe TSRI-methode versnelt studies naar koolhydraatbiologie
Nieuwe TSRI-methode versnelt studies naar koolhydraatbiologie Waarom beschouw je celmembraan als een semi-permeabele?
Waarom beschouw je celmembraan als een semi-permeabele?  Wat zou er gebeuren met de golflengte van een golf als de frequentie wordt gehalveerd?
Wat zou er gebeuren met de golflengte van een golf als de frequentie wordt gehalveerd?  Een nieuwe methode om polaronen in isolatoren en halfgeleiders te bestuderen
Een nieuwe methode om polaronen in isolatoren en halfgeleiders te bestuderen Welke geschikte eenheid is om de lengte van de snelweg te meten?
Welke geschikte eenheid is om de lengte van de snelweg te meten?  Wat zijn enkele voor- en nadelen van het gebruik van windenergie om elektriciteit te creëren?
Wat zijn enkele voor- en nadelen van het gebruik van windenergie om elektriciteit te creëren?  Hoe diesellocomotieven aandrijflijnen:hybride motoren, stalen wielen en geavanceerde tractie
Hoe diesellocomotieven aandrijflijnen:hybride motoren, stalen wielen en geavanceerde tractie  Hillwood wil AllianceTexas veranderen in mobiliteitsinnovatiezone voor drones, autonome voertuigen
Hillwood wil AllianceTexas veranderen in mobiliteitsinnovatiezone voor drones, autonome voertuigen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

