
Wetenschap
Aluminiumfolie en zwavelzuurreactie:chemische reactie en uitleg
Reactie:
* Aluminium (Al) + Zwavelzuur (H₂SO₄) → Aluminiumsulfaat (Al₂(SO₄)₃) + Waterstofgas (H₂)
Uitleg:
1. Aluminium is reactiever dan waterstof. Dit betekent dat het waterstof uit zijn verbinding, zwavelzuur, kan verdringen.
2. Wanneer aluminium in contact komt met zwavelzuur, verliest het elektronen en vormt aluminiumionen (Al³⁺) .
3. Deze aluminiumionen combineren met sulfaationen (SO₄²⁻) uit het zwavelzuur en vormen aluminiumsulfaat (Al₂(SO₄)₃) , een oplosbaar zout.
4. Tegelijkertijd winnen de waterstofionen (H⁺) uit het zwavelzuur elektronen en vormen waterstofgas (H₂) , die als belletjes vrijkomt.
Opmerkingen:
* U zult krachtig borrelen waarnemen als er waterstofgas vrijkomt.
* De aluminiumfolie zal oplossen geleidelijk, omdat het reageert met het zuur.
* De oplossing wordt warmer vanwege de exotherme aard van de reactie.
* Als de concentratie van het zwavelzuur hoog genoeg is, kan de oplossing er troebel uitzien door de vorming van aluminiumsulfaat.
Belangrijke opmerking:
* Deze reactie moet met voorzichtigheid worden uitgevoerd, omdat er warmte en brandbaar waterstofgas vrijkomen. Het is het beste om dit uit te voeren onder toezicht van een gekwalificeerde instructeur.
* De reactie kan worden vertraagd door een verdunde oplossing van zwavelzuur te gebruiken of door het reactiemengsel af te koelen.
Over het geheel genomen is de reactie tussen aluminiumfolie en zwavelzuur een klassieke demonstratie van de reactiviteit van metalen en de vorming van zouten en gassen.
 Wat is de moleculaire formule voor koper 1 arsenide?
Wat is de moleculaire formule voor koper 1 arsenide?  Hoe zijn fossiele brandstoffen en zure neerslagrelatie gerelateerd?
Hoe zijn fossiele brandstoffen en zure neerslagrelatie gerelateerd?  In welke toestand van materie overgang bewegen watermoleculen het minst?
In welke toestand van materie overgang bewegen watermoleculen het minst?  Berekening van de waterstofbehoefte voor koolstof-stikstofmoleculen
Berekening van de waterstofbehoefte voor koolstof-stikstofmoleculen  Bioluminescente worm met ijzeren superkrachten
Bioluminescente worm met ijzeren superkrachten
 Hoe worden woestijnplanten aangepast aan hun omgeving?
Hoe worden woestijnplanten aangepast aan hun omgeving?  Hoe wandelende takken de wrijving aanscherpen om grip te krijgen zonder te blijven plakken
Hoe wandelende takken de wrijving aanscherpen om grip te krijgen zonder te blijven plakken  Vijf belangrijke lessen die andere steden kunnen leren van de watercrisis in Kaapstad
Vijf belangrijke lessen die andere steden kunnen leren van de watercrisis in Kaapstad Waarom het koolstofvrij maken van zeevervoer misschien niet van een leien dakje gaat?
Waarom het koolstofvrij maken van zeevervoer misschien niet van een leien dakje gaat? Internationale SWOT-missie kan de voorspelling van overstromingen verbeteren
Internationale SWOT-missie kan de voorspelling van overstromingen verbeteren
Hoofdlijnen
- Wat is de term die wordt gebruikt om mRNA -vorming te beschrijven?
- Wat zijn de organellen in een plantencel?
- Waarom bestaat de opperhuid uit dode cellen?
- Er is een microklimaat nodig om een pinyonboom te laten groeien
- DNA draagt genetische informatie in zijn?
- Waarom zijn archaea en bacteriën anders dan andere koninkrijken?
- Nucleolus en endoplasmatisch reticulum:gedeelde cellulaire componenten
- Parasieten onthullen hoe de evolutie een oude nucleaire structuur heeft gevormd
- Eiwitten worden gemaakt op het wat?
- Team test de effecten van zuurstof op uranium

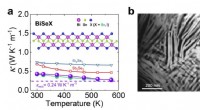
- Extreem lage thermische geleidbaarheid in 1-D zachte kettingstructuur
- Onderzoek biedt nieuwe inzichten in de behandeling van afgas van staalproductie

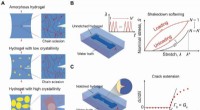
- Hydrogels tegen vermoeidheid en breuken
- Waarom sommige stoffen je warm houden:de wetenschap van thermische efficiëntie

 Extreme golven zullen groter en frequenter worden door klimaatverandering
Extreme golven zullen groter en frequenter worden door klimaatverandering Kan warmte door alle materie bewegen?
Kan warmte door alle materie bewegen?  Kan een geode in water drijven?
Kan een geode in water drijven?  Wat hebben de buitenste planeten wat de innerlijke niet hebben?
Wat hebben de buitenste planeten wat de innerlijke niet hebben?  Studie werpt licht op interacties die de manier veranderen waarop warmte en elektriciteit door microchips bewegen
Studie werpt licht op interacties die de manier veranderen waarop warmte en elektriciteit door microchips bewegen De eerste COVID-19 lockdowns verbeterden de luchtkwaliteit. Waar zijn we een jaar later?
De eerste COVID-19 lockdowns verbeterden de luchtkwaliteit. Waar zijn we een jaar later? Hoe verdun je 10 volume peroxide tot 5 peroxide?
Hoe verdun je 10 volume peroxide tot 5 peroxide?  Weerbaarheid herzien in het licht van klimaatverandering
Weerbaarheid herzien in het licht van klimaatverandering
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

