
Wetenschap
Aluminium- en zwavelzuurreactie:productie van waterstofgas
Reactie:
2 Al(s) + 3 H₂SO₄(aq) → Al₂(SO₄)₃(aq) + 3 H₂(g)
Uitleg:
* Aluminium (Al) is een reactief metaal dat gemakkelijk reageert met zuren.
* Zwavelzuur (H₂SO₄) is een sterk zuur.
* Aluminiumsulfaat (Al₂(SO₄)₃) is een oplosbaar zout dat oplost in water.
* Waterstofgas (H₂) wordt geproduceerd als bijproduct.
Wat er gebeurt:
1. Aluminiumatomen (Al) reageren met waterstofionen (H⁺) uit het zwavelzuur.
2. Aluminiumatomen verliezen elektronen en worden aluminiumionen (Al³⁺).
3. Waterstofionen nemen elektronen op en vormen waterstofgas (H₂).
4. Aluminiumionen combineren met sulfaationen (SO₄²⁻) om aluminiumsulfaat te vormen, dat oplost in water.
Belangrijkste punten:
*Deze reactie is exotherm, wat betekent dat er warmte vrijkomt.
* De reactie is krachtig en produceert belletjes waterstofgas.
* Waterstofgas is ontvlambaar, dus wees voorzichtig bij het uitvoeren van deze reactie.
 Hoe heet bos?
Hoe heet bos?  Het testen van de haalbaarheid van de VN-doelstellingen voor duurzame ontwikkeling op het gebied van water en sanitatie
Het testen van de haalbaarheid van de VN-doelstellingen voor duurzame ontwikkeling op het gebied van water en sanitatie Hoe zijn schimmels en planten vergelijkbaar?
Hoe zijn schimmels en planten vergelijkbaar?  Hoge hitte maar geen record:2018 was het 4e warmste jaar op aarde
Hoge hitte maar geen record:2018 was het 4e warmste jaar op aarde Welke bomen moeten in de buurt van een vijver worden geplant?
Welke bomen moeten in de buurt van een vijver worden geplant?
Hoofdlijnen
- Type nucleïnezuur dat van ouder tot nakomelingen overgaat en alle cellenfuncties stuurt?
- Klaar met de verkiezingen? De wetenschap legt uit hoe de politiek zo verschrikkelijk is geworden
- Nieuw inzicht in hoe het ‘opruimen’ van enzymen werkt
- Welke organellen in anafase zijn belangrijk voor het deel van de celdeling?
- Hoe maak je een celmodel van een Amoeba
- Wat zijn drie dingen die de BioShere vormen?
- Wat zijn de twee soorten haploïde cellen gemaakt in meiose?
- Hoe manukahoning infecties helpt bestrijden
- Heroverweging van rijping:Ethylenen hebben een grotere rol gespeeld in de ontwikkeling en rijping van aardbeienfruit
- Nieuwe bio-geïnspireerde dynamische materialen transformeren zichzelf
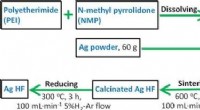
- Onderzoekers stellen een nieuwe methode voor om de elektrokatalytische omzetting van koolstofdioxide te verbeteren
- Hoe protonen, neutronen en elektronen in een isotoop te identificeren

- Doorbraak kunstmatige fotosynthese komt dichterbij

- De kernelementen van organische moleculen:koolstof, waterstof en zuurstof

 Zijn gekleurde chemische verbindingen die licht absorberen?
Zijn gekleurde chemische verbindingen die licht absorberen?  Directe herhalingen van voetbal kunnen de merkattitude van fans beïnvloeden
Directe herhalingen van voetbal kunnen de merkattitude van fans beïnvloeden Nieuwe studie ontkracht de mythe van de verloren beschaving van Cahokias Native American
Nieuwe studie ontkracht de mythe van de verloren beschaving van Cahokias Native American Wat is het mechanische voordeel voor een 2-meter lange hendel heeft een inspanning van 1,6 meter?
Wat is het mechanische voordeel voor een 2-meter lange hendel heeft een inspanning van 1,6 meter?  Wat is een waarschijnlijk product van fusiereactie?
Wat is een waarschijnlijk product van fusiereactie?  Covalente obligaties begrijpen:enkele, dubbele en drievoudige obligaties uitgelegd
Covalente obligaties begrijpen:enkele, dubbele en drievoudige obligaties uitgelegd  Waarom soorten ertoe doen
Waarom soorten ertoe doen  Vetcellen:structuur en aanpassingen voor energieopslag en -afgifte
Vetcellen:structuur en aanpassingen voor energieopslag en -afgifte
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

