
Wetenschap
Atoomstabiliteit:elementen versus verbindingen - een gedetailleerde uitleg
* Elementen: Atomen in hun elementaire vorm zijn inherent stabiel. Ze hebben een volledige buitenste elektronenschil (voor edelgassen) of een relatief stabiele configuratie. Beschouw ze als al 'inhoud'.
* Verbindingen: Atomen vormen verbindingen om een stabielere elektronenconfiguratie te bereiken, meestal door elektronen te delen of over te dragen. Dit resulteert vaak in lagere energietoestanden, wat betekent dat ze *samen* stabieler zijn dan alleen.
Voorbeelden:
* Natrium (Na): Zeer reactief als element, verliest gemakkelijk een elektron om stabiel te worden.
* Chloor (Cl): Ook reactief, verkrijgt gemakkelijk een elektron om stabiel te worden.
* Natriumchloride (NaCl): Stabiele verbinding gevormd doordat natrium een elektron verliest aan chloor, waarbij beide stabiele elektronenconfiguraties bereiken.
Het eindresultaat:
* Stabiliteit is relatief: Het hangt af van de specifieke betrokken atomen en hun individuele elektronenconfiguraties.
* Elementen kunnen stabiel zijn: Edelgassen zijn inherent stabiel als elementen.
* Verbindingen zijn vaak stabieler: Veel elementen worden stabieler door verbindingen met andere elementen te vormen.
Het gaat niet om 'stabieler', maar om de meest gunstige en stabiele toestand voor de betrokken atomen.
 Wat is de molaliteit van een oplossing bestaande uit 38,0 g rietsuiker (C12H 22O11) opgelost in 175 water?
Wat is de molaliteit van een oplossing bestaande uit 38,0 g rietsuiker (C12H 22O11) opgelost in 175 water?  Wat is de ionische vergelijking van natriumhydroxide verwarmd met ammoniumsulfaat?
Wat is de ionische vergelijking van natriumhydroxide verwarmd met ammoniumsulfaat?  Hoe wordt een koolwaterstof genaamd met Carbonyl Group aan de ene kant?
Hoe wordt een koolwaterstof genaamd met Carbonyl Group aan de ene kant?  Welke stof is een vloeistof bij 105 Celsius?
Welke stof is een vloeistof bij 105 Celsius?  Hoe zou het branden van lage zwavelkool de zuurgraad van regen beïnvloeden?
Hoe zou het branden van lage zwavelkool de zuurgraad van regen beïnvloeden?
Hoofdlijnen
- Welke organel in een eukaryotische cel is het meest merkbaar onder microscoop?
- Wat is de naam voor het lichaam van kennis verkregen door methoden op basis van systematische observatie?
- De cellen van de dunne darm begrijpen:structuur en functie
- Welke klier reguleert lichaamsfuncties of regelt andere endocriene klieren?
- Hoe classificeer je planten- en dierencellen?
- Waarom blijft de nettolading van een geïsoleerd systeem behouden?
- Evolutie:de begunstigden van massale uitsterving
- Wat zijn de twee chemische groepen die backbone van een DNA -streng vormen?
- Wat is het cumulatieve effect van twee paren genen?
- Wetenschappers onthullen nieuw dubbel-roamingmechanisme in chemische reactie

- Transparante inkt gebruiken om kleurenafbeeldingen af te drukken

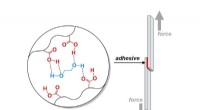
- Hoe maak je lijmen voor elektronica, voertuigen, en moeilijker bouwen?
- Grootschalig en duurzaam 3D-printen met het meest alomtegenwoordige natuurlijke materiaal

- Team ontwikkelt een familie van bio-geïnspireerde kunstmatige houtsoorten van traditionele harsen

 Welk bedrijf ontdekte Lucite?
Welk bedrijf ontdekte Lucite?  Hoe wordt het genoemd als de zon en de maan paden kruisen?
Hoe wordt het genoemd als de zon en de maan paden kruisen?  Waaruit bestaat een DNA -nucleotide?
Waaruit bestaat een DNA -nucleotide?  Inzicht in fractionele exponenten:wortels, machten en hoe u ze kunt berekenen
Inzicht in fractionele exponenten:wortels, machten en hoe u ze kunt berekenen  Wat is een belangrijk kenmerk van de wetenschappelijke methode?
Wat is een belangrijk kenmerk van de wetenschappelijke methode?  Hoe verspilt het menselijk lichaam energie-voorbeelden van het verspillen van energie?
Hoe verspilt het menselijk lichaam energie-voorbeelden van het verspillen van energie?  PARC gaat xerografisch:is dat een manier om een computer te maken?
PARC gaat xerografisch:is dat een manier om een computer te maken?  De kinetische energie van het waterstofatoomelektron is 13,65 eV Vind snelheid elektron?
De kinetische energie van het waterstofatoomelektron is 13,65 eV Vind snelheid elektron?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

