
Wetenschap
Wat is de ionische vergelijking van natriumhydroxide verwarmd met ammoniumsulfaat?
1. Schrijf de gebalanceerde moleculaire vergelijking:
2naOH (aq) + (nH₄) ₂so₄ (aq) → na₂so₄ (aq) + 2nh₃ (g) + 2h₂o (l)
2. Identificeer de oplosbare ionische verbindingen:
* NaOH (natriumhydroxide)
* (NH₄) ₂SO₄ (ammoniumsulfaat)
* Na₂so₄ (natriumsulfaat)
3. Schrijf de ionische vergelijking door de oplosbare ionische verbindingen in hun respectieve ionen af te breken:
2na⁺ (aq) + 2oH⁻ (aq) + 2nh₄⁺ (aq) + so₄²⁻ (aq) → 2na⁺ (aq) + so₄²⁻ (aq) + 2nh₃ (g) + 2h₂o (l)
4. Scheiding ionen annuleren:
Toeschouwersionen zijn de ionen die aan beide zijden van de vergelijking verschijnen en niet deelnemen aan de reactie. In dit geval zijn NA⁺ en SO₄²⁻ toeschouwersionen.
5. De laatste ionische vergelijking:
2OH⁻ (aq) + 2nh₄⁺ (aq) → 2nh₃ (g) + 2h₂o (l)
belangrijke opmerkingen:
* ammoniumhydroxide (NH₄OH) wordt niet gevormd: Hoewel het misschien intuïtief lijkt, is ammoniumhydroxide onstabiel en ontleedt gemakkelijk in ammoniakgas (NH₃) en water (H₂o).
* verwarming is cruciaal: De reactie wordt begunstigd door verwarming, omdat het het ammoniakgas af aandrijft, waardoor de reactie wordt voltooid.
Laat het me weten als je nog andere chemische vragen hebt!
 Hoe verhoudt landvormen zich tot de wetenschap?
Hoe verhoudt landvormen zich tot de wetenschap?  Cyprus:klimaatverandering, achteruitgang op het platteland verhoogt het risico op bosbranden
Cyprus:klimaatverandering, achteruitgang op het platteland verhoogt het risico op bosbranden Wat orkaan Michael ons heeft geleerd over de voorbereiding op het orkaanseizoen van dit jaar
Wat orkaan Michael ons heeft geleerd over de voorbereiding op het orkaanseizoen van dit jaar Gebouw te dicht bij het water. Het is belachelijk! Opkopen na overstromingen tonen noodzaak tot klimaatadaptatie
Gebouw te dicht bij het water. Het is belachelijk! Opkopen na overstromingen tonen noodzaak tot klimaatadaptatie Florida-schelpen zitten in heet water:kan het dieper verplaatsen van de schelpen een teruglopende populatie doen herleven?
Florida-schelpen zitten in heet water:kan het dieper verplaatsen van de schelpen een teruglopende populatie doen herleven?
Hoofdlijnen
- Vetmolecuul in menselijk bloed controleert malariaparasieten beslissing om op muggen te springen
- Wat voor soort ziekte is tyfus?
- Wat heeft Rosalind Franklin te maken met genetica?
- Wat is de bron van ribosomaal RNA rRNA?
- Hoe neuronale herkenning van zangvogelgeluiden zich in de loop van de tijd ontvouwt
- Wat is de term die wordt gebruikt om het vermogen te beschrijven, produceert een specifiek product efficiënter dan enig ander land?
- Zeebacteriën werken samen om een essentiële vitamine te produceren
- Hoe boa's zichzelf behoeden voor verstikking tijdens het insnoeren en verteren van het avondeten
- Wat zijn de dingen die wetenschap niet kan beantwoorden of doen?
- Elektrochemie spoelt antibioticaresistente eiwitten weg

- Slimme scheikunde verlost medicijnen tegen kanker van ernstige bijwerkingen
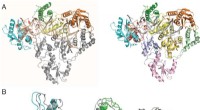
- Onderzoek onthult structuur van humane endogene reverse transcriptase
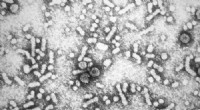
- Onderzoekers gebruiken supercomputer om inzicht te krijgen in hepatitis B
- Een duurzaam nieuw materiaal voor het afvangen van kooldioxide

 Wat absorbeert energie uit zijn omgeving?
Wat absorbeert energie uit zijn omgeving?  Hoe kun je thermische energie veranderen in kinetische energie?
Hoe kun je thermische energie veranderen in kinetische energie?  Waarom is meiose alleen voor sekscellen?
Waarom is meiose alleen voor sekscellen?  Hoe een natuurlijke verbinding uit zakpijpen kanker bestrijdt
Hoe een natuurlijke verbinding uit zakpijpen kanker bestrijdt  Wat zijn de planeten van het meest massief?
Wat zijn de planeten van het meest massief?  Wat als Homeostase mislukt?
Wat als Homeostase mislukt?  Taalsnelheid versus efficiëntie:is sneller beter?
Taalsnelheid versus efficiëntie:is sneller beter?  Hoe evoluerende landschappen de vroege migratiepatronen van First People naar Australië beïnvloedden
Hoe evoluerende landschappen de vroege migratiepatronen van First People naar Australië beïnvloedden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

