
Wetenschap
Massabehoud in chemische vergelijkingen:een gedetailleerde uitleg
Hier is hoe het werkt:
* De vergelijking in evenwicht brengen: Een uitgebalanceerde chemische vergelijking heeft hetzelfde aantal atomen van elk element aan beide zijden van de vergelijking. Dit wordt bereikt door coëfficiënten (getallen vóór de chemische formules) te plaatsen om het aantal moleculen dat bij de reactie betrokken is, aan te passen.
* Atomen blijven behouden: Omdat atomen niet kunnen worden gecreëerd of vernietigd in een chemische reactie (alleen herschikt), zorgt een uitgebalanceerde vergelijking ervoor dat het totale aantal atomen van elk element hetzelfde is voor en na de reactie.
* Massa is evenredig met atomen: Omdat de massa van een atoom constant is, moet de massa van de reactanten gelijk zijn aan de massa van de producten. Dit komt omdat de totale massa van de atomen in de reactanten gelijk is aan de totale massa van de atomen in de producten.
Voorbeeld:
Beschouw de verbranding van methaan (CH4) met zuurstof (O2) om koolstofdioxide (CO2) en water (H2O) te vormen:
CH4 + 2O2 → CO2 + 2H2O
* Reactanten: 1 koolstofatoom, 4 waterstofatomen en 4 zuurstofatomen.
* Producten: 1 koolstofatoom, 4 waterstofatomen en 4 zuurstofatomen.
De vergelijking is in evenwicht omdat het aantal atomen van elk element aan beide kanten hetzelfde is. Omdat het aantal atomen behouden blijft, moet de totale massa van de reactanten (methaan en zuurstof) gelijk zijn aan de totale massa van de producten (kooldioxide en water).
Conclusie:
Door chemische vergelijkingen in evenwicht te brengen, zorgen we ervoor dat het aantal atomen van elk element behouden blijft. Omdat atomen een constante massa hebben, impliceert dit direct dat de totale massa van de reactanten gelijk moet zijn aan de totale massa van de producten, waarmee het behoud van massa bij chemische reacties wordt aangetoond.
 Wat zijn de functies van het graslandecosysteem?
Wat zijn de functies van het graslandecosysteem?  Team laat zien hoe rivieren kruipen en stromen om landschappen in de loop van de tijd vorm te geven
Team laat zien hoe rivieren kruipen en stromen om landschappen in de loop van de tijd vorm te geven  Zwaardere regen en mest betekenen meer algenbloei
Zwaardere regen en mest betekenen meer algenbloei Gouverneur van Hawaï bezoekt degenen die de constructie van de telescoop blokkeren
Gouverneur van Hawaï bezoekt degenen die de constructie van de telescoop blokkeren Hoe een plaag zich aanpaste aan het leven in het donker
Hoe een plaag zich aanpaste aan het leven in het donker
Hoofdlijnen
- Waarom is pH biologisch belangrijk?
- De interne structuur en opstelling van het lichaam wordt genoemd?
- Wat zijn overblijfselen van structuren die belangrijke functies dienden in de voorouders van de organismen is het homoloog analoog overblijfselen of geen van beide?
- Wat hebben bacteriën nodig om te gedijen?
- Wat is de rol van DNA bij het bepalen van een eigenschappen?
- Onderzoekers presenteren nieuw wiskundig model voor het bestuderen van niercellen
- Zijn vissen de grootste atleten ter wereld?
- Wat zijn twee manieren waarop cellulaire ademhaling het tegenovergestelde is van fotosynthese?
- Hoe ratten onze koraalriffen doden
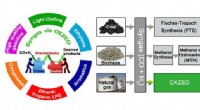
- Op oxide-zeoliet gebaseerd composietkatalysatorconcept maakt syngaschemie mogelijk die verder gaat dan Fischer-Tropsch-synthese
- Eenvoudige methode om te bepalen of noten en zuivelproducten gif bevatten

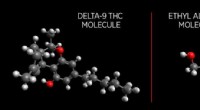
- Wetenschappers leggen de basis voor een betrouwbare marihuana-ademtester
- Zelfherstellend cement kan de geothermische industrie transformeren

- Algoritme gebruikt massaspectrometriegegevens om de identiteit van moleculen te voorspellen

 Koolhydraten:het primaire energieopslagmolecuul in levende organismen
Koolhydraten:het primaire energieopslagmolecuul in levende organismen  Hoe recombinatiefrequenties te berekenen:een praktische gids
Hoe recombinatiefrequenties te berekenen:een praktische gids  Wat zijn de beste telescopen onder de $ 200 voor amateur -astronomen?
Wat zijn de beste telescopen onder de $ 200 voor amateur -astronomen?  Energie van zichtbaar licht kan worden gemeten in georganiseerde pakketten die worden genoemd?
Energie van zichtbaar licht kan worden gemeten in georganiseerde pakketten die worden genoemd?  Wisseling van ploegen op de noordpool
Wisseling van ploegen op de noordpool Wat is het equivalent van 1 pond in metriek?
Wat is het equivalent van 1 pond in metriek?  Wat betekent een team met momentum?
Wat betekent een team met momentum?  Wat is de rol van een hart enzym?
Wat is de rol van een hart enzym?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

